Раздел для практикующего врача, назначающего лечение, наглядно демонстрирующий применение новейших научных разработок в области медицины. Статьи носят рекомендательный характер, сочетая в себе практическую информацию и научные обзоры.
Е.М. ОВСЯННИКОВА, д.м.н., Т.Ю. СТОЙКО, М.Б. ШАБАТ, поликлиника ОАО «Газпром», педиатрическое отделение №1, Москва, Н.А. КОРОВИНА, д.м.н., профессор, кафедра педиатрии Российской медицинской академии последипломного образования, Москва
Острые респираторные вирусные инфекции (ОРВИ) сопровождаются высоким риском развития осложнений и занимают значительный удельный вес в структуре заболеваемости детей. Осложнения ОРВИ, как правило, вызваны бактериальной этиологией. Лечение должно быть комплексным и включать этиотропную, симптоматическую и иммуномодулирующую терапию. Роль иммуномодулирующей терапии важна как в остром периоде заболевания, так и в периоде реконвалесценции острых респираторных заболеваний.
На протяжении последних десятилетий наблюдается рост заболеваемости детей в целом [1]. Этому способствуют неблагоприятное анте — и постнатальное развитие ребенка (недоношенность, морфофункциональная незрелость, гипотрофия, анемия, рахит, раннее искусственное вскармливание), все это приводит к различным транзиторным или стойким дефектам иммунной системы, что определяет высокую восприимчивость детей острым респираторным заболеваниям и способствуют формированию острой и хронической бронхолегочной патологии с раннего возраста. Острые респираторные вирусные инфекции (ОРВИ) сопровождаются высоким риском развития осложнений и занимают значительный удельный вес в структуре смертности детей первых трех лет жизни [1].
Частые и длительные эпизоды ОРВИ обуславливают выделение группы часто болеющих детей (ЧБД), которая составляет от 14 до 80% детской популяции. Очаги хронической инфекции носоглотки и полости рта сопровождаются дальнейшим снижением местного иммунитета и также способствуют повышению восприимчивости детей к различным инфекциям [2, 3].
Респираторные заболевания достигают 80% в структуре детских инфекционных заболеваний, среди которых значительное место занимают заболевания верхних дыхательных путей, острые бронхиты и пневмонии [4].
Осложнения ОРВИ, возникающие после вирусной инфекции, как правило, бактериальной этиологии. Чаще всего это поражение верхних дыхательных путей:
• Острый синусит обычно является осложнением ОРВИ и встречается с частотой 5—10%
• Острый средний отит, как осложнение ОРВИ, встречается в 80%
• Острый фарингит бактериальной этиологии встречается в 15—30% и вызывается бета-гемолитическим стрептококком группы А
• Как осложнения ОРВИ встречаются орбитальные осложнения синусита (флегмоны орбиты, периостит и др.) и внутричерепные осложнения (абсцесс головного мозга, синус-тромбоз)
Для вирусной инфекции в большинстве случаев характерна клиника острого простого бронхита. Как осложнение вирусной инфекции может быть острый бронхит бактериальной или внутриклеточной этиологии.
Увеличение заболеваемости острыми бронхитами приходится на весенне-осенний период, когда повышается уровень заболеваемости острыми респираторными вирусными инфекциями. Наибольшее значение в этиологии бронхитов имеют вирусы и вирусно-бактериальные ассоциации. В качестве самостоятельного этиологического фактора могут выступать бактерии, внутриклеточные возбудители и грибы [4,5].
Этиология бронхита представляет клинический интерес, так как каждый возбудитель оказывает свое повреждающее воздействие на слизистую оболочку трахеи и бронхов, тем самым определяя тяжесть и течение заболевания. Что касается бактериальной этиологии бронхитов, то на долю Haemophilus influenzae приходится от 45,9 до 48,7%, на Streptococcus pneumoniae от 16,5 до 25,5%, на Moraxella catarralis от 13,4 до 14,2% [6].
В качестве самостоятельного этиологического фактора могут выступать также внутриклеточные возбудители и грибы [6]. Наиболее частыми бактериальными возбудителями ОРЗ у детей являются Str. pneumoniae, Haemophylus influenzae, Str. pyogenes, Staph. aureus, Moraxella catarrhalis [3,4,7]. В последние годы все чаще в качестве возбудителей ОРЗ выступают микоплазмы, уреаплазмы, хламидии [5,7].
pneumoniae, Haemophylus influenzae, Str. pyogenes, Staph. aureus, Moraxella catarrhalis [3,4,7]. В последние годы все чаще в качестве возбудителей ОРЗ выступают микоплазмы, уреаплазмы, хламидии [5,7].
Возможна также смешанная вирусно-бактериальная инфекция (до 25% случаев) [7,8]. У детей в возрасте до 3 лет этиология респираторных инфекций нередко связана с несколькими возбудителями. Одним из важных компонентов патогенного воздействия респираторных вирусов является ухудшение мукоцилиарного клиренса, который облегчает продвижение бактерий в нижние отделы дыхательных путей. Одновременно с подавлением фагоцитарной активности альвеолярных макрофагов происходит блокада внутриклеточных бактерицидных процессов [7]. В результате этого создаются хорошие условия для присоединения бактериальной инфекции и формирования вирусно-бактериальных ассоциаций. Чаще всего при ОРВИ выявляется инфицирование Mycoplasma pneumonia.
В основном патогенные микроорганизмы проникают в организм через верхние дыхательные пути. Но респираторный тракт имеет систему защиты, которая препятствует фиксации микроорганизмов на слизистой, их размножению и повреждению эпителия дыхательных путей. Верхние дыхательные пути имеют мукоцилиарную и иммунную системы защиты. Мукоцилиарная защита осуществляется благодаря движению ресничек респираторного эпителия, которое обеспечивает удаление секрета вместе с микроорганизмами, проникшими в дыхательные пути. В состав секрета, кроме того, входят вещества, препятствующие адгезии бактерий и вирусов [8]. Если микроорганизмам удается преодолеть мукоцилиарный барьер и закрепиться на слизистой дыхательных путей, в процесс защиты включаются иммунные механизмы. Главными иммунными факторами защиты являются фагоцитирующие нейтрофилы и Ig AS, препятствующие фиксации и размножению возбудителей [9]. Инфекционный процесс в легких развивается, с одной стороны, в результате несостоятельности защитной системы, с другой стороны, ряд возбудителей обладают тропностью к эпителию респираторного тракта и оказывают на него сильное повреждающее действие.
Но респираторный тракт имеет систему защиты, которая препятствует фиксации микроорганизмов на слизистой, их размножению и повреждению эпителия дыхательных путей. Верхние дыхательные пути имеют мукоцилиарную и иммунную системы защиты. Мукоцилиарная защита осуществляется благодаря движению ресничек респираторного эпителия, которое обеспечивает удаление секрета вместе с микроорганизмами, проникшими в дыхательные пути. В состав секрета, кроме того, входят вещества, препятствующие адгезии бактерий и вирусов [8]. Если микроорганизмам удается преодолеть мукоцилиарный барьер и закрепиться на слизистой дыхательных путей, в процесс защиты включаются иммунные механизмы. Главными иммунными факторами защиты являются фагоцитирующие нейтрофилы и Ig AS, препятствующие фиксации и размножению возбудителей [9]. Инфекционный процесс в легких развивается, с одной стороны, в результате несостоятельности защитной системы, с другой стороны, ряд возбудителей обладают тропностью к эпителию респираторного тракта и оказывают на него сильное повреждающее действие.
Таким образом, патогенное воздействие возбудителей и недостаточная система защиты респираторного тракта приводят к развитию воспалительного процесса в трахеобронхиальном дереве, которое проявляется гиперпродукцией слизи, слущиванием поверхностных слоев эпителия и, в конечном счете, приводит к нарушению мукоцилиарного транспорта, что создает условия для скопления в дыхательных путях вязкой и густой слизи. При гиперрепродукции слизи нарушается местный иммунный ответ, что способствует дальнейшей реализации воспалительного процесса и нарушению мукоцилиарного транспорта.
Диагностика при поражении респираторного тракта
• Анамнез жизни, прививочный анамнез, анамнез заболевания
• Лабораторные исследования позволяют подтвердить предполагаемый диагноз бактериальной инфекции. Различают клинические, бактериологические, иммунологические и серологические методы исследования [10]
• Консультация пульмонолога, аллерголога
Из бактериологических методов наибольшее значение имеет культуральный метод, который заключается в заражении определенных клеток материалом, полученным от больных. Чувствительность и специфичность метода 100%-нтна, но высокая трудоемкость и себестоимость не позволяет использовать его широко.
Чувствительность и специфичность метода 100%-нтна, но высокая трудоемкость и себестоимость не позволяет использовать его широко.
Для определения антигенов указанных возбудителей используется иммуноферментный анализ и метод прямой иммунофлюоресценции.
К молекулярно-биологическим методам относится полимеразная цепная реакция, основанная на выявлении ДНК (РНК). Чувствительность и специфичность составляют 70%. Высокая себестоимость ограничивает широкое использование данного метода.
Наиболее широко используется серологический метод диагностики, основанный на определении антител классов А, G, M с помощью иммуноферментного, иммунофлюоресцентного анализа и реакции связывания комплемента [11].
Лабораторные данные не всегда при первом исследовании дают ожидаемый результат. По-прежнему остается важным анализ клинических данных в совокупности с динамикой лабораторных показателей. Приоритетными все-таки считаются клинические и инструментальные методы исследования, динамика которых позволяет не только определять степень активности инфекционного процесса, но и оценивать эффективность терапии.
В литературе встречаются указания на наличие инфицирования при различных заболеваниях. По данным Савенковой М.С., при крупе каждый шестой ребенок был инфицирован различными видами хламидий, высокая степень инфицированности была выявлена у больных бронхитом (17,4%), бронхиальной астмой (27,7%).
Нередко внутриклеточные возбудители сочетаются с бактериальной флорой или вирусной инфекцией [11]. В данном случае клиническая картина может иметь свои особенности. И решение вопроса о необходимости этиотропной терапии должно решаться только по совокупности клиники и результатов лабораторного обследования.
Для определения особенностей течения острого бронхита инфекционного генеза нами проведено клинико-инструментальное исследование 200 детей, в возрасте от 1—9 мес до 4 лет с острым простым бронхитом инфекционного генеза. Анализ результатов исследования показал, что у детей первого года жизни острый бронхит был первым у 95%, вторым — у 4%, третьим — у 1%. В группе детей старше года эпизод острого бронхита был первым у 70%, вторым — у 24%, третьим — у 5%, четвертым — у 1%. Таким образом, у большинства детей (95 и 70%) острый бронхит инфекционного генеза впервые развивается именно на первом году жизни. В тоже время у 30% детей в возрасте от года до 3 лет бронхит приобретает рецидивирующий характер, что требует особого внимания к проведению восстановительной терапии у детей, перенесших бронхит в раннем детстве и после первого эпизода заболевания проводить комплексную реабилитацию с включением иммунореабилитации.
Таким образом, у большинства детей (95 и 70%) острый бронхит инфекционного генеза впервые развивается именно на первом году жизни. В тоже время у 30% детей в возрасте от года до 3 лет бронхит приобретает рецидивирующий характер, что требует особого внимания к проведению восстановительной терапии у детей, перенесших бронхит в раннем детстве и после первого эпизода заболевания проводить комплексную реабилитацию с включением иммунореабилитации.
Установлено, что у детей первого года жизни бронхит чаще развивался при аденовирусной (24%) и при сочетании риносинцитиальной вирусной и аденовирусной этиологии (29%), реже риносинцитиальной вирусной инфекции (8%), у 4% бронхит развивался при гриппозной и парагриппозной этиологии заболевания. У детей в возрасте 2—3 лет бронхит был достоверно чаще, обусловлено это риносинцитиальной вирусной инфекцией (39%) (р < 0,005), реже аденовирусной (22%) и сочетанием риносинцитиальной и аденовирусной инфекцией (10%).
Таким образом, на основании проведенного вирусологического и бактериологического исследований установлено, что в настоящее время острый бронхит у детей раннего возраста чаще был вызван ассоциациями микроорганизмов.
Немаловажная роль в этиологии бронхитов у детей раннего возраста (24%) принадлежит внутриклеточным возбудителям, в частности Micoplasma pneumoniae. Этиологические особенности острых респираторных заболеваний определяют характер, особенности развития и течения остро бронхита у детей раннего возраста.
Течение острого бронхита микоплазменной и хламидийной этиологии имело свои клинические особенности:
• Развитию бронхита предшествовали катаральные симптомы (ринит, фарингит). В случае развития бронхита с бронхиальной обструкцией, которая развивалась на 4—5 сут. от начала заболевания
• Аускультативно преобладали мелко- и крупнопузырчатые влажные хрипы
• В рентгенологической картине отмечалось выраженное усиление интерстициального компонента легочного рисунка
• В клиническом анализе крови отмечалась тенденция к лейкоцитозу, эозинофилезу, моноцитозу по сравнению с этими показателями при бронхите вирусной этиологии (р < 0,05).
• Длительность течения бронхита данной этиологии была 9 (+- 0,99) сут., что больше, чем при вирусной этиологии.
Поскольку все случаи были расценены, как первичное инфицирование, была назначена этиотропная терапия макролидами. Всем назначался кларитромицин в дозе 7,5 мг/кг в сут. курсом 7 дней. Во всех случаях терапия была эффективной, переносилась хорошо. Побочных и нежелательных эффектов не отмечалось.
В первую очередь проводилась клиническая оценка эффективности. На 2—3-е сут. терапии отмечалось положительная динамика в аускультативной картине, уменьшалось количество хрипов и отмечалось отсутствие лихорадки.
С первого дня антибактериальной терапии назначалась иммуностимулирующая терапия Бронхо-Ваксомом детский по 1 капсуле 1 раз в сутки 10 дней. Далее в периоде реконвалесценции дети продолжали получать Бронхо-Ваксом детский по 1 капсуле 10 дней еще 2 курса с временным интервалом 20 дней между курсами.
Катамнестические наблюдения этих детей показали, что в течение месяца после перенесенного заболевания ОРЗ не болел ни один ребенок. Серологическое исследование крови на наличие АТ класса G и M в катамнезе было выполнено через 2—3 мес. после перенесенного заболевания только у 16 детей. Ни у одного не было обнаружено АТ класса G и M к хламидиям и микоплазмам в диагностически значимых титрах.
Серологическое исследование крови на наличие АТ класса G и M в катамнезе было выполнено через 2—3 мес. после перенесенного заболевания только у 16 детей. Ни у одного не было обнаружено АТ класса G и M к хламидиям и микоплазмам в диагностически значимых титрах.
Тактика ведения детей с острой респираторной патологией
Лечение должно быть комплексным и включать этиотропную, симптоматическую и иммуномодулирующую терапию.
Самочувствие больных определяется, как правило, возбудителем и этиологией заболевания. Ограничений двигательной активности также нет, наоборот, активный двигательный режим способствует восстановлению дренажной функции легких и более быстрому отхождению мокроты. При нормализации температуры и отсутствии противопоказаний детям раннего возраста показан массаж грудной клетки.
Диета при остром простом бронхите также не отличается от питания ребенка в здоровом состоянии.
Вопрос об антибактериальной терапии решается индивидуально.
Показания к системной антибактериальной терапии при ОРЗ
При неосложненном течении острого простого бронхита антибактериальная терапия не показана. Она назначается только в следующих случаях [8]:
Она назначается только в следующих случаях [8]:
• Развитие таких бактериальных процессов, как острый стрептококковый тонзиллит (фарингит), гнойный синусит, гнойный средний отит, ларингит с явлениями стеноза гортани 3-й степени, острый гнойный трахеобронхит/бронхит, бактериальная пневмония, лимфаденит, эпиглоттит, паратонзиллярный абсцесс
• Инфекция, вызванная внутриклеточными возбудителями (хламидии, микоплазмы)
• Без видимого бактериального очага (до выяснения диагноза) при наличии:
• T 0С > 38,0 > 3 дней
• одышки без обструкции
• ассиметрии хрипов
• лейкоцитоза > 15х109
В тех случаях, когда имеются показания для назначения антибактериальной терапии, выбор стартового препарата необходимо осуществлять, ориентируясь на предполагаемую этиологию возбудителя. Бактериальные трахеобронхиты и бронхиты чаще обусловлены стрептококками (в основном — пневмококком), гемофильной палочкой и моракселлой. Следует также учитывать увеличение роли внутриклеточных возбудителей (микоплазма, хламидии и др.) в этиологии инфекции нижних отделах респираторного тракта. Отсутствие терапевтического эффекта от применения стартовой антибактериальной терапии в течение 2—3 дней может быть обусловлено атипичными возбудителями. При этом препаратами выбора следует считать макролиды.
Следует также учитывать увеличение роли внутриклеточных возбудителей (микоплазма, хламидии и др.) в этиологии инфекции нижних отделах респираторного тракта. Отсутствие терапевтического эффекта от применения стартовой антибактериальной терапии в течение 2—3 дней может быть обусловлено атипичными возбудителями. При этом препаратами выбора следует считать макролиды.
Назначение иммунотропных препаратов показано при рецидивирующих и осложненных формах острых респираторных заболеваний как с лечебной, так и с профилактической целью.
Варианты иммунотерапии [12]
• Заместительная (донорские препараты Ig, цитокинов, клеток, гормонов, компонентов донорской плазмы, генов)
• Иммунодепрессия (трансплантология, аутоиммунные болезни, хроническое иммунное воспаление)
• Вакцинация (формирование иммунологической памяти)
• Специфическая иммунотерапия (АСИТ)
• Иммуномодуляция (иммуностимуляция, иммунокоррекция)
Именно иммуномодуляция приводит к «нормализации и активации собственных клеток иммунитета.
Лекарственные средства, обладающие иммунотропной активностью, в терапевтических дозах восстанавливают функции иммунной системы (эффекторную иммунную защиту). К препарату с данным механизмом действия относится бактериальный лизат Бронхо-Ваксом. С позиций современной медицины бактериальные лизаты индуцируют рецепторы врожденного иммунитета (в частности, TLR), опосредующих запуск продукции провоспалительных цитокинов и активацию гуморального и клеточного звена местного иммунитета. Захват и переработка компонентов препарата антигенпрезентирующими клетками (фагоцитами, дендритными клетками) с последующим представлением антигенных детерминант Т- и В-лимфоцитам приводит к активации адаптивного иммунитета, в т. ч. продукции специфических антител. Особенно важна для респираторной патологии стимуляция бактериальными лизатами секреции IgA, поскольку IgA занимает стратегическую позицию на поверхности слизистой оболочки и является фактором первой линии защиты.
Таким образом, бактериальные лизаты способствуют восстановлению естественной защиты дыхательных путей за счет усиления реакций врожденного и приобретенного иммунитета против наиболее распространенных респираторных патогенов.
Препарат содержит лизаты бактерий – Haemophilus influenzae, Streptococcus pneumonia, Streptococcus viridans, Streptococcus pyogens, Klebsiella pneumoniae, Klebsiella ozaenae, Staphylococcus aureus, Moraxella catarrhalis.
Именно вышеперечисленные микроорганизмы нередко являются этиологическими факторами заболеваний респираторного тракта.
Лекарственный препарат с выраженным иммуностимулирующим действием Бронхо-Ваксом способствует увеличению продукции IgА, которые секретируются слизистой оболочкой дыхательных путей, а также повышению уровня циркулирующих Т-лимфоцитов.
Только своевременная и комплексная диагностика позволяет установить правильный диагноз и определить правильную тактику ведения пациента как в остром периоде заболевания, так и выработать тактику реабилитационных мер, включая в состав, кроме общеукрепляющих мер профилактики, вакцинацию и иммунотропную терапию.
Клинический пример
Илья М. 5 лет находился в инфекционном отделении ТДГБ (Москва) с диагнозом «Острая правосторонняя верхнедолевая пневмония. Острый обструктивный бронхит, средне-тяжелое течение». ДН 1-11. В стационар доставлен бригадой скорой помощи с жалобами на лихорадку, затрудненное дыхание.
Острый обструктивный бронхит, средне-тяжелое течение». ДН 1-11. В стационар доставлен бригадой скорой помощи с жалобами на лихорадку, затрудненное дыхание.
Из анамнеза жизни известно, что ребенок от 2-й беременности, срочных родов. Данная беременность протекала на фоне токсикоза в первом триместре, анемии. Роды срочные самостоятельные. Масса тела при рождении 4 кг, длина 54 см. Закричал сразу, оценка по Апгар 8/9. К груди приложен на 1-е сутки. БЦЖ в р/доме. На грудном вскармливании, прикормы по возрасту. Период новорожденности без особенностей. Психомоторное развитие соответствует возрасту. Привит по возрасту. Аллергоанамнез не отягощен. Наследственность не отягощена. Болеет ОРВИ редко.
Эпиданамнез: кашлял отец.
Анамнез заболевания: Ребенок заболел остро 9 дней назад. Заболевание началось с субфебрильной лихорадки, ринита, покашливания. Получал симптоматическую терапию, на фоне которой состояние улучшилось. Однако на 7-й день от начала заболевания вновь отмечался подъем температуры до 38 0С, усилился кашель. На 9-й день от начала заболевания появилось затрудненное дыхание.
На 9-й день от начала заболевания появилось затрудненное дыхание.
При осмотре: Состояние средней тяжести, симптомы интоксикации выражены умеренно. Лихорадка при осмотре, температура 37,8 0С , ЧД 46, ЧСС 130.
Кожа бледная, чистая. Цианоз носогубного треугольника, усиливающийся при беспокойстве. Слизистые чистые, гиперемия в зеве.
Выражена одышка экспираторного характера. В легких дыхание жесткое, проводится во все отделы. Выслушиваются хрипы сухие с обеих сторон, в нижних отделах легких влажные средне- и мелкопузырчатые. Тоны сердца приглушены.
Живот мягкий, печень, селезенка не увеличены.
Стул без патологических примесей, диурез адекватный.
Данные лабораторного обследования:
ОАК : Hb 120, эритроциты 4,2, лейкоциты 15, сегментоядерные нейтрофилы 37, палочкоядерные нейтрофилы 2, лимфоциты 49, моноциты 10, эозинофилы 2, СОЭ 16 мм/час.
По данным общего анализа мочи, патологии не выявлено.
По данным биохимического анализа крови, все показатели (К, Nа, Са, Р, о.белок, билирубин, АЛТ, АСТ, мочевина) в пределах возрастной нормы.
Определяется инфильтративная тень в области верхней доли правого легкого. Легочный сосудистый рисунок обогащен с обеих сторон с выраженным интерстициальным компонентом.
Поставлен предварительный диагноз: Острое респираторное заболевание. Обструктивный бронхит, средне-тяжелое течение. ДН11. Правосторонняя пневмония.
При серологическом исследовании сыворотки крови были выявлены антитела класса М к Mikoplasma Pneumonia, превышающие допустимую норму (1:400).
Наличие инфильтративной тени в области верхней доли правого легкого и лабораторно выявленная микоплазменная инфекция, позволили предположить участие в этиологии данного заболевания смешанной кокковой и микоплазменной флоры.
Была назначена следующая терапия:
Ингаляции сальбутамола 3 р/сут через небулайзер.
Спирамицин в дозе 1500 млн. МЕ/10 кг в сутки, т. е. 3 млн МЕ в сутки в 2 приема.
Назначенная этиотропная терапия спирамицином была продолжена до 7 дней.
Через 3 дня терапии отмечалась положительная рентгенологическая динамика. Уменьшение интенсивности и размера инфильтрата. Сохраняется обогащение, сосудистый рисунок обогащен с обеих сторон.
С первого для АБ-терапии был назначен бактериальный лизат Бронхо-Ваксом по 1 капсуле 1 раз в день с целью иммуностимуляции.
После курса АБ-терапии (7 дней) была продолжена терапия бактериальным лизатом Бронхо-Ваксомом детский до 10 дней с последующими рекомендациями продолжить 2 цикла 10-дневной терапии Бронхо-Ваксомом по 1 капсуле 1 раз в день, с интервалами между циклами 20 дней.
Клиническое выздоровление сочеталось с нормализацией уровня антител класса IgМ и G.
Заключение по истории болезни
Данный клинический случай интересен тем, что ОРЗ смешанной этиологии – бактериально-микоплазменной, изначально имеющее клинику острой респираторной вирусной инфекции, со всеми характерными симптомами (субфебрильная лихорадка, ринит, покашливание) в дальнейшем (на 9-е сут. от начала заболевания) привело к развитию осложнения в виде острой бронхиальной обструкции и пневмонии. Данные клинического осмотра, дополненные лабораторными (лейкоцитоз в общем анализе крови, положительные титры антител к микоплазменной инфекции при серологическом исследовании) и инструментальными исследованиями (инфильтративные изменения в легких больше характерные для кокковой флоры, на фоне усиление интерстициального рисунка легких, которое характерно для микоплазменной инфекции) позволили поставить полный диагноз «Острое респираторное заболевание вирусно-бактериально-микоплазменной этиологии. Правосторонняя верхнедолевая пневмония. Обструктивный бронхит, средне-тяжелое течение». Назначенная этиопатогенетическая терапия способствовала быстрому выздоровлению.
от начала заболевания) привело к развитию осложнения в виде острой бронхиальной обструкции и пневмонии. Данные клинического осмотра, дополненные лабораторными (лейкоцитоз в общем анализе крови, положительные титры антител к микоплазменной инфекции при серологическом исследовании) и инструментальными исследованиями (инфильтративные изменения в легких больше характерные для кокковой флоры, на фоне усиление интерстициального рисунка легких, которое характерно для микоплазменной инфекции) позволили поставить полный диагноз «Острое респираторное заболевание вирусно-бактериально-микоплазменной этиологии. Правосторонняя верхнедолевая пневмония. Обструктивный бронхит, средне-тяжелое течение». Назначенная этиопатогенетическая терапия способствовала быстрому выздоровлению.
Таким образом, можно сделать вывод о том, что назначение антибактериальной терапии в сочетании с Бронхо-Ваксомом показало свою высокую активность в отношении ряда грамположительных кокков (стрептококков и пневмококков), внутриклеточных возбудителей. Данная терапия позволила совместить антибактериальный эффект с иммуномодулирующим, что способствовало выздоровлению и предотвращению рецидива.
Данная терапия позволила совместить антибактериальный эффект с иммуномодулирующим, что способствовало выздоровлению и предотвращению рецидива.
Литература
1. Альбицкий В.Ю., Баранов А.А. Часто болеющие дети. Клинико- социальные аспекты. Пути оздорвления: межвуз. сб. науч. тр. Сарат. гос. ун-т; Саратов: Изд-во Сарат. ун-та, 2006: 183.
2. Caers G. Recurrent infections of the upper respiratory tract: their medical treatment. Acta-Otorhinolaryngology-Belgium, 2003, 47(2): 221-229.
3. Острые респираторные заболевания у детей: лечение и профилактика. Научно-практическая программа, 2002.
4. Учайкин В.Ф. Руководство по инфекционным болезням у детей. М.: Гэотар Медицина, 2002: 824.
5. Коровина Н.А., Заплатников А.Л. Респираторный микоплазмоз у детей. РМЖ, 2002, 45(13-14): 560-561.
6. Савенкова М.С. Хламидийная и микоплазменная инфекции в практике педиатра. Консилиум Медикум. Приложение №1, 2005: 10-15.
7. Самсыгина Г.А. Антибиотики в лечении острых бронхитов у детей. Лечащий врач, 2001, 1: 12–15.
8. Таточенко В.К. Антибиотики при бактериальных заболеваниях дыхательных путей у детей. Респираторные заболевания в педиатрической практике, 2002, 1: 1-3.
9. Rogala B, Gluck J, Mazur B. Do the molecules CD26 and lymphocytes activation gene-3 differentiate between type 1 and 2 T cell response. J Investig Allergol Clin Immunol., 2012, 1(3): 198-203.
10. Таточенко В.К., Шамансурова Э.А. Серологическая и клиническая характеристика респираторного хламидиоза у детей первых месяцев жизни. Актуальная микробиология и клинические проблемы хламидийной инфекции, М. 1990.
11. Запруднов А.М., Мазанкова Л.Н. Хламидийная инфекция у детей: диагностика, лечение, профилактика. Российский вестник перинатологии и педиатрии, 2002, 3: 46-48.
12. Справочник Видаль. Лекарственные препараты в России. М., АстраФармСервис, 2006: 345.
Источник: Медицинский совет, № 6, 2015
Профилактика острых респираторных заболеваний у детей
О центре — Учимся быть здоровыми
04. 12.2017
12.2017
Осенне-зимний период в нашей климатической зоне всегда сопровождается подъемом заболеваемости острыми инфекционными заболеваниями, в первую очередь среди детей. В среднем каждый ребенок переносит от 3 до 5 случаев ОРЗ в год. Чаще болеют дети раннего возраста, дошкольники и младшие школьники. Рецидивирующие респираторные инфекции приводят к нарушениям функционального состояния организма, могут обуславливать срыв адаптации и вызывать развитие хронической патологии.
Факторами, влияющими на повышенную частоту ОРЗ у детей, являются: анатомо-физиологические особенности дыхательных путей, запаздывание созревания иммунной системы, социальные условия жизни, экологические характеристики места проживания. К факторам риска можно отнести и неблагоприятные жилищные условия, низкий уровень образования и культуры в семье, вредные привычки родителей, плохие взаимоотношения между супругами и частые стрессовые ситуации в семье. Особенно следует отметить «пассивное курение», приводящее к снижению иммунитета слизистой оболочки носоглотки ребенка и повышению аллергизации организма.
Особенно следует отметить «пассивное курение», приводящее к снижению иммунитета слизистой оболочки носоглотки ребенка и повышению аллергизации организма.
Профилактика острых респираторных заболеваний у детей должна быть комплексной: рациональный режим дня, оптимальное питание, регулярные закаливающие мероприятия и индивидуальная медикаментозная коррекция.
С учетом путей распространения гриппа и ОРВИ, ведущую роль в предупреждении ОРЗ играет изоляция ребенка от больного и потенциального источника инфекции. Основные меры, которые могут быть предприняты в этом отношении:
— ограничение контактов ребенка в сезоны повышения респираторной заболеваемости,
— сокращение использования городского транспорта для поездок с детьми,
— удлинение времени пребывания ребенка на воздухе,
— ношение масок членами семьи, имеющими признаки ОРЗ,
— тщательное мытье рук после контакта с больным ОРЗ или предметами ухода за ним,
— ограничение посещения детских учреждений детьми со свежими катаральными симптомами.
Основными методами повышения сопротивляемости ребенка инфекционным агентам служат вакцинация и закаливание.
Закаливание не требует очень низких температур, важна контрастность температуры и систематичность проведения процедур. Хорошо закаливают воздействия на подошвы ног, на кожу шеи, поясницы, однако для получения равномерного эффекта лучше воздействовать на кожу всего тела. Максимальная длительность холодового воздействия на ребенка не должна превышать 10-20 минут, гораздо важнее его повторность и постепенность.
Начинать закаливание надо с первых недель жизни — это воздушные ванны во время пеленания, гимнастики, перед купанием. Для этого ребенка оставляют на воздухе раздетым на несколько минут при температуре 22° C с последующим постепенным снижением ее до 20° C в возрасте 2-3 месяцев и 18° C к 4-6 месяцам.
Для закаливания следует использовать и купание: по окончании ванны уместно облить ребенка водой с температурой на 2-4° C ниже, чем вода в ванне, т. е. начать с температуры 32-34° C, снижая ее каждые 3 дня на 2-3° C. После обливания ребенка следует растереть полотенцем.
е. начать с температуры 32-34° C, снижая ее каждые 3 дня на 2-3° C. После обливания ребенка следует растереть полотенцем.
Плавание грудных детей в бассейне закаляет не столько само по себе (температура воды в нем обычно не бывает ниже 26° C), сколько в комплексе с воздушными ваннами до и после бассейна.
На втором году к обливанию после ванны (2-3 раза в неделю) можно добавить ежедневное мытье ног прохладной водой. Процедуры начинают с температуры воды 27-28° C, снижая ее каждые 1-2 дня на 2-3° C до конечной температуры 15° C (немного холоднее комнатной).
Хорошим закаливающим эффектом обладает контрастный душ: смена теплой воды (до 40° C 30-40 секунд) холодной (14-15° C) — удлиняя ее воздействие от 15-20 секунд до 30 секунд. Доводить холодовые воздействия до неприятных (т.е. применять слишком холодную воду или же оставлять ребенка под холодным душем дольше 30-40 секунд) недопустимо — не по причине возможной «простуды», а из-за опасности вызвать негативное отношение ребенка к закаливанию.
Любая закаливающая процедура должна вызывать положительные эмоции. Если ребенок «ежится», боится, его принуждать не следует. Закаливание после нетяжелого ОРЗ можно возобновить (или начать) через 7-10 дней, при заболевании с длительностью температурной реакции более 4 дней — через 2 недели, а после 10-дневной лихорадки — через 3-4 недели.
Основным методов специфической профилактики гриппа и ОРЗ является вакцинопрофилактика.
Вакцинация против гриппа обязательна на территории Российской Федерации для детей, посещающих организованные коллективы (сады, школы, вузы). При 95%-ном охвате коллективов она способна значительно снизить заболеваемость гриппом.
Заболевание гриппом у привитых протекает в более легкой форме с низким риском осложнений. Также отмечено снижение частоты ОРВИ у привитых против гриппа детей.
Прививочные реакции и осложнения при применении гриппозной вакцины, как правило, отсутствуют. Слабые реакции кратковременны (48-72 ч. ), встречаются не более чем у 3% привитых и проявляются небольшой болезненностью в месте введения вакцины. Существуют вакцины, препятствующие развитию осложнений ОРЗ (отитов, пневмоний, менингитов и энцефалитов), вызванных гемофильной палочкой (вакцина против Нib-инфекции) и пневмококковой флорой ( Пневмо 23).
), встречаются не более чем у 3% привитых и проявляются небольшой болезненностью в месте введения вакцины. Существуют вакцины, препятствующие развитию осложнений ОРЗ (отитов, пневмоний, менингитов и энцефалитов), вызванных гемофильной палочкой (вакцина против Нib-инфекции) и пневмококковой флорой ( Пневмо 23).
С целью профилактики гриппа и ОРЗ другой этиологии широко применяются интерфероны. Особо показана интерферонопрофилактика детям с тяжелым преморбидным фоном (предболезнь), только начинающим посещать детские учреждения, а также всем детям во время вспышки гриппа.
Препараты интерферона, используемые для профилактики ОРВИ: Человеческий лейкоцитарный L-интерферон, Гриппферон, Виферон (свечи, гель), Анаферон, Эргоферон.
При рецидивирующих ОРЗ в качестве иммунных стимуляторов используют бактериальные вакцины-лизаты или клеточные компоненты капсульных микроорганизмов.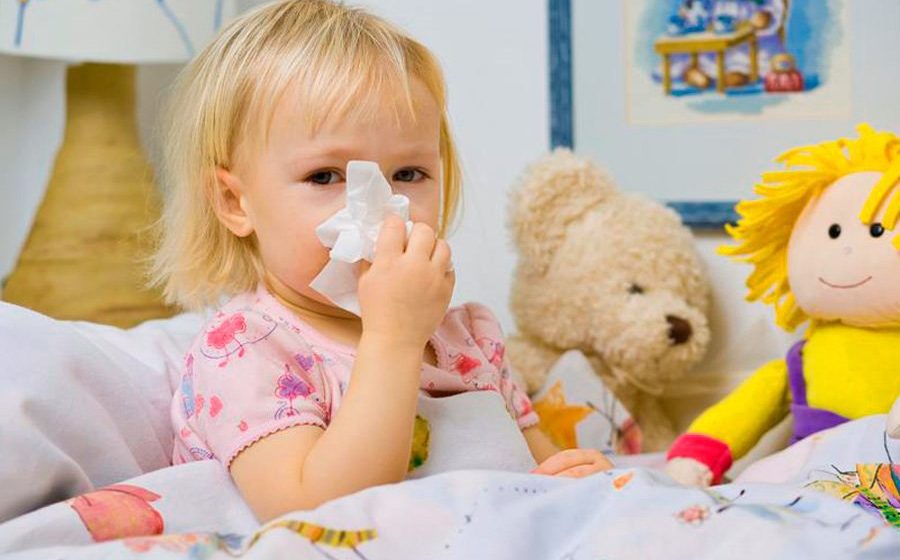 Это препараты ИРС-19, Имудон, Рибомунил, Бронхомунал, способные снижать в 2-4 раза респираторную заболеваемость детей.
Это препараты ИРС-19, Имудон, Рибомунил, Бронхомунал, способные снижать в 2-4 раза респираторную заболеваемость детей.
Профилактика антибиотиками бактериальных осложнений, чем иногда оправдывают их необоснованное применение при ОРВИ, неэффективна. Более того, подавляя рост чувствительной микрофлоры, они открывают путь для заселения дыхательных путей устойчивой флорой, повышая в 2,5 раза частоту таких осложнений, как отит и пневмония.
Заместитель начальника Медицинского центра № 3
по амбулаторно-поликлинической помощи
Ирина Петровна Семина
Профилактика и лечение частых респираторных заболеваний у детей с ослабленным иммунитетом | КЛАДОВА
1. Острые респираторные заболевания у детей: учебно-методическое пособие / С. О. Ключников и др. — М., 2009. — С. 36.
О. Ключников и др. — М., 2009. — С. 36.
2. Зайцев А.А. Лечение острых респираторных вирусных инфекций // Лечащий врач. — 2008. — No 8. — C. 42—45.
3. Regamey N. Roiha Viral etiology of acute respiratory infection with cough in infancy / N. Regamey, L. Kaiser, L. Hanna // The Pediatric Infection Disease Journal. — 2008. — No 2. — P. 100—104.
4. Identification of respiratory viruses in asymptomatic subjects / T. Jartti et al. // The Pediatric Infection Disease Journal. — 2008. — No 12. — P. 1103—1107.
5. Острые респираторные заболевания у детей: лечение и профилактика. Научно-практическая программа. Союз педиатров России. Международный фонд охраны здоровья матери и ребенка. — М., 2002. — 70 с.
— М., 2002. — 70 с.
6. Коровина Н.А. Часто болеющие дети и современные возможности иммунопрофилактики острых респираторных инфекций / Н.А. Коровина, А.Л. Заплатников // Трудный пациент. Спец. выпуск. — 2007. — С. 7—10.
7. Булгакова В.А. Современное состояние проблемы часто болеющих детей / В.А. Булгакова, И.И. Балаболкин, В.В. Ушакова // Пед. фармакология. — 2007. — Т. 4, No 2. — С. 48— 52.
8. Применение топических иммунотропных препаратов при интеркуррентных инфекциях у детей с аллергической патологией / В.А. Булгакова и др. // Пед. фармакология. — 2006. — Т. 3, No 4. — С. 56—62.
9. Федосеев Г.Б. Механизмы обструкции бронхов. — СПб.: Медицинское информационное агенство, 1995. — 336 с.
— 336 с.
10. Pavia D. Acute respiratory infections and mucociliary clearance // Europ. J. Resp. Dis. — 1987. — V. 71. — No 4. — P. 219—226.
11. Кладова О.В. Иммунопатогенез, клиника и лечение рецидивирующего крупа у детей: Автореф. дисс. … д.м.н. — М., 2003.
12. Химиопрепараты в терапии гриппа и других респираторных вирусных инфекций у детей / В.П. Дриневский и др. // Антибиотики и химиотерапия. — 1998. — Т. 43, Вып. 9. — С. 29—34.
13. Особенности вирусспецифического действия препарата арбидол. В кн: Арбидол Новые данные / И.А. Ленева и др. — М., 2004. — С. 3—8.
14. Ленева И.А. Арбидол — эффективный препарат для лечения и профилактики гриппа и ОРВИ у детей // РМЖ. — 2005. — Т. 13, No 1. — С. 72—76.
— 2005. — Т. 13, No 1. — С. 72—76.
15. Бурцева Е.И. Арбидол — специфический препарат для профилактики и лечения гриппа во время эпидемий и пандемии // Вопр. практ. педиатрии. — 2010. — Т. 5, No 1. — С. 55—59.
16. Ленева И.А., Гуськова Т.А. Арбидол — эффективный препарат для лечения и профилактики гриппа и ОРВИ: обзор результатов клинических исследований // РМЖ. — 2008. — Т. 16, No 29. — С. 3—7.
АКТУАЛЬНЫЕ АСПЕКТЫ ЛЕЧЕНИЯ ОСТРЫХ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ У ДЕТЕЙ: ПРЕПАРАТЫ ТОПИЧЕСКОГО ДЕЙСТВИЯ ПРИ РИНОФАРИНГИТЕ | Островская
1. Булгакова В. А. Острые респираторные инфекции у детей: рациональный выбор фармакотерапии. Справочник педиатра. 2011; 8: 28–37.
2. Зайцева О. В. Острый инфекционный ринит в практике врача- интерниста. Справочник поликлинического врача. 2010; 1: 34–36.
Зайцева О. В. Острый инфекционный ринит в практике врача- интерниста. Справочник поликлинического врача. 2010; 1: 34–36.
3. Острые респираторные заболевания у детей: лечение и профилактика. Научн.-практ. прогр. Союза педиатров России под ред. акад. А. А. Баранова. М. 2008.
4. Таточенко В. К. Терапия ОРЗ у детей. РМЖ. 2004; 21: 21–24.
5. Dagnelie C. F. Sore throat in general practice. A diagnostic and therapeutic study. MMW Fortschr. Med. 2011; 153 (38): 14.
6. Гончарова О. В. Программы профилактики острых респираторных инфекций у часто болеющих детей. Consilium medicum (Приложение: Педиатрия). 2010; 1: 12–16.
7. Бережной В. В. Иммунокоррекция в педиатрии. Здоровье Украины. 2004; 108: 15–19.
Бережной В. В. Иммунокоррекция в педиатрии. Здоровье Украины. 2004; 108: 15–19.
8. Василевский И. В. Иммунитет часто болеющих детей. Медицинская панорама. 2003; 1: 12–16.
9. Романцов М. Г., Ершов Ф. И. Часто болеющие дети: современная фармакотерапия. М.: ГЭОТАР-Медиа. 2006. 162 с.
10. Таточенко В. К. Антибиотико- и химиотерапия инфекций у детей. М.: Континент-Пресс. 2008. 256 с.
11. Дворецкий Л. И., Яковлев С. В. Ошибки в антибактериальной терапии инфекций дыхательных путей в амбулаторной практике. Лечащий врач. 2003; 8: 48–54.
12. Рязанцев С. В., Коцеровец В. И. Этиопатогенетическая терапия заболеваний верхних дыхательных путей и уха: Методические рекомендации. С.-Пб.: Национальный регистр. 2008. 100 с.
С.-Пб.: Национальный регистр. 2008. 100 с.
13. Tomii K., Matsumura Y., Maeda K., Kobayashi Y. Minimal use of antibiotics for acute respiratory tract infections: validity and patient satisfaction. Intern. Med. 2007; 46 (6): 267–272.
14. Овчинников А. Ю. «Трудный» пациент, или о некоторых причинах неэффективной антимикробной терапии больных инфекционным риносинуситом. Справочник поликлинического врача. 2010; 9: 56–57.
15. World Health Organization. Cough and cold remedies for the treatment of acute respiratory infections in young children. WHO/FCH/CAH/01.02. WHO. 2001.
16. Лопатин А. С. Лечение острого и хронического фарингита. РМЖ. 2001; 9 (16–17): 33–36.
17. Маркова Т. П., Чувиров Д. Г. Лечение и профилактика воспа- лительных заболеваний слизистой оболочки полости рта и глотки у детей. М. 2002. С. 52–59.
Маркова Т. П., Чувиров Д. Г. Лечение и профилактика воспа- лительных заболеваний слизистой оболочки полости рта и глотки у детей. М. 2002. С. 52–59.
18. Klimek L., Schottler S., Grevers G. Differential diagnosis and therapeutic options in acute sore throat. CMAJ. 2011; 63 (5): 113–114.
19. Chiappini E., Principi N., Mansi N., Serra A., De Masi S. Management of acute pharyngitis in children: summary of the Italian National Institute of Health guidelines. Clin. Ther. 2012; 34 (6): 1442–1458.
20. Рябова М. А. Кашель — междисциплинарная проблема. Взгляд оториноларинголога. Лечащий врач. 2010; 9: 14–18.
21. Морозова С. В. Актуальные вопросы дифференциальной диагностики и лечения острых фарингеальных инфекционно-воспалительных заболеваний. Лечащий врач. 2010; 3: 72–74.
Лечащий врач. 2010; 3: 72–74.
22. Сидоренко С. В., Гучев И. А. Тонзиллофарингит: вопросы диаг ностики и антибактериальной терапии. Consilium medicum (Приложение: Инфекции и антимикробная терапия). 2004; 4: 36–38.
23. Pelucchi C., Grigoryan L., Galeone C., Esposito S. Guideline for the management of acute sore throat. Clin. Microbiol. Infect. 2012; 18 (1): 1–28.
24. Васяева А. А., Арефьева Н. А. Иммунотерапия при хронических фарингитах: показания, результаты. РМЖ. 2010; 30: 1864.
25. Рябова М. А. Боль в горле. Участковый терапевт. 2010; 2: 18–19.
26. Субботина М. В. Боль в горле: возможные причины, диагностика и лечение. Лечащий врач. 2010; 9: 36–41.
Лечащий врач. 2010; 9: 36–41.
27. Милованова О. А., Бегашева О. И. Лечение болевых синдромов у детей. РМЖ. 2006; 3: 33–34.
28. Павленко Н. С. Эпидемиология болевых синдромов у детей и подростков. Медицина неотложных состояний. 2007; 6 (13): 12–19. 29. Кунельская Н. Л., Туровский А. Б., Кудрявцева Ю. С. Ангины: диагностика и лечение. РМЖ. 2010; 7: 438.
29. Church A., Evans P., Pickford M. et al. Scintigraphy: an appropriate methodology to assess the effectiveness of medication formats in providing local delivery to the mouth and throat. Annual Scientific Meeting of the British Pain Society. Glasgow, UK. 2007.
30. Marshall S. Giving advice on sore throats. Pharm. J. 2008; 280: 127–130.
31. Wade A. G., Marshall L. E., Simpson M., Shephard A. Bioavailability and efficacy of active lozenges in the relief of sore throat pain. Poster presented at the Annual Scientific Meetings of The British Pain Society. Glasgow, UK. 2007.
32. Wade A. G. A randomized, double-blind parallel-group, placebocontrolled, multiple-dose study of the efficacy of Strepsils lozenges in the relief of acute sore throat. In: Oxford J. S. (ed.). Developments in acute sore throat relief efficacy and sensorial benefits of medicated lozenges. Royal society of Medicine Press Ltd. 2008. P. 22–32.
33. Солдатский Ю. Л., Онуфриева Е. К., Гаспарян С. Ф., Щепин Н. В. Выбор оптимального средства для местного лечения фарингита у детей. Вопр. совр. педиатрии. 2012; 11 (2): 84–87.
34. Официальная инструкция по использованию препарата Стрепсилс для детей с 5 лет. Интернет-ресурс: www.medi.ru.
35. Oxford J. S., Leuwer M. Acute sore throat revisited: clinical and experimental evidence for the efficacy of over-the-counter AMC/DCBA throat lozenges. Int. J. Clin. Pract. 2011; 65 (5): 524–530.
36. McNally D., Simpson M., Morris C., Shephard A., Goulder M. Rapid relief of acute sore throat with AMC/DCBA throat lozenges: randomised controlled trial. Int. J. Clin. Pract. 2010; 64: 194–207.
37. RSV, SARS-assoziiertes Coronavirus, Influenza-A-Virus. A throat lozenge containing amylmetacresol and dichlorobenzyl alcohol has a direct virucidal effect on respiratory syncytial virus, influenza A and SARS-CoV. Antivir. Chem. Chemother. 2005; 16: 129–134.
Antivir. Chem. Chemother. 2005; 16: 129–134.
РЕКУРРЕНТНЫЕ РЕСПИРАТОРНЫЕ ЗАБОЛЕВАНИЯ У ДЕТЕЙ И СОСТОЯНИЕ ГУМОРАЛЬНОГО ИММУНИТЕТА | Лебеденко
1. Самсыгина Г.А. О рецидивирующей инфекции респираторного тракта у детей / Г.А. Самсыгина // Педиатрия. Журнал им. Г.Н. Сперанского. – 2012. – Т. 91, №2. – С. 6-8.
2. Кузнецова М.Н. Особенности заболеваемости детей дошкольного возраста и связь с носительством условно-патогенной микрофлоры / М.Н. Кузнецова, Л.К. Катосова, Е.Л. Королькова, О.А. Пономаренко // Российский педиатрический журнал. – 2010. – №5. – С. 53-56.
3. Охотнікова О.М. Сучасні аспекти імунопрофілактики рекурентних гострих респіраторних інфекцій у дітей /
4. О.М. Охотнікова // Мистецтво лікування. – 2010. – №6 (72). – С. 42-47.
О.М. Охотнікова // Мистецтво лікування. – 2010. – №6 (72). – С. 42-47.
5. Крамарев С.А. Результаты исследования эффективности препарата афлубин при острых респираторных инфекциях у детей / С.А. Крамарев, А.П. Мощич // Современная педиатрия. – 2011. – №3 (37). – С. 28-31.
6. Coexistenseof (Partial) Immune Defectsand Riskof Recurrent Respiratory Infections / X. Bossuyt, L. Moens, VanHoeyveld [etal.] // ClinicalChemistry. – 2007. – №53. – Р. 124-130.
7. Третьякова Н.М. Факторы риска развития и состояние общей реактивности у детей с рецидивирующими респираторными заболеваниями / Н.М. Третьякова, И.Н. Гаймоленко, О.А. Тихоненко, М.В. Максименя // Забайкальский медицинский вестник. – 2010. – №1. – С.23-26.
8. Юлиш. Е.И. Подходы к терапии острых респираторных заболеваний у часто и длительно болеющих детей / Е.И. Юлиш, Б.И. Кривушев, С.Я. Ярошенко // Здоровье ребенка. – 2011. − №2 (29). – С. 85-89.
Юлиш. Е.И. Подходы к терапии острых респираторных заболеваний у часто и длительно болеющих детей / Е.И. Юлиш, Б.И. Кривушев, С.Я. Ярошенко // Здоровье ребенка. – 2011. − №2 (29). – С. 85-89.
9. Шабалдина Е.В. Роль сенсибилизации к инфекционным агентам в патогенезе рецидивирования острых респираторных инфекций у детей младшего возраста / Е.В. Шабалдина, Н.Е. Кутенкова, А.В. Шабалдин [и др.] // Педиатрия. Журнал им. Г.Н. Сперанского. – 2013. – Т. 92, №1. – С. 30-39.
Профилактика ОРВИ у часто болеющих детей
Самыми распространенными болезнями среди людей являются острые респираторные заболевания (ОРЗ). ОРЗ, вызванное вирусами, называют острыми респираторными вирусными инфекциями (ОРВИ), которые в 95% случаях вызываются респираторными вирусами.
Практически на земле не найдется человека, который бы не болел ими в детстве или в зрелом возрасте. С ОРВИ связано 30-50% потерь рабочего времени у взрослых и 60-80% пропусков школьных занятий у детей.
С ОРВИ связано 30-50% потерь рабочего времени у взрослых и 60-80% пропусков школьных занятий у детей.
К сожалению ОРВИ могут поражать одного и того же ребенка в течение «простудного сезона» не единожды, и таких детей становится все больше. Они относятся к группе так называемых «часто и длительно болеющих детей» (ЧДБ) и находятся на диспансерном наблюдении. Но слудует отметить, что ЧДБ – это не заболевание и не диагноз. В каждом конкретном случае следует выяснить причину частых респираторных инфекций у ребенка, так как от этого зависит комплекс мероприятий его реабилитационной программы.
Что представляют собой ОРВИ и причина их возникновения
Острые респираторные вирусные инфекции (ОРВИ) – это группа заболеваний, в которую входят: грипп, парагрипп, аденовирусная, риновирусная, реовирусная, коронавирусная инфекции, характеризующиеся коротким инкубационным периодом, непродолжительными лихорадкой и интоксикацией, поражением различных отделов респираторного тракта.
Возбудителями ОРВИ являются различные вирусы. Известно более 200 респираторных вирусов. В основном они поражают верхние дыхательные пути (нос, глотку, гортань, трахею), однако у детей раннего возраста во время эпидемий возникают бронхиты и пневмонии.
Каждый из видов ОРВИ имеет своего возбудителя и свои особенности протекания.
Риновирусная инфекция — считается основной причиной банальной простуды. Чаще всего протекает легко и специального лечения не требует.
Коронавирусная инфекция — протекает аналогично риновирусной инфекции, однако продолжительность заболевания несколько меньше (6-7суток).
Аденовирусная инфекция — этому виду заболевания подвержены в основном дети, в том числе грудные. Часто сопровождается симптомами конъюнктивита (ощущение песка в глазах, покраснение, слезотечение).
Парагрипп — частыми симптомами парагриппа являются боль в горле, осиплость, лающий кашель.
Причин возникновения ОРВИ множество, основные из них следующие:
- значительная распространенность вирусов в природе и большое количество видов (серотипов) каждого из них;
- повышенная восприимчивость детей (особенно раннего возраста) к возбудителям респираторных инфекций. Чувствительность ребенка к различным вирусам в значительной мере определяется пассивным иммунитетом, который мать передает ребенку во время беременности (через плаценту), а также с грудным молоком. Если же ребенок находится на искусственном вскармливании, то материнской защиты хватает лишь на первые 2-3 месяца жизни. Потом малыш остается практически беззащитным перед группой ОРВИ, поскольку его иммунная система еще не сформирована полностью, а потому противодействие вирусам будет слабым;
- наследственная предрасположенность к ОРВИ, характеризующаяся наличием у ребенка с рождения каких-либо «малых аномалий» иммунитета;
- влияние неблагоприятных экологических и социальных воздействий достаточно быстро истощают иммунную систему ребенка — различные загрязнители внешней среды (ксенобиотики – вещества промышленного производства, отходы, загрязнения, лекарства, пестециды), оказывающие вредное воздействие на организм;
- частые психоэмоциональные стрессы;
- нерациональное питание;
- недостаточность витаминов и микроэлементов в пищевом рационе;
- социальная и экономическая нестабильность семьи;
- наличие хронических очагов инфекции у ребенка (хронический тонзиллит, аденоиды, кариозные зубы и т.
 д.), способствующих напряжению иммунной системы и приводящих к развитию вторичных иммунодефицитных состояний, что способствует хронизации инфекции, особенно вирусной (чаще герпетической).
д.), способствующих напряжению иммунной системы и приводящих к развитию вторичных иммунодефицитных состояний, что способствует хронизации инфекции, особенно вирусной (чаще герпетической).
Источники инфекций, пути передачи и течение болезни
Источником инфекции выступает больной человек, который выделяет вирусы в окружающую среду, а поэтому он опасен для окружающих. Максимальное выделение вирусов больным длится 2-3 дня. Но до седьмого дня, при неосложненном течении ОРВИ, и к четырнадцатому — в осложненных случаях, больной остается опасным для окружающих в плане заражения.
Кроме того, для детей источником инфекции могут быть взрослые, которые переносят болезнь «на ногах». Вирусоносителями становятся также дети с хроническими очагами инфекции, поскольку в случае заболевания они более длительно выделяют вирусы.
Путь передачи ОРВИ — воздушно-капельный. Во время кашля, чихания, а также с выделениями из носа вирусы из дыхательных путей больного попадают в воздух, а дальше в органы дыхания лиц, которые контактируют с больным.
Во время кашля, чихания, а также с выделениями из носа вирусы из дыхательных путей больного попадают в воздух, а дальше в органы дыхания лиц, которые контактируют с больным.
Из всех ОРВИ наибольшую опасность для организма ребенка своими осложнениями представляет грипп.
Болезнь начинается внезапно, и первым признаком является повышение температуры тела. В первые же часы температура достигает 39-41о и держится на протяжении нескольких дней. У детей первого года жизни повышение температуры может сопровождаться рвотой, общим беспокойством. Для гриппа характерны и такие признаки, как сильная головная боль, слезотечение, боль в мышцах, горле, заложенность носа, охриплость голоса, общее недомогание. В дальнейшем больного может тревожить частый сухой и болезненный кашель, который через 2-3 дня приобретает влажный характер.
Течение гриппа у детей грудного возраста имеет определенные особенности. Температура достигает максимума на вторые сутки заболевания, сопровождается двигательным беспокойством, раздражимостью, нарушением сна, отказом от груди, покашливанием. Ребенок дышит полуоткрытым ртом, сопит носиком. Нередко вздувается животик, стул частый, жидкий, с примесями слизи.
Ребенок дышит полуоткрытым ртом, сопит носиком. Нередко вздувается животик, стул частый, жидкий, с примесями слизи.
Заболеваемость парагриппом по большей части характерна для детей первого года жизни. Первые симптомы это появление незначительного кашля, изменение голоса, нарушение носового дыхания, повышение температуры тела. Кашель имеет стойкий характер, но остается сухим и грубым. В среднем на 2-3 день заболевания возможно ухудшение состояния ребенка: в ночное время возникает грубый, приступоподобный кашель («лающий»), с длительным шумным вдохом, который сопровождается отдышкой.
Аденовирусная инфекция представляет не меньшую опасность для организма ребенка при несвоевременном лечении. Она имеет острое начало с повышением температуры тела до 38-39о. Одновременно появляется вялость ребенка, быстрая утомляемость, сонливость, снижение аппетита, насморк (с первых же дней избыточные водянистые выделения). Течение аденовирусной инфекции сопровождается увеличением миндалин и шейных лимфатических узлов.
Все перечисленные ОРВИ не столь опасны, если они своевременно выявлены и начато лечение. В противном случае не исключены осложнения, перерастающие в хроническую форму; осложнения в первую очередь касаются органов дыхания. 60% осложнений составляют пневмонии, поражения нервной системы (энцефаломиелиты) — 0.3-3%, патология ЛОР-органов — 1%, воспаление сердечной мышцы до 1%.
Лечения ОРВИ при несложных формах осуществляется в основном в домашних условиях при строгом выполнении рекомендаций лечащего врача.
- Должен соблюдаться спокойный полупостельный режим при регулярном проветривании комнаты больного.
- Обильное теплое питье (не менее 2л в сутки), лучше богатое витамином С — чай с лимоном, настой шиповника, морс.
Профилактика заболеваний ОРВИ у ЧДБ
Наилучшей системой профилактики острых респираторных заболеваний у часто и длительно болеющих детей является формирование у них стойкого иммунитета к болезням. Этому способствуют:
Этому способствуют:
- здоровый образ жизни;
- рациональный режим дня;
- полноценное питание;
- разнообразные программы закаливания;
- ограничение контактов ребенка с больными гриппом и ОРВИ;
- проведение санитарно-гигиенических мероприятий;
- одежда ребенка должна соответствовать его возрасту (быть по размеру) и погодным условиям;
- сокращение использования городского транспорта и удлинение времени пребывания ребенка на воздухе;
- исключение пассивного курения;
- в случае наличия у ребенка очагов хронической инфекции (хронический тонзиллит, аденоидит, кариес и др.) они должны быть санированы;
- закаливание ребенка (как основного метода повышения сопротивляемости организма различным инфекциям) должно начинаться с самого раннего детства;
- проведение профилактических прививок в соответствии с возрастом ребенка;
- использование адаптогенов (по рекомендации врача).

Систематическое контрастное воздушное или водное закаливание сопровождается повышением устойчивости организма к температурным колебаниям окружающей среды и повышением иммунологической реактивности организма. Закаливание не требует очень низких температур, важна контрастность воздействия и систематичность процедур. Максимальная деятельность закаливающих процедур не должна превышать 10-20 минут. Закаливающие процедуры хорошо сочетать с проведением гимнастики и массажа грудной клетки.
Из средств неспецифической профилактики хорошо известны такие растения как: китайский лимонник, элеутерококк, женьшень, эхинацея, левзея.
Нередко возникает вопрос о возможности и целесообразности проведения календарной вакцинации или гриппозной прививки детям, получающим лечение бактериальными вакцинами. Специальными исследованиями было доказано, что вакцинация часто болеющих детей является одним из самых важных профилактических мероприятий, поскольку частые ОРВИ у этой группы детей не свидетельствуют о наличии иммунодефицита, они не могут быть поводом для отвода от прививок.
Родителям часто болеющих детей необходимо знать и помнить, что их дети нуждаются в проведении регулярных комплексных профилактических мероприятий, а при развитии острой респираторной инфекции – в своевременной и адекватной терапии,
а самое главное – в постоянном родительском внимании к своим детям!
Автор: Некрасова О.В., главный педиатр комитета по здравоохранению Мингорисполкома
Редактор: Арский Ю.М.
Компьютерная верстка и оформление: Згирская И.А.
Ответственный за выпуск: Тарашкевич И.И.
Комитет по здравоохранению Мингорисполкома
Городской Центр здоровьяЛечение гриппа и острых респираторных вирусных инфекций у детей
С. А. Крамарев,Национальный медицинский университет имени А.А. Богомольца, г. Киев
А. Крамарев,Национальный медицинский университет имени А.А. Богомольца, г. Киев
Сегодня известно более 200 возбудителей, которые способны вызывать сходные клинические симптомы со стороны верхних дыхательных путей. В 80-90% случаев ОРВИ у детей вызываются вирусами гриппа и парагриппа, аденовирусами, респираторно-синцитиальными вирусами.
 В связи с этим
первоочередное значение в этиотропном лечении ОРВИ имеют
противовирусные лекарственные средства (ЛС) прямого действия.
В связи с этим
первоочередное значение в этиотропном лечении ОРВИ имеют
противовирусные лекарственные средства (ЛС) прямого действия. К первому поколению таких ЛС относятся средства адамантанового ряда – амантадин и ремантадин. Данные ЛС являются блокаторами ионных каналов, образуемых трансмембранной областью вирусного белка М2 для переноса протонов, способствующих созданию внутри вириона низких значений рН, необходимых для освобождения рибонуклеопротеинов вируса от белка М1 и начала транскрипции вирусного генома. Установлено, что молекулы амантадина и ремантадина, соответствующие по размерам диаметру этих ионных каналов, ингибируют перенос протонов, повышая тем самым рН внутри эндосом, что затрудняет вышеописанный процесс, и таким образом подавляют репродукцию вируса. М2-каналы имеются только у вируса гриппа А, поэтому ингибиторы М2-каналов неэффективны при гриппе В [23]. Кроме того, в ряде исследований было показано, что к ингибиторам М2-каналов быстро развивается резистентность вируса гриппа А.
 В США в сезон
2005-2006 гг. было выделено 92,3% штаммов вируса гриппа Н3N2 и 25%
штаммов вируса гриппа Н1N1, устойчивых к ингибиторам М2-каналов [13]. В
связи с этим эксперты Центра по контролю и профилактике болезней (CDC)
не рекомендовали применение этой группы ЛС для лечения гриппа в 2006 г.
[14].
В США в сезон
2005-2006 гг. было выделено 92,3% штаммов вируса гриппа Н3N2 и 25%
штаммов вируса гриппа Н1N1, устойчивых к ингибиторам М2-каналов [13]. В
связи с этим эксперты Центра по контролю и профилактике болезней (CDC)
не рекомендовали применение этой группы ЛС для лечения гриппа в 2006 г.
[14].К ЛС второго поколения относятся ингибиторы нейраминидазы: 1) в виде ингаляций или аэрозольного спрея (занамивир) и 2) в виде капсул или суспензии для перорального применения (озельтамивир). Эти ЛС ингибируют вирусный фермент нейраминидазу, затрудняя высвобождение новых вирусных частиц из клеток и дальнейшее распространение вируса в организме. Их назначение в первые 48 ч заболевания уменьшает выраженность и продолжительность симптомов гриппа, снижает риск развития осложнений [18, 21]. В двойных слепых рандомизированных исследованиях показано, что у детей в возрасте от 1 до 12 лет, больных гриппом А и В, применение озельтамивира по сравнению с плацебо снижает медиану длительности болезни на 36 ч.
 Частота среднего отита в группе
озельтамивира была достоверно ниже [25].
Частота среднего отита в группе
озельтамивира была достоверно ниже [25].В России широкое распространение получило ЛС арбидол, рекомендованное для лечения гриппа А и В, а также таких ОРВИ, как аденовирусная инфекция, парагрипп, респираторно-синцитиальная инфекция. Высокая терапевтическая эффективность этого представителя класса индолов является результатом его широкой биологической активности и обусловлена иммуномодулирующим, интерферониндуцирующим, антиоксидантным и вирусоспецифическим действием.
Важнейшей характеристикой арбидола является отсутствие штаммовой специфичности. Арбидол, взаимодействуя с гемагглютинином вируса, ингибирует процесс слияния липидной оболочки вируса с мембраной клетки, подавляет вирусную репродукцию на ранней стадии. В отличие от амантадина и ремантадина, которые практически не влияют на репродукцию вируса гриппа В, арбидол подавляет ее на 60%.
Ранее уже упоминалось, что одним из недостатков ЛС адамантанового ряда является быстрое развитие резистентности к ним.
 Изучение влияния
арбидола на репродукцию различных штаммов вируса гриппа показало, что
он, в отличие от ремантадина, подавляющего репродукцию только
ремантадинчувствительных штаммов, подавляет репродукцию как
ремантадинчувствительных, так и ремантадинрезистентных штаммов вируса
гриппа [3]. В открытом сравнительном исследовании, в котором
участвовали 500 детей, было продемонстрировано, что включение арбидола
в комплекс терапии при ОРВИ (в т.ч. гриппе) достоверно укорачивает
длительность заболевания на 3,1 дня и снижает частоту осложнений на 11%
[11].
Изучение влияния
арбидола на репродукцию различных штаммов вируса гриппа показало, что
он, в отличие от ремантадина, подавляющего репродукцию только
ремантадинчувствительных штаммов, подавляет репродукцию как
ремантадинчувствительных, так и ремантадинрезистентных штаммов вируса
гриппа [3]. В открытом сравнительном исследовании, в котором
участвовали 500 детей, было продемонстрировано, что включение арбидола
в комплекс терапии при ОРВИ (в т.ч. гриппе) достоверно укорачивает
длительность заболевания на 3,1 дня и снижает частоту осложнений на 11%
[11].Для лечения ОРВИ широкое применение в нашей стране получили ЛС класса интерферонов (ИФН), которые обладают универсальным неспецифическим противовирусным действием. Под действием ИФН наблюдается индукция антигенов на поверхности клеток, что приводит к изменениям в топографии клеточной мембраны. Это препятствует фиксации вируса и его пенетрации внутрь клетки. Установлена ингибирующая активность ИФН по отношению к репликации вирусов.
 Увеличение продукции ИФН является наиболее быстрой
реакцией организма в ответ на заражение инфекционным агентом. Система
ИФН формирует защитный барьер на пути вирусов намного раньше
специфических защитных реакций иммунитета, путем стимуляции
резистентности клеток, делая их непригодными для размножения вирусов
[4].
Увеличение продукции ИФН является наиболее быстрой
реакцией организма в ответ на заражение инфекционным агентом. Система
ИФН формирует защитный барьер на пути вирусов намного раньше
специфических защитных реакций иммунитета, путем стимуляции
резистентности клеток, делая их непригодными для размножения вирусов
[4]. В рандомизированном исследовании в течение 4 дней назначали ИФН или плацебо здоровым добровольцам, зараженным риновирусом. Применение ИФН позволило предотвратить развитие заболевания в 90% случаев, плацебо при этом не оказывало никакого эффекта [16].
Четырехнедельное применение ИФН в период эпидемии позволило снизить заболеваемость ОРВИ более чем на 75% по сравнению с группой плацебо [19].
В литературе имеются неоднозначные данные относительно оценки клинической эффективности препаратов ИФН при ОРВИ у детей. В ряде работ отмечается, что комплексная терапия ОРВИ у детей с использованием ИФН имеет клиническую эффективность, проявляющуюся в уменьшении продолжительности интоксикационного и катарального синдромов [9].
 Вместе с тем G.A. Tannock et al. (1988), проведя исследование у 412
детей, больных ОРВИ, указывают на отсутствие клинического эффекта от
применения препаратов ИФН [24]. В данном вопросе, вероятно, существуют
методологические пробелы, которые препятствуют корректному
сопоставлению тех или иных результатов.
Вместе с тем G.A. Tannock et al. (1988), проведя исследование у 412
детей, больных ОРВИ, указывают на отсутствие клинического эффекта от
применения препаратов ИФН [24]. В данном вопросе, вероятно, существуют
методологические пробелы, которые препятствуют корректному
сопоставлению тех или иных результатов.| У детей при ОРВИ чаще применяют препараты экзогенных рекомбинантных ИФН для интраназального введения. Они имеют специфическую активность и не загрязнены посторонними примесями и некоторыми вирусами (гепатитов, иммунодефицита человека, цитомегаловирусами) [7]. |
Наряду с назначением противовирусных ЛС большое значение в терапии ОРВИ имеет их патогенетическое и симптоматическое лечение. В первую очередь это лечение направлено на ликвидацию таких синдромов и симптомов заболевания, как интоксикация, лихорадка, заложенность носа, кашель, головная боль, боль в горле.
 Проведение данной терапии улучшает
качество жизни больного, повышает его трудоспособность.
Проведение данной терапии улучшает
качество жизни больного, повышает его трудоспособность.Первостепенное значение при ОРВИ имеет борьба с гипертермией. При большинстве инфекционных заболеваний лихорадка является защитной реакцией организма на внедрение возбудителя. При этом повышение температуры тела способствует активации обменных процессов в организме больного, усилению иммунного ответа в виде активации выработки специфических антител и синтеза эндогенного ИФН, стимуляции фагоцитарной активности нейтрофилов, повышению антитоксической функции печени, увеличению почечного кровотока, угнетению репликации вирусов и размножения бактерий. Однако повышение температуры тела ребенка в подмышечной области выше 38,5-39 °С может приводить к изменению функций различных органов и систем. На фоне гипертермии повышается тонус симпатической нервной системы, вследствие чего развивается тахикардия и усиливается возбудимость дыхательного центра. На этом фоне возрастает потребление кислорода, интенсифицируется основной обмен.
 Изменение обмена веществ способствует задержке натрия и хлоридов в
организме ребенка. Чрезмерная активация симпатического отдела нервной
системы может привести к сужению сосудов не только кожи, но и
внутренних органов. При этом возникают спазмы прекапиллярных
сфинктеров, нарушается кровоток, происходит централизация
кровообращения, что в конечном итоге способствует гипоксии органов и
тканей. Гипоксия миокарда влечет за собой ослабление его сократительной
способности, гипоксия мозга приводит к его отеку, нарушению сознания и
судорогам. Чем меньше возраст ребенка, тем выше вероятность
отрицательного воздействия высокой температуры на его организм.
Особенно опасна гипертермия у детей первых 5 лет жизни. В этом возрасте
дети имеют небольшую поверхность тела, незначительные запасы жировой
ткани, недостаточную регуляторную функцию центра терморегуляции в
гипоталамусе. Все это не дает возможности организму ребенка
контролировать колебания температуры тела, адаптировать функциональное
состояние органов в ответ на ее повышение.
Изменение обмена веществ способствует задержке натрия и хлоридов в
организме ребенка. Чрезмерная активация симпатического отдела нервной
системы может привести к сужению сосудов не только кожи, но и
внутренних органов. При этом возникают спазмы прекапиллярных
сфинктеров, нарушается кровоток, происходит централизация
кровообращения, что в конечном итоге способствует гипоксии органов и
тканей. Гипоксия миокарда влечет за собой ослабление его сократительной
способности, гипоксия мозга приводит к его отеку, нарушению сознания и
судорогам. Чем меньше возраст ребенка, тем выше вероятность
отрицательного воздействия высокой температуры на его организм.
Особенно опасна гипертермия у детей первых 5 лет жизни. В этом возрасте
дети имеют небольшую поверхность тела, незначительные запасы жировой
ткани, недостаточную регуляторную функцию центра терморегуляции в
гипоталамусе. Все это не дает возможности организму ребенка
контролировать колебания температуры тела, адаптировать функциональное
состояние органов в ответ на ее повышение. Опасна гипертермия у детей с
хроническими заболеваниями сердечно-сосудистой, дыхательной и нервной
систем, фебрильными судорогами в анамнезе, заболеваниями,
сопровождающимися нарушениями метаболизма. Такие пациенты могут давать
отрицательные реакции даже на повышение температуры на 1 °С по
сравнению с нормой [1]. Сказанное заставляет врача прибегать к мерам по
снижению высокой температуры тела у ребенка.
Опасна гипертермия у детей с
хроническими заболеваниями сердечно-сосудистой, дыхательной и нервной
систем, фебрильными судорогами в анамнезе, заболеваниями,
сопровождающимися нарушениями метаболизма. Такие пациенты могут давать
отрицательные реакции даже на повышение температуры на 1 °С по
сравнению с нормой [1]. Сказанное заставляет врача прибегать к мерам по
снижению высокой температуры тела у ребенка. Назначение дополнительного количества жидкости необходимо любому лихорадящему ребенку для профилактики обезвоживания, легко наступающего у детей в связи с учащением дыхания и усилением потоотделения и приводящего к сгущению крови. У детей 1-го года жизни рекомендуется использовать отвары фруктов и овощей без добавления сахара, слабоминерализованную воду без газов, слабо заваренный чай (особенно зеленый) без сахара, слегка подсоленную кипяченую воду. Детям старше 1 года дополнительную жидкость дают в виде ягодных и фруктовых морсов, отваров, соков, слабо заваренных чаев.
Диетические ограничения определяются характером заболевания, преморбидным фоном.
 Важно, чтобы ребенок не голодал, и даже при
сниженном аппетите целесообразно давать легкоусвояемые углеводы. При
повышении температуры тела следует избегать острых блюд,
трудноусвояемой пищи, белковой нагрузки, консервированных продуктов,
кофе, крепко заваренного чая, мясных и рыбных бульонов. Пища должна
быть химически, механически и термически щадящей.
Важно, чтобы ребенок не голодал, и даже при
сниженном аппетите целесообразно давать легкоусвояемые углеводы. При
повышении температуры тела следует избегать острых блюд,
трудноусвояемой пищи, белковой нагрузки, консервированных продуктов,
кофе, крепко заваренного чая, мясных и рыбных бульонов. Пища должна
быть химически, механически и термически щадящей. Физические методы охлаждения увеличивают отдачу тепла с поверхности тела и обычно применяются при температуре тела выше 39,5 °С (у детей первых месяцев жизни – выше 39 °С). Ребенка раскрывают, освобождают от тесной одежды. Эффективным средством снижения температуры тела является обтирание губкой, смоченной водой температуры 30-32 °С, в течение 5 мин каждые полчаса (4-5 раз подряд). Следует отметить, что обтирание водой комнатной температуры (20-25 °С) оказывает меньший жаропонижающий эффект. Также было показано, что добавление в воду для обтирания алкоголя или уксуса не увеличивает эффект этой жаропонижающей процедуры.
При гиперпирексии (температура тела 40,5 °С и выше) показаны охлаждающие ванны: ребенка погружают в ванну с водой температуры на 1 °С ниже, чем температура тела у ребенка, далее воду постепенно охлаждают до 37 °С.
 Вся процедура должна продолжаться не более
10 мин. Эффект охлаждающих ванн возрастает при добавлении в воду
настойки валерианы (1 столовая ложка на ванну).
Вся процедура должна продолжаться не более
10 мин. Эффект охлаждающих ванн возрастает при добавлении в воду
настойки валерианы (1 столовая ложка на ванну). Показаниями к назначению жаропонижающих ЛС являются: лихорадка с температурой тела в аксиллярной области выше 38,5 °С; возраст до 5 лет (возраст повышенного риска возникновения фебрильных судорог), в частности первые 3 мес жизни; температура тела выше 38-38,5 °С у детей групп риска; плохая переносимость повышенной температуры тела (снижение коммуникабельности, избыточное возбуждение либо угнетение и т.п.) [2].
| Всемирной организацией здравоохранения в качестве средств выбора при лихорадочных состояниях у детей рекомендованы парацетамол (10-15 мг/кг массы тела, при максимальной суточной дозе 60 мг/кг массы тела) и ибупрофен (5-10 мг/кг массы тела, при максимальной суточной дозе 25-30 мг/кг массы тела) [26]. |
При ОРВИ в носу образуется слизь, которая нейтрализует различные вирусы и бактерии.
 Для того чтобы слизь наиболее полноценно выполняла свои
функции, необходимо стараться, чтобы она не высыхала. Для этого
применяют закапывание в нос раствора натрия хлорида (0,65%). На
фармацевтическом рынке Украины имеются готовые лекарственные формы
0,65% раствора натрия хлорида.
Для того чтобы слизь наиболее полноценно выполняла свои
функции, необходимо стараться, чтобы она не высыхала. Для этого
применяют закапывание в нос раствора натрия хлорида (0,65%). На
фармацевтическом рынке Украины имеются готовые лекарственные формы
0,65% раствора натрия хлорида. Помещение, в котором находится ребенок, увлажняют. При выраженной заложенности носа допускается применение специальных сосудосужающих детских капель для носа. Однако следует помнить, что их можно использовать не более 2-3 дней, так как при длительном применении могут возникнуть осложнения со стороны сердца, развиться синдром рикошета [20].
Подавляющие кашель ЛС можно давать детям только в случае сухого кашля, связанного с раздражением слизистых оболочек верхних дыхательных путей и мешающего ребенку спать и есть. Использование ненаркотических ЛС центрального действия не рекомендуется у детей в возрасте до 2 лет, так как кашель и обструктивный синдром у них обусловлены гиперплазией и отеком слизистой оболочки бронхов, нарушением моторики бронхиол, уменьшением подвижности секрета из-за повышенной его вязкости и низкого содержания сурфактанта.
 При этом назначение противокашлевых ЛС
центрального действия замедляет освобождение дыхательных путей от
секрета, ухудшает аэродинамику респираторного тракта и оксигенацию
легких. При остром кашле, сопровождающем ОРВИ, оптимальными являются
ЛС, увлажняющие и обволакивающие слизистые оболочки.
При этом назначение противокашлевых ЛС
центрального действия замедляет освобождение дыхательных путей от
секрета, ухудшает аэродинамику респираторного тракта и оксигенацию
легких. При остром кашле, сопровождающем ОРВИ, оптимальными являются
ЛС, увлажняющие и обволакивающие слизистые оболочки. При вовлечении в процесс нижних дыхательных путей (трахеобронхит, бронхит, пневмония) наряду с увлажнением слизистых оболочек показано применение муколитических и отхаркивающих ЛС. Они разжижают мокроту и облегчают ее отхождение [6]. Кроме ЛС (которые в раннем детском возрасте нужно применять как можно реже), для этой цели рекомендуются обильное теплое питье и увлажнение воздуха в помещении.
Сегодня ведется дискуссия о необходимости включения антигистаминных ЛС в комплекс терапии ОРВИ. Проведенный в 2003 г. метаанализ по изучению клинической эффективности антигистаминных ЛС для лечения ОРВИ, включавший данные 22 рандомизированных клинических исследований, в которых антигистаминные ЛС выступали в качестве монотерапии, и 13 испытаний, в которых антигистаминные ЛС комбинировали с деконгестантами (общее количество участников – 8930 человек, включая детей разного возраста и взрослых), показал, что использование антигистаминных ЛС в комплексной терапии ОРВИ имеет клиническую эффективность, проявляющуюся улучшением носового дыхания, уменьшением ринореи и чихания.
 Однако у детей младшего возраста клиническая
эффективность антигистаминных ЛС не доказана. Также не подтверждена
клиническая эффективность при монотерапии антигистаминными ЛС ОРВИ у
детей различного возраста [23].
Однако у детей младшего возраста клиническая
эффективность антигистаминных ЛС не доказана. Также не подтверждена
клиническая эффективность при монотерапии антигистаминными ЛС ОРВИ у
детей различного возраста [23]. Выполненный в 2005 г. метаанализ результатов исследований по изучению клинической эффективности антигистаминных ЛС для лечения кашля при ОРВИ у детей выявил, что использование антигистаминных ЛС І поколения в комплексе с деконгестантами у детей старшего возраста имеет незначительную клиническую эффективность, выражающуюся в уменьшении продолжительности кашля, заложенности носа и ринореи. Антигистаминные ЛС ІІ и ІІІ поколения неэффективны при кашле [12].
Результаты исследований польских авторов, проведенных в 2006 г. у 9640 больных ОРВИ, включая детей и взрослых, показали, что назначение цетиризина в комплексной терапии имело клиническую эффективность, проявляющуюся в уменьшении выраженности и продолжительности клинических симптомов ларингита, синусита, бронхита, тонзиллита, ринита.
 Особенно
высокой она была у больных с отягощенным аллергологическим анамнезом
[17].
Особенно
высокой она была у больных с отягощенным аллергологическим анамнезом
[17]. Выполненный в 2008 г. метаанализ данных по изучению эффективности антигистаминных ЛС для лечения длительного кашля у 793 детей продемонстрировал их клиническую эффективность, проявляющуюся в уменьшении продолжительности кашля [15].
В настоящее время широкое применение получили комбинированные противопростудные препараты, в состав которых входят жаропонижающие (чаще парацетамол), противокашлевые (преимущественно декстрометорфан), отхаркивающие (главным образом гвайфенезин) и антигистаминные (чаще хлорфенирамина малеат, цетиризин) ЛС.
Одной из актуальных проблем сегодня является применение антибиотиков при лечении острых респираторных инфекций. По данным фармакоэпидемиологических исследований, проведенных в России, из 800 опрошенных участковых врачей 76,5% используют или готовы использовать антибиотики начиная с первых дней заболевания, якобы с целью предупреждения бактериальных осложнений ОРВИ.
 Подобная практика в
большинстве случаев является не только неэффективной, но и вредной. Она
приводит к повышению микробной резистентности, угнетению
иммунологической реактивности, развитию дисбиоза. Кроме того,
назначение антибиотиков с высоким риском побочного действия
(ампициллина, гентамицина, ко-тримоксазола) может способствовать
поражению желудочно-кишечного тракта, сенсибилизации организма,
развитию специфических для антибиотиков побочных эффектов (ото-, нефро-
и гематотоксичности) [5]. Показаниями к антибактериальной терапии ОРВИ
у детей являются [8]:
Подобная практика в
большинстве случаев является не только неэффективной, но и вредной. Она
приводит к повышению микробной резистентности, угнетению
иммунологической реактивности, развитию дисбиоза. Кроме того,
назначение антибиотиков с высоким риском побочного действия
(ампициллина, гентамицина, ко-тримоксазола) может способствовать
поражению желудочно-кишечного тракта, сенсибилизации организма,
развитию специфических для антибиотиков побочных эффектов (ото-, нефро-
и гематотоксичности) [5]. Показаниями к антибактериальной терапии ОРВИ
у детей являются [8]:• сохранение температуры тела выше 38 °С более 3 дней;
• наличие одышки без обструкции и асимметрии хрипов;
• лейкоцитоз выше 15х109/л;
• острый средний отит;
• тонзиллит стрептококковой этиологии;
• синусит с болевым синдромом, отеком лица;
• бронхит, вызванный хламидиями и микоплазмой;
• пневмония.
Литература
1. Бережной В.В., Ершова И.Б., Кунегина Е. Н. Острые респираторные
вирусные заболевания у детей и подростков. – Луганск: Феникс,
2003. – 150 с.
Н. Острые респираторные
вирусные заболевания у детей и подростков. – Луганск: Феникс,
2003. – 150 с.
2. Ветров В.П., Длин В.В., Османов В.В. и др. Рациональное
использование антипиретиков в детском возрасте (Пособие для врачей).
– М., 2006. – 26 с.
3. Глушков Р.Г., Фадеева Н.И., Ленева И.А. и др.
Молекулярно-биологические особенности действия арбидола –
нового противовирусного препарата // Хим.-фарм. журнал. –
1992. – № 2. – С. 8-15.
4. Ершов Ф.И., Киселев О.И. Интерфероны и их индукторы (от молекул до
лекарств). – М.: ГЭОТАР, 2005. – С. 212, 221-227,
275-277.
5. Карпов О.И. Фармакоэпидемиология острого синусита // Новые
Санкт-Петербургские врачебные ведомости. – 2000. –
№ 1. – С. 58-62.
6. Майданник В.Г. Кашель у детей: причины, механизмы, диагностика и
лечение // Современная педиатрия. – 2005. – № 3.
– С. 23-27.
7. Попов В.Ф. Лекарственные формы интерферонов. – М.:
Триада-Х, 2002. – 136 с.
– М.:
Триада-Х, 2002. – 136 с.
8. Таточенко В.К. Антибиотики при бактериальных заболеваниях
дыхательных путей // Респираторные заболевания в педиатрической
практике. – 2001. – № 1. – С. 1-3.
9. Феликсова Л., Шебекова В., Целипанова Е. и др. Гриппферон у детей,
больных ОРВИ // Врач. – 2001. – № 1. – С.
40-41.
10. Шаханина И.Л. Грипп и острые респираторные заболевания –
приоритетная социально-экономическая проблема здравоохранения.
Вакцинопрофилактика гриппа. – М.: Медицина, 1998. –
С. 10-16.
11. Учайкин В.Ф., Шустер А.М., Кладова О.В., Медников Б.Л. Арбидол в
профилактике и лечении гриппа и других острых респираторных вирусных
инфекций у детей // Педиатрия. – 2002. – № 6.
– С. 1-9.
12. Arroll B. Non-antibiotic treatments for upper-respiratory tract
infections. Respir Med 2005; 99: 1477-1484.
13. Bright R.A., Shay D.K., Shu B. et al. Adamantane resistense among
influenza A viruses isolated early during the 2005-2006 in the United
States. JAMA 2006; 295: 891-894.
JAMA 2006; 295: 891-894.
14. Centers for Disease Control and Prevention. CDC health alert. CDC
recommends against the use of amantadine and rimantadine for the
treatment or prophylaxis of influenza in the United States during the
2005-2006 influenza season // www.cdc.gov/flu/han011406.htm.
15. Chang A.B., Peake J., McElrea M.S. Anti-histamines for prolonged
non-specific cough in children. – The Cochrane Library, 2008.
16. Higgins P.G., Al-Nakib W., Wilman J., Tyrrell D.A. Interferon-beta
ser as prophylaxis against experimental rhinovirus infection in
volunteers. J Interferon Res 1986; 6: 153-159.
17. Jahnz-Rozyk K. Ceterizine and respiratory tract infections in
opinion of Polish doctors. Pol Merkur Lekarski 2006; 21: 454-458.
18. Kaiser L., Keene O.N., Hammond J. Impact of zanamivir on
antibiotics use for respiratory events following acute influenza in
adolescents and adults. Arch Int Med 2000; 160: 3234-3240.
Arch Int Med 2000; 160: 3234-3240.
19. Monto A.S., Shope T.C., Schwartz S.A., Albrecht J.K. Intranasal
interferon-alpha-2-beta for seasonal prophylaxis of respiratory
infection. J Infect Dis 1986; 154: 128-133.
20. Mossad S. Treatment of the common cold. Br Med J 1998; 317: 33-36.
21. Nicholson K.G., Aoki F.Y., Osterhaus A.D. et al. Efficacy and
safety of oseltamivir in treatment of influenza: randomized controlled
trial. Lancet 2000; 335: 1845-1858.
22. Stephenson I., Nicholson K.G. Influenza: vaccination and treatment.
Eur Respir J 2001; 17: 1282-1293.
23. Sutter A.I., Lemiengre M., Campbel H., Mackinnon H.F.
Antihistamines for the common cold. Cohrane Detabase Syst Rev 2003; 3:
CD001267.
24. Tannock G.A., Gillett S.M., Gillett R.S. et al. A study of
intranasally administered interferon A (rIFN-alpha-2A) for the seasonal
prophylaxis of natural viral infections of the upper respiratory tract
in healthy volunteers. Epidemiol Infect 1988; 101: 611-621.
Epidemiol Infect 1988; 101: 611-621.
25. Whitley R.J., Hayden F.G., Reisinger K.S. et al. Oral oseltamivir
treatment in children. Ped Inf Dis 2001; 2: 127-133.
26. World Health Organisation. The management of fever in young
children with acute respiratory infections in developing countries.
Programme for the control of acute respiratory infections,
WHO, Geneva. WHO/ARI/ 93.30.
7 распространенных респираторных заболеваний у детей
Из U.S. News & World Report
Автор: Элейн К. Хоули
Респираторные заболевания очень распространены.
Дыхательные пути человека открыты для внешнего мира, чтобы впускать воздух и выходить углекислый газ, что делает его легкой точкой входа для микробов, которые потенциально могут вызвать болезнь. Заболевания, поражающие дыхательную систему — нос, горло и легкие, — очень распространены, особенно у детей, у которых еще не сформировался иммунитет к распространенным вирусам и бактериям, которые могут вызывать такие проблемы.
Эти семь распространенных детских респираторных заболеваний могут в какой-то момент повлиять на вашего ребенка. Знайте признаки и симптомы и обратитесь за помощью к педиатру, если симптомы сохраняются или ухудшаются со временем.
Грипп
Также называемый гриппом, «грипп — это вирус, который обычно вызывает от пяти до семи дней высокой температуры, мышечных болей, усталости, кашля и насморка», — говорит Доктор Кэтрин Уильямсон , педиатр из CHOC Children’s at Mission Hospital. в округе Ориндж, штат Калифорния, и представитель Американской академии педиатрии.«Осложнениями от гриппа являются пневмония и госпитализация из-за вторичных бактериальных инфекций».
Грипп может быть опасным, даже смертельным, особенно для маленьких детей. У детей температура обычно выше, чем у взрослых, и их пищеварительные симптомы обычно тоже хуже.
Но существуют вакцины, которые могут значительно снизить риск заражения болезнью или уменьшить ее симптомы, если ваш ребенок действительно заболел гриппом.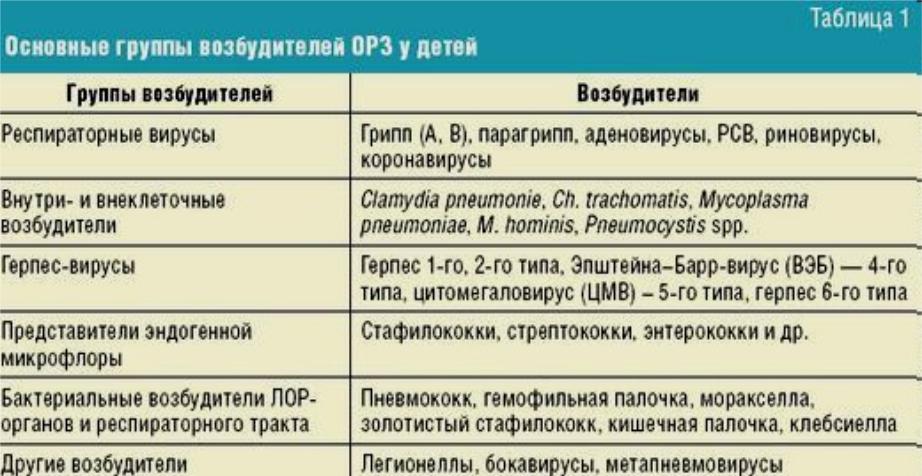 Ваш ребенок может быть вакцинирован с 6-месячного возраста. Вакцины необходимо вводить ежегодно, поскольку состав препарата меняется каждый год в ожидании штамма (ов), который, как ожидается, будет преобладать в следующем сезоне.Для того чтобы вакцина стала эффективной после введения, требуется около двух недель.
Ваш ребенок может быть вакцинирован с 6-месячного возраста. Вакцины необходимо вводить ежегодно, поскольку состав препарата меняется каждый год в ожидании штамма (ов), который, как ожидается, будет преобладать в следующем сезоне.Для того чтобы вакцина стала эффективной после введения, требуется около двух недель.
Не существует лекарств, которые полностью излечили бы случай гриппа, но «существует противовирусное лекарство под названием Осельтамивир (Тамифлю), которое может сократить продолжительность болезни, если начать в первые 48 часов после начала лихорадки», Уильямсон говорит. Вы также можете «помочь своему организму бороться с инфекцией» с помощью соответствующего отдыха и жидкости. Ацетаминофен и ибупрофен могут помочь при мышечных болях, лихорадке и общем дискомфорте.”
Простуда
Также вызванная вирусами простуда, также известная как инфекция верхних дыхательных путей, является основной причиной, по которой дети остаются дома больными и не ходят в школу, сообщает Центры по контролю и профилактике заболеваний. Детская больница Филадельфии сообщает, что большинство детей болеют от шести до восьми простуд в год.
Детская больница Филадельфии сообщает, что большинство детей болеют от шести до восьми простуд в год.
Обычно симптомы включают:
- Насморк.
- Боль в горле.
- Кашель.
- Чихание.
- Головная боль и ломота в теле.
Простуда вызывается вирусами, которые «обычно менее серьезны, чем грипп, и имеют меньший риск возникновения вторичной пневмонии», — сообщает Williamson . Симптомы очень похожи у взрослых и детей, но у детей также может быть небольшая температура, тогда как у взрослых обычно нет.
Миллионы людей в США простужаются каждый год, и в большинстве случаев они не проявляют серьезности и выздоравливают самостоятельно за несколько дней. Отдых и питье большого количества жидкости помогут вашему ребенку быстрее почувствовать себя лучше.Но не давайте лекарства от простуды, отпускаемые без рецепта, особенно если вашему ребенку меньше 2 лет. В 2008 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов предоставило обновленное руководство, в котором отмечалось, что безрецептурные препараты от кашля и простуды не следует использовать у младенцев и детей в возрасте до 2 лет из-за потенциально опасных побочных эффектов, включая судороги, учащенное сердцебиение, потерю сознания. и даже смерть.
и даже смерть.
Астма
CDC сообщает, что более 6,2 миллиона детей в Соединенных Штатах, или около 8% всех американских детей, страдают астмой.Астма — потенциально очень серьезное заболевание легких, вызывающее:
- Кашель.
- Плотность или давление в груди.
- Одышка или затрудненное дыхание.
- Хрипы или свистки при выдохе.
Симптомы у взрослых, как правило, такие же, как у детей. Однако у взрослых симптомы могут быть более стойкими. Дети также чаще страдают аллергией в дополнение к астме, чем взрослые.
Приступы астмы могут быть вызваны рядом факторов, например, вдыханием пыли или пыльцы или воздействием аллергена, например, перхоти домашних животных.Астма повышает риск развития бронхита или пневмонии у детей. По данным Американской ассоциации легких, это также третья по значимости причина госпитализаций среди детей в возрасте до 15 лет.
Если кажется, что ваш ребенок сильно кашляет, кашляет во время физических упражнений или у него одышка, обратитесь к педиатру. Свистящее или свистящее дыхание или повторяющиеся эпизоды бронхита также должны отправить вас к врачу для обследования.
Свистящее или свистящее дыхание или повторяющиеся эпизоды бронхита также должны отправить вас к врачу для обследования.
Синусит
Синусит, также называемый инфекцией носовых пазух, представляет собой воспаление или отек ткани, выстилающей пазухи.В этих обычно заполненных воздухом мешочках за носом и глазами может скапливаться жидкость, что может привести к инфекции. Он часто сопровождает простуду или грипп или может быть вызван аллергией.
Синусит может привести к:
- Боль и давление в лице, особенно за глазами и носом.
- Чувство заложенности или перегруженности.
- Кашель и насморк.
- Постназальные выделения, которые могут вызвать боль в горле, неприятный запах изо рта, тошноту или рвоту.
У детей симптомы могут сохраняться дольше, чем у взрослых.Использование нети-пота для промывания носовых пазух или прием противоотечных средств, отпускаемых без рецепта, может помочь уменьшить воспаление и уменьшить симптомы. Если присутствует бактериальная инфекция, ваш педиатр может назначить антибиотик. Детям с хроническим синуситом может быть рекомендовано хирургическое вмешательство для очистки перегруженных участков.
Если присутствует бактериальная инфекция, ваш педиатр может назначить антибиотик. Детям с хроническим синуситом может быть рекомендовано хирургическое вмешательство для очистки перегруженных участков.
Бронхит
Бронхит — это воспаление бронхов или больших дыхательных трубок в легких. Обычно это вызвано вирусом и может развиться после простуды или гриппа.Постоянный кашель — классический симптом, который может сохраняться в течение трех-четырех недель после того, как вирус выйдет из системы. Помимо грудного кашля, симптомы могут включать:
- Насморк.
- Боль и заложенность в груди.
- Лихорадка и озноб.
- Общее ощущение недомогания или усталости.
- Свистящее дыхание.
- Боль в горле.
Симптомы у взрослых и детей с бронхитом в основном одинаковы, но дети с бронхитом с большей вероятностью проглотят слизь, чем откашливают ее.Дети, страдающие астмой или аллергией, или те, кто страдает хроническим синуситом, подвержены более высокому риску развития бронхита. Иногда астму принимают за бронхит или наоборот, поэтому в случае сомнений проконсультируйтесь с педиатром. Лечение обычно направлено на ослабление симптомов.
Иногда астму принимают за бронхит или наоборот, поэтому в случае сомнений проконсультируйтесь с педиатром. Лечение обычно направлено на ослабление симптомов.
Круп
Круп, также называемый ларинготрахеобронхитом, обычно вызывается вирусом, вызывающим отек трахеи (дыхательного горла) и гортани (голосовой аппарат). Отек препятствует свободному проникновению воздуха в легкие и создает своего рода писк или пронзительный хрипящий звук при глубоком вдохе.Голос вашего ребенка тоже может звучать хрипло, чем обычно.
«Круп, как правило, поражает детей младше 4 лет и характеризуется резким лающим кашлем и респираторной недостаточностью», — говорит Williamson . Хотя это гораздо более распространено среди детей, у взрослых также может развиться круп.
Поскольку круп обычно вызывается вирусом, его обычно лечат отдыхом, жидкостями и безрецептурными противовоспалительными и болеутоляющими средствами, такими как ибупрофен или парацетамол. Вдыхание увлажненного воздуха также может помочь облегчить дыхание, особенно ночью.В тяжелых случаях вашему ребенку могут потребоваться стероиды, чтобы снять воспаление и облегчить дыхание.
Вдыхание увлажненного воздуха также может помочь облегчить дыхание, особенно ночью.В тяжелых случаях вашему ребенку могут потребоваться стероиды, чтобы снять воспаление и облегчить дыхание.
Стрептококковая ангина
Доктор Раджсри Намбудрипад, специалист по интегративной медицине из Медицинского центра Св. Джуда в Фуллертоне, Калифорния, говорит, что стрептококковая ангина довольно часто встречается у детей. «До 3 из 10 детей, страдающих ангиной, страдают стрептококковой ангиной», — отмечает она. Для сравнения, по ее словам, только у 1 из 10 взрослых, страдающих ангиной, будет стрептококковая инфекция.
Поскольку ангина вызвана бактериальной инфекцией, ее обычно лечат антибиотиками.«Наиболее часто используемый антибиотик — пенициллин или амоксициллин в течение 10 дней», — говорит Намбудрипад. Лекарство обычно дается в виде жидкой суспензии для питья, а не в виде таблетки для проглатывания, поскольку детям младшего возраста может быть трудно справиться с приемом таблетки. Доза будет скорректирована в соответствии с массой тела вашего ребенка.
Доза будет скорректирована в соответствии с массой тела вашего ребенка.
Strep следует относиться серьезно и лечить как можно скорее как у детей, так и у взрослых. При отсутствии лечения это может привести к серьезным осложнениям со здоровьем, включая ревматическую лихорадку, которая является серьезным воспалительным заболеванием, поражающим сердце, суставы, нервную систему и кожу.Это также может привести к ревматическому пороку сердца и заболеванию почек.
«У детей существует возможная связь между стрептококковой инфекцией группы А и неврологическим заболеванием, называемым детским аутоиммунным психоневрологическим расстройством, связанным со стрептококками группы А (PANDAS)», — говорит Намбудрипад. Это состояние вызывает неврологические симптомы, включая обсессивно-компульсивное расстройство, тики и другие проблемы с психическим здоровьем.
Пневмония
Пневмония вызывается инфекцией легких и может стать опасным заболеванием.Симптомы включают:
- Учащенное дыхание.

- Высокая температура и озноб.
- Кашель.
- Усталость.
- Боль в груди, особенно при дыхании.
Симптомы могут быть менее очевидными у детей, чем у взрослых, а это означает, что их сложнее диагностировать. Всемирная организация здравоохранения сообщает, что на пневмонию приходится 15% всех случаев смерти детей в возрасте до 5 лет.
Вирусы, бактерии или грибки могут быть виноваты, а пневмония может развиться после того, как ваш ребенок переболел простудой, гриппом или стрептококковой ангиой.Бактериальную пневмонию можно лечить антибиотиками. Не существует специального лекарства, которое могло бы вылечить вирусную пневмонию, но ваш врач может назначить противовирусный препарат, который сократит продолжительность болезни. Отдых и много жидкости также могут помочь вашему ребенку почувствовать себя немного лучше. Вакцины против пневмококка, кори и сильного кашля могут снизить риск развития пневмонии у вашего ребенка.
Относительно аспирина
Предупреждение: никогда не используйте аспирин или другие лекарства, содержащие аспирин, для лечения вирусных заболеваний, таких как грипп, простуда или ветряная оспа у детей. Использование аспирина для лечения вирусных инфекций связано с синдромом Рейе, потенциально смертельным заболеванием, которое вызывает повреждение мозга и печени у детей. Повышенная температура обычно является признаком вирусной инфекции, поэтому, если у вашего ребенка высокая температура, не давайте ему аспирин. В случае сомнений проконсультируйтесь со своим врачом.
Использование аспирина для лечения вирусных инфекций связано с синдромом Рейе, потенциально смертельным заболеванием, которое вызывает повреждение мозга и печени у детей. Повышенная температура обычно является признаком вирусной инфекции, поэтому, если у вашего ребенка высокая температура, не давайте ему аспирин. В случае сомнений проконсультируйтесь со своим врачом.
Сохранение здоровья
«Самый важный подход к респираторным заболеваниям — это их профилактика», — говорит Уильямсон . Следуйте этим простым советам, чтобы уменьшить передачу этих распространенных заболеваний:
- Прикрывайте рот своим кашлем или чиханием.Поскольку эти состояния обычно передаются через кашель и чихание, важно прикрывать кашель или чихание — желательно локтем или салфеткой, а не голой рукой.
- Часто мойте руки. «Респираторные заболевания передаются через слюну и выделения из носа либо при прямом контакте, таком как рукопожатие, прикосновение к общим поверхностям, таким как дверные ручки и столешницы, либо при кашле поблизости», — говорит Williamson .
 Обязательно умывайтесь не менее 20 секунд теплой водой с мылом, чтобы убить вирусы или бактерии, которые могут оставаться на вашей коже.
Обязательно умывайтесь не менее 20 секунд теплой водой с мылом, чтобы убить вирусы или бактерии, которые могут оставаться на вашей коже. - Не прикасайтесь к глазам, носу и рту. Эти области являются обычными точками входа в организм многих вирусов.
- Ограничить контакт с больными людьми. По возможности избегайте контактов с другими больными людьми. Это также означает, что больного ребенка не пускают в школу.
- Сделайте прививку от гриппа. «Самая эффективная профилактика гриппа — вакцина против гриппа, которая значительно снижает риск заражения пневмонией или госпитализации, если вы контактируете с больным гриппом», — говорит Williamson .
Пульмонология (лечение заболеваний легких и органов дыхания у детей) | Детская больница CS Mott
Отделение детской пульмонологии детской больницы C.S. Mott обеспечивает комплексную клиническую помощь и консультации младенцам, детям и молодым людям с острыми и хроническими проблемами дыхания.
Наша команда детских пульмонологов предлагает экспертные знания в области диагностики и лечения распространенных нарушений дыхания, а также редких заболеваний легких.
Помимо наших сертифицированных преподавателей, пациенты детской пульмонологии UM имеют доступ к нашей многопрофильной команде, в том числе медсестрам, диетологам, респираторным терапевтам, социальным работникам и специалистам по детской жизни, что позволяет нам предоставлять комплексные услуги, ориентированные на пациента и семью. каждому ребенку, о котором мы имеем честь заботиться.
Опыт в области лечения респираторных заболеваний у детейМы лечим весь спектр респираторных симптомов и заболеваний, в том числе:
Расширенные возможности диагностикиДиагностика — это первый шаг в создании эффективного плана лечения для вашего ребенка.Отделение программы детской пульмонологии U-M предлагает широкий спектр диагностических услуг, в том числе:
- Современная детская легочная лаборатория, оснащенная для выполнения:
- Проба с метахолином (для диагностики астмы)
- Тестирование оксида азота в выдыхаемом воздухе (для измерения воспаления дыхательных путей)
- Назальный анализ оксида азота (для диагностики первичной цилиарной дискинезии)
- Потовые пробы (для диагностики муковисцидоза)
- Нагрузочные испытания
- Исследование функции легких у младенцев (для раннего выявления муковисцидоза легких и других заболеваний)
- Гибкая бронхоскопия для выявления структурных поражений дыхательных путей
- Бронхоальвеолярный лаваж для выявления инфекции или аспирации
- Протоколы визуализации грудной клетки с высоким разрешением для снижения радиационного облучения
- Комбинированные процедуры для уменьшения воздействия анестезии
- Генетические исследования муковисцидоза и интерстициальных заболеваний легких
- Биопсия ресничек и легких проанализирована специализированной бригадой педиатров
- Тест на кожную аллергию на общие аллергены, вызывающие астму
Отделение детской пульмонологии руководит программами фундаментальных и клинических исследований, связанных с астмой, муковисцидозом и бронхолегочной дисплазией.Исследования факультета в настоящее время финансируются Национальными институтами здравоохранения и Фондом кистозного фиброза. Узнайте больше о наших текущих исследованиях.
Запишитесь на прием, позвонив нам по телефону 734-764-4123.
Заболевания легких у детей — Детские пульмонологи
Сертифицированные детские пульмонологи, доктор Питер Шохет и доктор Хау Ли, проводят оценку и лечение следующих детских легочных заболеваний и расстройств.
Острая и хроническая обструкция верхних дыхательных путей
Острый респираторный дистресс — ARDS
Респираторное заболевание, связанное с аллергией.
Апноэ недоношенных (АОП) / младенческое апноэ / мониторинг апноэ
Синдромы аспирации
Бронхоэктатическая болезнь
Бронхиолит
Бронхолегочная дисплазия / хроническая болезнь легких у недоношенных
Грудная боль
Хронический кашель
Хроническая болезнь легкихХроническая болезнь легких, связанная с нервно-мышечными расстройствами
Хроническая заложенность носа
Хроническая потребность в кислороде
Врожденные аномалии легких, дыхательных путей и грудной клетки
Врожденные аномалии легких (пороки развития легких)
Круп и рецидивирующий круп
Кистозный фиброз
Затрудненное дыхание
Оценка рецидивирующей пневмонии
Гибкая бронхоскопия
Аспирация инородного тела
Привычный кашель
Интерстициальное заболевание легких
Инвазивная и неинвазивная механическая вентиляция
Ларингомаляция / трахеобронкомаляция
Обструктивное апноэ сна (СОАС)
Воронкообразная деформация грудной клетки
Плевральные выпоты и эмпиема
Пневмония
Интерпретация полисомнографии (исследования сна)
Тестирование легочной функции
Пульсоксиметрия
Реактивное заболевание дыхательных путей (РАД)
Рецидивирующие и стойкие / респираторные инфекции
Ринит / аллергический или хронический
Одышка
Простое тестирование с помощью упражнений
Нарушения сна
Проблемы с дыханием, связанные со сном
Храп
Проблемы с дыханием, вызванные спортом и физическими упражнениями
Стридор (шумное дыхание)
Уход и лечение трахеостомии
Неинвазивная вентиляция с положительным давлением в дыхательных путях
Туберкулез
Обструкция верхних дыхательных путей
Дисфункция голосовых связок
Хрипы
Свяжитесь с нами
Наши офисы расположены в пресвитерианской больнице Texas Health Plano, здание медицинского офиса 1 (MOB 1).Если вашему ребенку нужен специалист по детской пульмонологии, свяжитесь с нами по телефону 972-981-3251 или отправьте онлайн-заявку на прием.
Заболевания легких у детей | Европейский фонд легких
Бронхиолит
Бронхиолит — это воспаление или отек мельчайших дыхательных путей, называемых бронхиолами. Он поражает детей в возрасте до 2 лет и является наиболее частой причиной госпитализации детей в возрасте до 1 года.
Бронхиолит вызывается вирусной инфекцией, чаще всего респираторно-синцитиальным вирусом (RSV).Это наиболее распространенная легочная инфекция в младенчестве. У большинства детей RSV-инфекция развивается к 2 годам, и по большей части симптомы похожи на простуду. Вирус вызывает избыток слизи и отек слизистой оболочки дыхательных путей.
У заболевших младенцев развивается учащенное дыхание, раздражительность при хрипах, плохое питание и рвота.
Младенцам, инфицированным респираторно-синцитиальным вирусом (РСВ), обычно требуется поддерживающая терапия, но не лекарства. В очень тяжелых случаях назначают противовирусные препараты.Младенцам с высоким риском развития этого состояния может быть назначено лечение антителом под названием паливизумаб, чтобы помочь уменьшить тяжелые инфекции.
Заболевания легких, связанные с недоношенностью, включая бронхолегочную дисплазию (БЛД)
Недоношенные дети подвергаются повышенному риску развития проблем с легкими. Легкие — один из последних органов, которые развиваются, когда ребенок растет. Это означает, что при преждевременном рождении ребенка его легкие еще не полностью развиты.
В исследовании, проведенном в США с участием 100 детей, родившихся на сроке 23 недели, 60 умерли до выписки из больницы, в основном от дыхательной недостаточности.
Наиболее частым заболеванием легких, поражающим недоношенных детей, является бронхолегочная дисплазия (БЛД).
БЛД — одно из наиболее серьезных осложнений преждевременных родов: у 23% детей, рожденных на 28 неделе, и у 73% детей, рожденных на 23 неделе, наблюдается это заболевание. Для него характерно учащенное и затрудненное дыхание с затрудненным дыханием и кашлем, а также трудности с поддержанием нормального уровня кислорода, что часто приводит к искусственной вентиляции легких.
БЛД обычно диагностируется, если младенец все еще нуждается в дополнительном кислороде и продолжает проявлять признаки респираторных заболеваний в возрасте старше 28 дней. Лечение направлено на поддержку дыхания до тех пор, пока развивающиеся легкие не станут адекватными, но ПРЛ часто приводит к проблемам с дыханием в более позднем детстве и во взрослом возрасте. Нет доступных методов лечения кондитина, и необходимы дополнительные исследования для разработки эффективного лечения детей, рожденных с незрелыми легкими.
Пневмония
Пневмония распространена во всем мире, но особенно в развивающихся странах.По оценкам, около 151 миллиона новых случаев пневмонии ежегодно возникает среди детей в возрасте до 5 лет в развивающихся странах. В развитых странах серьезные осложнения обычно возникают у детей с основными заболеваниями.
Пневмония чаще всего встречается у детей младшего возраста и часто начинается после простуды, кашля или боли в горле, и она может легко передаваться от человека к человеку по воздуху или через зараженную поверхность. Пневмония чаще всего вызывается бактерией Streptococcus pneumoniae или вирусом, например:
- Аденовирус
- Риновирус
- Вирус гриппа
- Респираторно-синцитиальный вирус (RSV)
У людей с пневмонией кашель появляется вместе с другими симптомами, такими как жар или одышка.Между странами существуют большие различия в количестве случаев пневмонии и числа смертей от этого заболевания. Это связано с рядом факторов, включая недоедание, перенаселенность, низкий вес при рождении, ранее существовавшую ВИЧ-инфекцию и эффективность программ иммунизации внутри стран. Смертность от пневмонии в странах Восточной Европы выше, чем в странах Западной Европы.
Пневмония также может развиться как осложнение кори, и встречается у 5–10% детей, заболевших корью.
Пневмония обычно диагностируется на рентгеновском снимке грудной клетки, который показывает затенение легких. Антибиотики обычно используются для лечения пневмонии. Антибиотики убивают бактерии, но не вирусы. Однако часто причина пневмонии неизвестна на ранней стадии болезни, и для устранения вероятных бактериальных причин назначают антибиотики; кроме того, инфекция бактериями может последовать за первоначальной вирусной инфекцией.
Туберкулез (ТБ)
ТБ вызывается бактерией Mycobacterium Tuberculosis. Туберкулез у детей чаще всего возникает в результате контакта с кем-то из членов семьи, кто болеет активной формой туберкулеза.
Младенцы и дети подвержены повышенному риску заражения туберкулезом, и у них может развиться активная форма болезни быстрее, чем у взрослых. Если не лечить, вероятность смерти младенцев от инфекции составляет 50-60%.
Симптомы туберкулеза различаются, но включают кашель, боль в груди, мокроту, усталость и потерю аппетита.
Диагноз ТБ может быть трудно подтвердить, поскольку трудно собрать образцы слизи, образующейся при кашле у детей. Врачи будут изучать симптомы ребенка, образцы тканей и свидетельства заражения туберкулезом, чтобы решить, есть ли у него заболевание.
Хотя дети очень уязвимы к туберкулезу, он не является одной из основных причин детской смертности. Вакцина с бациллами Кальметта-Герена (БЦЖ) используется в некоторых странах, особенно там, где туберкулез является относительно распространенным явлением, но во многих странах, где вероятность заболевания туберкулезом мала, ее общее использование постепенно прекращено.
Проблемы с легкими, присутствующие с рождения (врожденные проблемы с легкими)
Врожденные респираторные заболевания присутствуют с рождения и влияют на структуру и функцию легких.Они могут повлиять на диафрагму, легкие, кровоснабжение, дыхательные пути, гортань и ротовую полость.
Причины врожденных патологий обычно неизвестны. Иногда они могут быть вызваны наследственным заболеванием. Одним из примеров этого является первичная цилиарная дискинезия, когда ребенок наследует дефектный ген от своего родителя.
Последствия врожденных проблем с легкими обычно проявляются на 1-м году жизни. Симптомы первичной цилиарной дискинезии могут включать неспособность удалить слизь из легких, рецидивирующий бронхит, стойкую заложенность носа и синусит.
Диагностика и лечение врожденных проблем с легкими должны проводиться в специализированных центрах, поскольку эти состояния встречаются редко и часто трудно поддаются лечению.
Коклюш
Коклюш, также известный как коклюш, представляет собой кратковременную респираторную инфекцию, вызываемую бактерией Bordetella Pertussis. Симптомы характеризуются продолжительными периодами кашля, часто сопровождаемыми характерным «криком» при вдохе. Кашель может длиться неделями или месяцами.
Поскольку большинство детей в ЕС вакцинируются от коклюша, симптомы часто бывают легкими. Однако вспышки болезни все еще происходят, потому что вакцина не обеспечивает пожизненной защиты, и все чаще случаи коклюша наблюдаются у взрослых.
Детские респираторные заболевания: прошлое, настоящее и будущее
Детское респираторное заболевание изменилось за последние 20 лет; мы могли бы заполнить целый номер журнала, отдавая дань памяти нашим знаменитым предкам. Мы ставим перед нашими коллегами новые задачи в области респираторных заболеваний у взрослых.Они должны научиться справляться с состояниями, которые 20 лет назад были редкостью в клинике грудной клетки для взрослых, такими как муковисцидоз (МВ) и отдаленные последствия преждевременных родов и врожденных пороков развития дыхательных путей. Более того, исследования в детстве бросают вызов патофизиологическим концепциям на протяжении всей жизни.
Множество крупных проспективных когортных исследований при рождении пролили свет на различные модели свистящего дыхания, их факторы риска и их эволюцию в детстве. Кто бы мог подумать, что родиться в сарае хорошо! Становится все более очевидным, что даже для «взрослых» заболеваний, таких как хроническая обструктивная болезнь легких (ХОБЛ), дородовые и ранние события жизни не менее важны, чем курение во взрослом возрасте 1.МВ также стало заболеванием взрослых 2. Несмотря на то, что этому способствовало множество факторов, основной причиной было создание специализированных центров МВ, модель, все чаще применяемая взрослыми бригадами. Это может служить моделью для других болезней; как хорошо структурированный междисциплинарный подход к лечению может принести пользу пациентам. Возможно, в количественном отношении наиболее важным достижением является область общественного здравоохранения. Снижение инвазивных бактериальных инфекций благодаря программам вакцинации младенцев является одним из важнейших достижений прошлого.
Другие области изменений включают выживание недоношенных новорожденных, которые становятся все меньше и меньше. Эти дети достигают взрослой жизни с нарушенной функцией легких и аномальными результатами компьютерной томографии. Что будет с их стареющими легкими? Интерстициальное заболевание легких (ILD) становится все более понятным с появлением новых генетических объектов, таких как мутации сурфактантного протеина C, имеющих отношение к ILD 3 у взрослых. Появление новых мощных методов лечения, в частности антибиотиков и противовоспалительных средств, привело к появлению потребность в более совершенных инструментах для мониторинга, включая достаточно маленькие бронхоскопы, чтобы обследовать даже недоношенных детей, а также в новых физиологических тестах.Ниже рассматриваются конкретные будущие задачи; во-первых, области конкретных заболеваний; во-вторых, инструменты мониторинга; и, в-третьих, педиатрическая интенсивная терапия.
СПЕЦИАЛЬНЫЕ ЗАБОЛЕВАНИЯ
Новорожденный
В неонатальной практике был достигнут значительный прогресс, включая более эффективное применение традиционных методов лечения, таких как антенатальные кортикостероиды и экзогенные сурфактанты, а также признание их долгосрочных эффектов. Этот урок также привел к более крупным испытаниям, таким как использование оксида азота у недоношенных детей 4 и неинвазивная вентиляция в этой популяции 5.Были улучшены физиологические определения (например, хроническое заболевание легких у недоношенных (ХЗЛ) или бронхолегочная дисплазия (БЛД)), и текущие испытания во всем мире сосредоточены на оптимальной насыщенности кислородом для недоношенных детей (BOOST (Преимущества целевого определения насыщения кислородом) и BOOST 2). Для определения того, является ли недоношенность фактором риска развития ХОБЛ, важны более отдаленные респираторные исходы, и растет признание того, что дети с легкой неонатальной болезнью легких могут иметь значительные долгосрочные последствия 6.Распознавание антенатальной инфекции Ureaplasma spp. 7 как причина преждевременных родов снова появляется как потенциальный целевой вариант для снижения бремени ХЗЛ / ПРЛ.
Детская астма
Детская астма будет оставаться основным направлением специальности. Хотя распространенность, возможно, снизилась в некоторых частях развитого мира, она растет в других странах 8. Новые подходы к пониманию основных механизмов все больше зависят от характеристики фенотипа 9, и для определения фенотипов необходимы передовые биологические методы, как показано на примере U- BIOPRED (Объективные биомаркеры для прогнозирования результатов респираторных заболеваний), партнерство между научными кругами и промышленностью в рамках Инициативы Европейского Союза в области инновационных лекарственных средств.Очень раннее происхождение астмы, включая дородовое здоровье легких, будет по-прежнему в центре внимания 10, 11, особенно включая эпигенетические механизмы.
Аллергическая сенсибилизация — частый, но не обязательный признак астмы. Сенсибилизации иммуноглобулином Е к конкретным аллергенам недостаточно для развития аллергического заболевания. Недавние открытия были сосредоточены на функции эпителиального барьера; ORMDL3 , недавно было показано, что он играет важную роль в метаболизме сфингомиелина 12, и гены, экспрессируемые в эпителии, e.грамм. филаггрин 13 вовлечены в астму. Приводит ли сочетание снижения барьерной функции в сочетании с инфекцией и воздействием аллергенов к астме?
Хотя многие дети, страдающие астмой, легко поддаются лечению низкими дозами ингаляционных кортикостероидов, основная часть тяжелых резистентных к терапии астматиков продолжает иметь симптомы. Задача будет заключаться в том, чтобы охарактеризовать этих детей и выбрать подходящую новую, вероятно, цитокин-специфическую терапию для каждого человека. Мы должны найти способ безопасного и этичного тестирования этих лекарств у детей.
Муковисцидоз
В прошлом акцент на симптоматической терапии был важен, но лучшее понимание клеточных последствий мутаций трансмембранного регулятора проводимости при муковисцидозе (CFTR) привело к стратегиям, направленным на первичную аномалию. Генная терапия, специфическая фармакотерапия CFTR и модуляторы ионных каналов в настоящее время проходят клинические испытания, и некоторые соединения, вероятно, станут доступны в ближайшем будущем 14. В конечном счете, комбинированная терапия, направленная на различные аспекты клеточной дисфункции ( e.грамм. внутриклеточный трафик и открытие каналов) может показать наивысшую эффективность, но определение лучших комбинаций будет сложной задачей.
Скрининг новорожденных, вероятно, станет доступным по всей Европе в следующем десятилетии. Одной ранней диагностики и оказания помощи при МВ будет недостаточно, чтобы избежать раннего повреждения легких 15. Хотя в настоящее время проводятся исследования для поиска более эффективных стратегий раннего вмешательства, не существует проверенных критериев оценки результатов для младенцев и детей младшего возраста.Поэтому, параллельно с разработкой новых методов лечения, валидация новых критериев оценки результатов является высокоприоритетной задачей в ближайшем будущем 16.
Первичная цилиарная дискинезия и бронхоэктазы без МВ
При первичной цилиарной дискинезии (ПЦД) знания о спектре генных мутаций и их функциональных последствиях, скорее всего, увеличатся. В сочетании с неинвазивными скрининговыми тестами, такими как определение оксида азота в носу, эти знания помогут уточнить частоту этого недиагностированного заболевания 17.Спектр цилиопатии постоянно расширяется: цилиарная дисфункция обнаруживается при кистозной болезни почек и печени, пигментном ретините, гетеротаксии и врожденных пороках сердца, а также при сложных синдромах. Множественные функции первичных, узловых и подвижных ресничек только начинают изучаться, и это, несомненно, станет основным направлением исследований. Стратегии лечения в значительной степени скопированы с CF. Продольные обсервационные исследования помогут определить ключевые факторы, которые вызывают структурное повреждение дыхательных путей как при бронхоэктазах, так и при бронхоэктазах, не связанных с МВ.
Детская медицина сна
Текущее исследование сосредоточено на оценке распространенности обструктивного апноэ во сне (СОАС) и на взаимосвязи СОАС с последующими сердечно-сосудистыми заболеваниями, неврологическими нарушениями и метаболическим синдромом. Лечение ОАС у детей непросто и непросто, и в настоящее время существует очень мало данных о том, каким должен быть порог лечения или какими будут последствия недостаточного лечения. 18. Детская медицина сна — одна из многих областей, которые пострадает от эпидемии детского ожирения.В центре внимания исследований в этой области будет разработка клинических методов скрининга детей из группы риска и определение триггерных точек, которые приведут к более подробному исследованию или вмешательству.
Трансплантация легких у детей
Трансплантация легких у детей — это гораздо меньшая область, чем трансплантация легких у взрослых. Поэтому неизбежно, что исследования в педиатрии ограничены, и что многие достижения являются следствием исследований и практики взрослых. Об улучшении исходов у взрослых также сообщалось в педиатрической практике, при этом международные данные теперь сообщают о средней выживаемости после трансплантации около 5 лет, а некоторые центры сообщают об исходах лучше, чем это 19.
В центре внимания следующего десятилетия будет сотрудничество со взрослыми коллегами для разработки нового определения синдрома облитерирующего бронхиолита и хронической дисфункции трансплантата, которые, в свою очередь, могут послужить трамплином для лучшего понимания патофизиологии и потенциального лечения этого гетерогенного состояния.
ИНСТРУМЕНТЫ МОНИТОРИНГА
Детская респираторная физиология
За последнее десятилетие в области физиологии дыхания у детей всех возрастов произошли важные достижения.Произошла дальнейшая стандартизация тестирования функции легких у младенцев, до такой степени, что подавляющее большинство лабораторий функции легких у детей грудного возраста теперь используют коммерческое оборудование и проводят тестирование в соответствии с протоколами, согласованными на международном уровне. В тот же период был ликвидирован разрыв между функцией легких у младенцев и функцией легких школьного возраста. Сотрудничество между международными группами исследователей в области стандартизации и контроля качества завершилось публикацией в 2007 году совместного руководства Европейского респираторного общества / Американского торакального общества 20.Третьей важной особенностью последнего десятилетия стало возрождение интереса к альтернативным функциональным измерениям. Вымывание инертным газом, осциллометрия, сопротивление прерывателя, плетизмографическое сопротивление дыхательных путей и структурированная световая плетизмография — все это значительно продвинулось вперед. Во многих случаях это не новые методы, а развитие и модификации старых идей.
Задача следующего десятилетия будет заключаться в том, чтобы предоставить клиницистам и исследователям новые инструменты для ведения отдельных пациентов и в качестве критериев оценки результатов в эпидемиологических и интервенционных исследованиях.
Эндоскопия дыхательных путей у детей
Ультратонкие гибкие инструменты с рабочим каналом 1,2 мм могут использоваться для пересечения и исследования всего дыхательного пути, от ноздри до бронха, с минимальным механическим искажением анатомии и динамики дыхательных путей.
Сегодня детская гибкая бронхоскопия (ФБ) — это хорошо зарекомендовавшее себя диагностическое исследование. Оценка обструкции дыхательных путей, которая может затрагивать верхние и нижние дыхательные пути или и то, и другое, является наиболее частым показанием для ФБ у младенцев 21.
Диагностическая ценность FB во многих клинических случаях может быть увеличена за счет информации, полученной с помощью бронхоальвеолярного лаважа (БАЛ) 22. БАЛ является важным инструментом в диагностике легочной инфекции как у детей с ослабленным иммунитетом, так и у иммунокомпетентных детей, поскольку патогены можно легко идентифицировать из небольшие образцы БАЛ. У детей с хроническими ВЗЛ БАЛ может играть важную роль в исключении или подтверждении конкретного диагноза, в характеристике альвеолита и в наблюдении за пациентом во время лечения и последующего наблюдения.
Интервенционная бронхоскопия становится все более важной и включает восстановление проходимости или стабильности дыхательных путей или удаление тканей или веществ из дыхательных путей или альвеолярных пространств, которые мешают нормальному функционированию. Интервенционная бронхоскопия включает лазерную терапию, расширение стеноза дыхательных путей, установку стента, тотальный лаваж легких и лечение бронхоплевральных свищей 23. Наши коллеги во взрослой практике опережают нас в таких методах, как эндобронхиальное ультразвуковое исследование; поскольку оборудование миниатюризировано, дети смогут извлечь пользу из этих методик.По-прежнему необходимы более совершенные инструменты, лучшая подготовка и лучшие исследовательские приложения эндоскопии для улучшения нашего понимания детских респираторных заболеваний.
ИНТЕНСИВНАЯ УХОД
В педиатрической интенсивной терапии достигнут значительный прогресс. Защита легких от баротравмы и волютравмы, вызванной вентилятором, по-прежнему заставляет нас снижать давление и объемы. Этому способствуют новейшие технологии в аппаратах ИВЛ, и перспектива создания аппаратов ИВЛ, управляемых пациентом ( e.грамм. ИВЛ) близко. Наше понимание инфекций, связанных с аппаратом искусственной вентиляции легких, также помогает минимизировать заболеваемость, и уроки взрослой практики показывают нам, насколько можно избежать таких осложнений. Также растет признание того, что долгосрочное лечение детей с нервно-мышечными заболеваниями требует решения 24.
СЛАВНОЕ ПРОШЛОЕ, БОЛЬШОЕ БУДУЩЕЕ
Увеличится число выживших детей, родившихся очень преждевременно (до 25 недель беременности, вес при рождении <500 г).Для взрослых врачей это будет новая группа пациентов с высоким риском развития ХОБЛ.
Бронхит и бронхиолит, вызванный вирусами, по-прежнему будет причиной респираторных заболеваний у младенцев и детей дошкольного возраста. Эффективного лечения бронхиолита не существует, и этот пробел необходимо восполнить. Дальнейшая разработка вакцин для профилактики ранних инфекций может иметь большое влияние на риск астмы в более позднем детстве. Нам нужны стратегии для предотвращения эпизодических (вирусных) хрипов, прогрессирующих до множественных триггерных хрипов и астмы.Мы знаем, что ингаляционные кортикостероиды не могут предотвратить это изменение. Нужны новые идеи.
Астма есть и будет самым распространенным хроническим заболеванием у школьников и подростков. При аллергическом рините и астме новые индивидуализированные вакцины против аллергии могут стать возможным лечением для предотвращения астмы и / или ухудшения состояния. Важное значение будут иметь новые методы лечения и биомаркеры для отбора детей и отслеживания результатов лечения.
При МВ, диагностированном при скрининге новорожденных, нам нужны новые терапевтические комбинации, чтобы изменить заболеваемость.Поскольку лечение, специфичное для генотипа, становится доступным и, скорее всего, применяется к маленьким детям до того, как болезнь прогрессирует, нам нужны биомаркеры для отбора тех, кто подвержен риску более быстрого ухудшения, и подтвержденные конечные точки у очень маленьких детей, чтобы оценить ответ на лечение. Риск обострения туберкулеза и особенно заболеваний с множественной лекарственной устойчивостью и широкой лекарственной устойчивостью требует внимания со стороны многих специалистов и международного сообщества. То же самое верно и для других возникающих инфекций, например, устойчивых к метициллину Staphylococcus aureus .Новые диагностические инструменты, такие как тесты на интерферон-гамма, могут дать более точные результаты, чем туберкулиновая кожная проба.
Мы будем становиться все лучше и лучше в спасении очень больного ребенка. Химиотерапия при раке и трансплантация костного мозга, легких и других твердых органов улучшит прогноз злокачественных новообразований и прогрессирующих заболеваний легких, таких как ILD, у детей. И наоборот, это приведет к усилению легочных осложнений. Мы должны быть начеку, чтобы обнаруживать эти новые осложнения и правильно управлять ими.
Использование технологий, как неинвазивных, так и инвазивных, для сохранения жизни детей с неврологическими заболеваниями и заболеваниями дыхательных путей и дома будет приобретать все большее значение. По мере того, как дети младшего возраста используют эти методы, все большее значение приобретает разработка ориентированных на детей машин и интерфейсов.
Орфанные болезни легких, такие как легочный фиброз неизвестного происхождения, аутоиммунные заболевания с легочными осложнениями, ILD и врожденные пороки развития дыхательных путей, будут по-прежнему создавать бремя для здравоохранения и потребовать высокоспециализированных центров третичной помощи.Все чаще международные сети сотрудничают, чтобы собрать большое количество пациентов, чтобы узнать больше об этих пациентах.
Так каковы темы прошлых десятилетий и будущего? Проделана большая работа, но разрабатывается еще много вопросов 25; Прежде всего, нам необходимо горизонтальное сотрудничество между группами детских пульмонологов-специалистов и вертикальное сотрудничество со взрослыми коллегами-респираторами. Будущее за молодыми педиатрами-пульмонологами, и мы должны обеспечить их максимально возможную подготовку; Инициатива pHERMES претендует на это 26. Floreat ERS !
Что такое интерстициальная болезнь легких у детей?
Детское интерстициальное заболевание легких, известное как «ДЕТИ», представляет собой группу редких заболеваний легких, поражающих младенцев, детей и подростков.
Все формы ДЕТЕЙ вызывают повреждение легких у ребенка, поэтому они не работают должным образом.
Многие типы детей поражают интерстиций, тонкую ткань между крошечными воздушными мешочками и кровеносными сосудами в легких. Некоторые виды ДЕТЕЙ поражают и другие участки легких.
Врачи только начали понимать это состояние за последние несколько лет, и многого они не знают. Например, они не знают, у скольких детей есть РЕБЕНКИ.
Среди детей, страдающих ДЕТЯМИ, некоторые рождаются с ним, а другие имеют его позже в детстве. Взрослые тоже могут получить интерстициальное заболевание легких, но его причины и исходы часто бывают разными.
Причины
РЕБЕНОК может возникнуть без известной причины. С другой стороны, виновниками могут быть определенные гены, токсины или другие заболевания.
Некоторые возможные причины:
Унаследованные состояния : Заболевания, вызывающие проблемы с сурфактантом — жидкостью в легких, которая помогает вашему ребенку дышать, — могут передаваться через гены.
Продолжение
Расстройства иммунной системы : Определенные проблемы иммунной системы затрудняют детям борьбу с болезнями.
Аутоиммунные заболевания : они возникают, когда иммунная система вашего ребенка по ошибке атакует здоровые ткани.Воспалительное заболевание кишечника и заболевание коллагеновых сосудов — два аутоиммунных состояния, обычно связанных с ДЕТИ.
Инфекция : Некоторые дети заболевают ДЕТЯМИ после простуды или вируса.
Врожденные дефекты : Дети могут родиться с врожденным дефектом, вызывающим проблемы с легкими.
Аспирация : При вдыхании пищи, жидкости или рвоты в легкие может произойти повреждение. Аспирация часто поражает детей с проблемами глотания или состоянием, называемым гастроэзофагеальной рефлюксной болезнью (ГЭРБ).
Лечение рака : Лечение, такое как лучевая терапия и химиотерапия, может привести к развитию ДЕТЕЙ.
Триггеры окружающей среды : Химические вещества и плесень могут раздражать легкие вашего ребенка.
Операции : В некоторых случаях ДЕТЕЙ виноват трансплантат легкого или трансплантат костного мозга.
Типы
Существуют разные виды ДЕТЕЙ. У многих длинные, трудно произносимые имена. Хотя все они считаются редкими заболеваниями, некоторые формы чаще встречаются в определенных возрастных группах.
Продолжение
Заболевания детей, которые обычно поражают младенцев:
- Мутации, связанные с дисфункцией сурфактанта
- Нарушения развития, такие как дисплазия альвеолярных капилляров
- Нарушения роста легких
- Нейроэндокринная клеточная гиперплазия в младенческом возрасте (NEHI) PIG)
Типы детей, которые чаще встречаются у детей и подростков:
Идиопатические интерстициальные пневмонии : В эту категорию входят криптогенная организующая пневмония, острая интерстициальная пневмония, неспецифическая интерстициальная пневмония, десквамативная интерстициальная пневмония и лимфатическая пневмония.
Другие первичные заболевания: Этими заболеваниями могут быть синдромы альвеолярных кровоизлияний, синдромы аспирации, гиперчувствительный пневмонит, облитерирующий бронхиолит, эозинофильная пневмония, легочный альвеолярный протеиноз, легочные инфильтраты с эозинофилией, легочные лимфатические и сосудистые заболевания (лимфатические и легочные сосудистые заболевания) (гемангиоматоз).
ILD, связанные с системными болезнями: Примеры: заболевания соединительной ткани, гистиоцитоз, заболевания легких, связанные со злокачественными новообразованиями, саркоидоз и болезни накопления.
Заболевания ослабленной иммунной системы: В эту группу входят оппортунистические инфекции, расстройства, связанные с терапевтическим вмешательством, заболевания легких, связанные с трансплантацией костного мозга, и диффузное поражение альвеол неизвестной причины.
Симптомы
Признаки и симптомы ребенка часто зависят от типа заболевания и степени его тяжести. Они могут включать:
- Затрудненное дыхание или одышку
- Быстрое или шумное дыхание
- Свистящее дыхание
- Кашель или заложенность грудной клетки
- Повторные приступы пневмонии или бронхита
- Низкий уровень кислорода
- Неспособность набрать вес или набрать вес высота
Взрослые vs.Детское интерстициальное заболевание
Некоторые дети, которые заболевают ДЕТЯМИ, будут иметь это заболевание на протяжении всей жизни, поэтому технически это может произойти как у детей, так и у взрослых.
Но когда у взрослого диагностируется интерстициальное заболевание легких, врачи обычно считают его совершенно другим заболеванием, чем ребенок.
Детям с детьми следует обращаться к детскому пульмонологу, а не к врачу, специализирующемуся на взрослых.
Диагноз
Часто бывает трудно диагностировать ДЕТЕЙ.Каждый тип индивидуален, поэтому методы, которые использует ваш врач, будут разными.
Тесты, которые помогают диагностировать ДЕТЯ, включают:
Рентген грудной клетки или компьютерная томография: Эти процедуры визуализации используют рентгеновские лучи, чтобы сделать снимки легких вашего ребенка.
Функциональные тесты легких : Врачи измеряют, как дети дышат и выдыхают, чтобы проверить, насколько хорошо работают их легкие.
Анализы крови : Забор крови иногда используется для проверки аномальных генов.
Бронхоальвеолярный лаваж : С помощью этой процедуры врач вводит соленую воду через трубку в легкие вашего ребенка, чтобы увидеть определенные типы клеток.Это может помочь обнаружить травму легких, аспирацию, инфекцию или проблемы с дыхательными путями.
Биопсия легкого : Хирург извлекает небольшой кусочек легочной ткани для исследования в лаборатории.
Лечение
Было проведено очень мало исследований по лечению ДЕТЕЙ. Но некоторые методы лечения могут помочь легким детей работать лучше, облегчить симптомы или просто улучшить их самочувствие.
Ваш врач может порекомендовать:
Лекарства : стероиды уменьшают воспаление легких, противомикробные препараты лечат инфекции, а бронходилататоры помогают расслабить мышцы вокруг дыхательных путей.
Кислород : Больше кислорода может помочь детям лучше дышать и дать их сердцу отдых.
Питание : План питания, ориентированный на увеличение веса, может принести пользу некоторым детям с ДЕТЯМИ.
Легочная реабилитация и упражнения : Специальные методы лечения направлены на облегчение заложенности и улучшение работы легких (ваш врач может назвать это «функцией легких»).
Дыхательные аппараты : Аппараты, называемые вентиляторами, помогают детям легче дышать.
Трансплантация легких : Это может быть вариант для детей с серьезными или опасными для жизни случаями ДЕТЕЙ. Пока что у детей, перенесших операцию, похоже, что они не возвращаются.
Каковы перспективы?
При отсутствии лекарства для ДЕТЯ заболевание возникает и прогрессирует по-разному у каждого ребенка.
Некоторые случаи тяжелые и, как правило, опасны для жизни в раннем возрасте. Другие типы остаются такими же или медленно ухудшаются. Но некоторые формы заболевания, такие как гиперплазия нейроэндокринных клеток в младенчестве, со временем могут даже улучшиться.
У детей с ДЕТЯМИ могут быть особые потребности. Было бы неплохо поговорить с учителями, членами семьи и другими родителями о том, как поддержать вашего ребенка и остальных членов вашей семьи. Позаботьтесь и о собственном здоровье. Воспитатели часто ставят себя в последнюю очередь, но вам нужно быть здоровым, чтобы помочь своей семье.
Динамика смертности детей от респираторных заболеваний в Англии и Уэльсе с 1968 по 2000 год
Детская смертность заметно снизилась в промышленно развитых странах за последние три десятилетия. 1– 3 Это падение объясняется многими различными улучшениями в сфере здравоохранения, включая иммунизацию, достижениями в первичной, вторичной и неонатальной помощи, а также более глубоким пониманием и лечением детских болезней.
Респираторные инфекции и астма являются одними из самых распространенных детских болезней, на их долю приходится более пятой части всех консультаций терапевтов и 15% всех госпитализаций детей в Великобритании. 4, 5 Большинство респираторных заболеваний у детей носят незначительный характер и проходят самостоятельно, но меньшая часть эпизодов острых и хронических респираторных заболеваний приводит к летальному исходу.Например, в 1999 г. на респираторные заболевания приходилось 9,6% всех смертей в возрасте от 1 до 14 лет в Англии и Уэльсе, и только травмы и отравления (23,1%), злокачественные новообразования (18,4%) и заболевания центральной нервной системы (13,0%). вызвали больше смертей в том году. 3
Всем странам необходима точная эпидемиологическая информация для определения приоритетов, планирования, реализации и мониторинга вмешательств в области общественного здравоохранения. 3, 6 Было проведено несколько исследований детской смертности от отдельных респираторных заболеваний, таких как астма 7– 9 и муковисцидоз, 10, 11 , но мы не знаем о подробном анализе тенденции всех респираторных причин смерти детей в Англии и Уэльсе за длительный период.Целью этого исследования было изучить эти тенденции и проанализировать изменяющиеся модели смертности от отдельных заболеваний, которые являются причиной большинства респираторных смертей у детей, а именно пневмонии, астмы, муковисцидоза и бронхиолита.
МЕТОДЫ
Данные предоставлены Управлением национальной статистики (УНС). Они состояли из всех смертей, зарегистрированных от всех причин у детей в возрасте от 28 дней до 16 лет в Англии и Уэльсе с 1 января 1968 года по 31 декабря 2000 года.Данные включали год смерти, причину смерти в соответствии с Международной классификацией болезней (МКБ), возраст на момент смерти и пол. Коды восьмой редакции МКБ (МКБ-8) использовались с 1968 по 1978 год, а коды девятой редакции МКБ (МКБ-9) — с 1979 по 2000 годы. Мы определили смерть от респираторной причины как смерти, зарегистрированные в категориях МКБ 460–519.9 в сочетании со смертельным исходом. муковисцидозу (273,0 в МКБ 8, 277,0–277,01 в МКБ 9), туберкулезу легких (011–012,9 и 019,0 в МКБ 8 и 9), коклюше (коклюш) (033.0–033,9) и врожденные аномалии дыхательной системы (748,0–748,9).
Данные были проанализированы по четырем возрастным группам: младенцы постнеонатального возраста (возраст 28–364 дня), 1–5 лет, 6–10 лет и 11–16 лет. Показатели смертности были выражены на 100 000 населения с использованием среднегодовых возрастных групп населения, оцененных ONS. Неонатальная смерть (смерть младенцев в возрасте до 28 дней) была исключена по двум причинам: (1) потому что респираторные причины смерти у новорожденных сильно различаются 4 и (2) с момента введения свидетельства о неонатальной смерти в 1986 г. не удалось установить первопричину смерти в этой возрастной группе. 12
Мы рассчитали общие коэффициенты смертности, возрастные коэффициенты смертности от всех респираторных причин, а также конкретные коэффициенты пневмонии, астмы, муковисцидоза и коэффициенты постнеонатальной детской смертности от бронхиолита. Смертность от бронхиолита анализировалась с 1979 по 2000 год, поскольку в МКБ-9 использовалась отдельная кодировка МКБ для острого бронхиолита. В МКБ-8 острый бронхит и бронхиолит кодировались вместе (466).
Stata версии 8 и SPSS версии 11.0 использовались для статистического анализа.
РЕЗУЛЬТАТЫ
Коэффициенты смертности от всех причин для детей в возрасте от 1 до 16 лет составляли 49,9 на 100 000 в 1968 году, 29,6 в 1985 году и 16,3 в 2000 году. Коэффициенты смертности от респираторных заболеваний в этой возрастной группе составляли 8,6, 2,6 и 1,3 на 100 человек. 000 в 1968, 1985 и 2000 годах соответственно (рис. 1). Доля смертей от респираторных заболеваний среди детей в возрасте от 1 до 16 лет снизилась с 17,3% в 1968 году до 8,8% в 1985 году и 8,0% в 2000 году (рис. 1).К 2000 году пневмония (43%), астма (20%) и кистозный фиброз (10%) составляли 73% из 138 случаев смерти от респираторных заболеваний в возрасте от 1 до 16 лет.
Рисунок 1Показатели смертности и процент смертей от респираторных заболеваний у детей в возрасте 1–16 лет с 1968 по 2000 год.
Гораздо более высокие показатели смертности наблюдались у младенцев в постнеонатальном периоде (возраст 28–364 дня). В этой группе общий уровень смертности снизился с 592.8 в 1968 году до 397,6 в 1985 году и 176 в 2000 году. Смертность от респираторных заболеваний у этих младенцев составляла 280, 65,1 и 22,8 в 1968, 1985 и 2000 годах, соответственно. Процент смертей от респираторных заболеваний в этой возрастной группе снизился с 47,2 в 1968 году до 16,4 в 1985 году и до 13,0 в 2000 году (рис. 2).
Рисунок 2Показатели смертности и процент смертей от респираторных заболеваний у новорожденных в постнеонатальный период (в возрасте от 28 до 364 дней) с 1968 по 2000 год.
Смертность от детской пневмонии снизилась во всех возрастных группах (рис. 3). Наиболее разительное изменение произошло у младенцев в постнеонатальном периоде, где уровень смертности снизился со 165 на 100 000 в 1968 году до 27 в 1985 году и 6,78 в 2000 году, что составляет 96% в этой возрастной группе. Абсолютное число смертей, связанных с пневмонией у детей в возрасте от 28 дней до 16 лет, составило 1855 в 1968 г., 224 в 1985 г. и 101 в 2000 г., что на 95% меньше за 32 года.
Рисунок 3Смертность от пневмонии с 1968 по 2000 гг.
На рис. 4 показаны тенденции смертности от астмы в трех возрастных группах. Возрастные коэффициенты смертности от астмы резко снизились. Между 1968 и 2000 годами уровень смертности от астмы снизился на 78% (с 0,58 до 0,13) в возрасте от 1 до 5 лет, на 57% (с 0,53 до 0,23) в возрасте от 6 до 10 лет и на 73% (с 1,38 до 0,37). в возрасте 11–16 лет. У детей в возрасте 11–16 лет показатели были стабильно выше, чем у детей младшего возраста. В 1968 году от астмы умерло 99 детей в возрасте 1–16 лет по сравнению с 50 и 27 случаями смерти в 1985 и 2000 годах, соответственно.
Рисунок 4Смертность от астмы с 1968 по 2000 год.
Смертность от муковисцидоза снизилась во всех возрастных группах с конца 1960-х годов, при этом наиболее заметное снижение произошло среди младенцев в постнеонатальном периоде (рис. 5). Тенденции показателей смертности были очень похожи в группах 6–10 лет и 11–16 лет, поэтому они не показаны отдельно. Рост показателей смертности среди детей в возрасте 6–16 лет в конце 1970-х — начале 1980-х годов сопровождался падением показателей смертности среди младенцев и детей в возрасте 1–5 лет.В 1968 году 118 случаев смерти были отнесены на счет муковисцидоза у детей в возрасте от 28 дней до 16 лет по сравнению с 75 в 1985 году и 15 в 2000 году.
Рисунок 5Смертность от муковисцидоза с 1968 по 2000 год.
Тяжелый острый вирусный бронхиолит наблюдается почти исключительно у младенцев в возрасте от 1 месяца до 1 года. Смертность от бронхиолита у новорожденных в постнеонатальном периоде снизилась с 21,47 в 1979 г. до 1,82 в 2000 г. (рис. 6), а абсолютное число смертей упало со 137 до 11 в год за тот же период.
Рисунок 6Показатели смертности (на 100 000 человек) от бронхиолита у новорожденных в постнеонатальном периоде с 1979 по 2000 год.
Среднее (SD) соотношение показателей смертности мужчин и женщин в период с 1968 по 2000 год составляло 1,24 (0,17) от пневмонии, 1,41 (0,48) от астмы и 0,82 (0,28) от муковисцидоза для детей в возрасте от 28 дней до 16 лет и 1,77 ( 1.25) при бронхиолите у младенцев в постнеонатальном периоде. В течение периода исследования значимых тенденций в отношении показателей смертности мужчин и женщин от пневмонии, астмы, муковисцидоза или бронхиолита не наблюдалось.
ОБСУЖДЕНИЕ
Мы показали, что, как и во всех промышленно развитых странах, уровень детской смертности в Англии и Уэльсе за последние 32 года резко снизился. Показатели смертности от респираторных заболеваний снизились более круто, чем общие показатели, и теперь гораздо меньшая доля детских смертей вызвана респираторными заболеваниями, чем в прошлом. Наибольшие улучшения были у младенцев и детей младшего возраста. Между 1968 и 2000 годами уровень постнеонатальной смертности от всех причин снизился на 70%, а уровень смертности от респираторных заболеваний снизился на 92%.В 1968 году почти половина смертей младенцев в постнеонатальном периоде была связана с респираторными заболеваниями, но к 2000 году эта доля упала до 13%. В период с 1968 по 2000 год среди детей в возрасте от 1 до 16 лет показатели общей смертности и смертности от респираторных заболеваний снизились на 67% и 85% соответственно, а процент смертей от респираторных заболеваний упал с 17,3 в 1968 году до 8,8 в 1985 году и до 8,0. в 2000 г.
У этого исследования есть некоторые ограничения. Значительная часть младенцев и детей, которые умирают от пневмонии или бронхиолита, имеют серьезное основное заболевание, такое как врожденные аномалии кардиореспираторной системы или ЦНС, хромосомные аномалии или иммунодефицит.УНС не собирает и не предоставляет данные об этих важных сопутствующих состояниях, которые значительно предрасполагают детей к смерти от респираторных заболеваний. Поэтому мы не можем комментировать их вклад в тенденции, о которых мы сообщаем. В течение анализируемого периода произошло несколько изменений в сборе данных УНС и его предшественниками. Между 1984 и 1992 годами произошли изменения в выборе основной причины смерти из свидетельства о смерти. С 1993 года для определения причины смерти использовалось автоматическое кодирование.Было высказано предположение, что на изменения показателей смертности от пневмонии с 1993 г. могли повлиять изменения в сборе данных, но точно количественно оценить эти эффекты сложно. 12, 13 Однако наши данные не показывают какого-либо резкого изменения смертности от пневмонии у детей во время этих изменений.
Изменения в кодировке МКБ также могут повлиять на уровень смертности от астмы. 14 Например, в 1979 г., с введением девятой редакции МКБ (МКБ-9), смертность от астмы с упоминанием бронхита регистрировалась как неуточненная астма (493.9), а не бронхит (490). Это изменение классификации привело к очевидному увеличению числа смертей от астмы, особенно у взрослых, у которых может быть путаница с другими заболеваниями, такими как хроническая обструктивная болезнь легких. Стюарт и Нанн 15 сообщили, что переход от кодирования МКБ-8 к МКБ-9 вызвал явное 28% -ное увеличение смертности от астмы среди всего населения, хотя в более молодых возрастных группах эффект был меньше. Обследование случаев смерти от астмы в Англии показало, что свидетельство о смерти было более точным у молодых людей, чем у пожилых. 16 Sears et al 17 показали, что в Новой Зеландии точность сертификации смертей от астмы составляла 100% у пациентов младше 35 лет по сравнению с 50% у пациентов старше 70 лет. Однако существует мало свидетельств того, что изменения в диагностической маркировке клиницистами или в кодировке МКБ объясняют изменения в уровне смертности от астмы у детей, которые мы описываем.
Поскольку пневмония, астма, муковисцидоз и бронхиолит вместе составляли большую часть смертей от респираторных заболеваний у детей в возрасте от 28 дней до 16 лет в исследуемый период, мы изучили эти состояния более подробно.
Смертность от детской пневмонии снизилась во всех возрастных группах. Ставки резко упали между 1968 и серединой 1980-х годов и с тех пор выровнялись. Наибольшее снижение было у младенцев в постнеонатальном периоде, но даже сейчас большинство детских смертей от пневмонии происходит на первом году жизни. В 2000 г. 40% случаев смерти детей в возрасте от 28 дней до 16 лет от пневмонии приходилось на младенцев в постнеонатальном периоде. Наши данные не могут объяснить, почему снизилось количество случаев смерти детей от пневмонии, но вполне вероятно, что улучшение первичной, вторичной и специализированной помощи, использования противомикробных препаратов и иммунизации способствовало этому снижению.Например, Mulholland и др. 18 сообщили, что конъюгированная вакцина HiB ( Haemophilus influenzae B), которая была введена в Великобританию в 1992 г., на 95% эффективна в предотвращении инвазивной болезни HiB, на 100% — в профилактике пневмонии HiB. и эффективен в предотвращении 21% всех пневмоний, определенных рентгенологически. Высокий уровень защиты от коклюша и кори, обеспечиваемый иммунизацией, также, вероятно, повлиял на смертность. Важно изучить влияние предлагаемой программы вакцинации детей от пневмококка на смертность от пневмонии в этой популяции.Эти данные могут предоставить ценную основу для оценки воздействия новых клинических мер общественного здравоохранения, которые могут быть введены в ближайшем будущем. Например, было показано, что универсальная программа иммунизации против пневмококковой инфекции является высокоэффективной в предотвращении инвазивного пневмококкового заболевания, при этом частота радиологически подтвержденной пневмонии у детей снижается примерно на 25%. 19
Мы обнаружили, что за снижением показателей смертности от астмы до середины 1970-х последовал рост в 1980-х, дальнейшее падение в начале 1990-х и стабилизация с середины 1990-х.Эта картина несколько отличается от других стран. В Соединенных Штатах у детей в возрасте 0–17 лет смертность от астмы увеличивалась в среднем на 3,4% в год с 1980 по 1998 год. 8 В Австралии и Германии смертность от астмы в детстве увеличилась в период с середины 1970-х годов. и середина 1980-х гг. 20 Кэмпбелл и др. сообщили о нерегулярной тенденции к снижению у детей в возрасте 5–14 лет с 1983 по 1995 год в Англии и Уэльсе со средним падением около 6% в год. 9
Выживаемость детей и взрослых с муковисцидозом резко улучшилась за последние 30 лет. 21 В 1968 г. было 118 случаев смерти детей от муковисцидоза, но к 2000 г. их было только 15. Небольшое увеличение смертности среди детей в возрасте 6–16 лет в 1970–1980-е гг. Коэффициенты постнеонатальной смертности и смертности в возрасте 1–5 лет, что позволяет предположить, что это отражает выживаемость до более позднего возраста. Такое улучшение выживаемости связано с множеством факторов, включая более раннюю диагностику и более интенсивное и эффективное лечение.Возможно, на эти цифры повлияли изменения в кодировке и свидетельстве о смерти, а также более точный диагноз. В прошлом признание случаев смерти от муковисцидоза могло быть неполным, а показатели смертности могли быть недооценены. Мы не можем оценить влияние на смертность от муковисцидоза факторов, которые могут изменить распространенность заболевания, таких как пренатальная диагностика с терапевтическим прекращением или неонатальный скрининг, который стал доступным в период нашего исследования.
Острый вирусный бронхиолит — важная причина госпитализаций младенцев и необходимости интенсивной терапии. Смертность от бронхиолита у новорожденных в постнеонатальном периоде снизилась более чем на 92% в период с 1979 по 2000 год. За это время не было изменений в кодировке МКБ и никаких свидетельств каких-либо изменений в распространенности бронхиолита. Вероятно, что сокращение числа смертей отражает улучшение педиатрической помощи, особенно педиатрической интенсивной терапии.
В заключение, мы наблюдаем заметное и прогрессирующее снижение детской смертности от респираторных заболеваний.Это снижение было более быстрым, чем снижение детской смертности от всех причин, поэтому сегодня меньшая доля детских смертей является результатом респираторных заболеваний. Наиболее существенно снизилась смертность от пневмонии в первый год жизни.
Благодарности
Авторы благодарят Мойру Микельбург из Управления национальной статистики за предоставленные данные.
ССЫЛКИ
- ↵
- ↵
Логан С .Эпидемиология здоровья детей. В: Макинтош Н., Хелмс П., Смит Р., ред. Учебник педиатрии Форфара и Арнея. 6-е изд. Эдинбург: Черчилль Ливингстон, 2003.
- ↵
Кристофер А , Кроули С. Бремя респираторных заболеваний в детстве. Airways J2004; 2: 104–7.
- ↵
Couriel J . Обследование ребенка с рецидивирующими инфекциями дыхательных путей. Br Med Bull, 2002; 61: 115–32.
- ↵
Black RE , Morris SS, Bryce J. Где и почему ежегодно умирают 10 миллионов детей? Lancet2003; 361: 2226–34.
- ↵
Берни П. . Смертность от астмы в Англии и Уэльсе в 1931–1985 гг .: свидетельство реального увеличения смертности от астмы. J Epidemiol Community Health 2988; 42: 316–20.
- ↵
Akinbami LJ , Schoendorf KC.Тенденции астмы у детей: распространенность, обращение за медицинской помощью и смертность. Педиатрия, 2002; 110: 315–22.
- ↵
Campbell MJ , Cogman GR, Holgate ST, et al. Возрастные тенденции смертности от астмы в Англии и Уэльсе, 1983–1995 годы: результаты обсервационного исследования. BMJ1997; 314: 1439–41.
- ↵
Кулич М , Розенфельд М, Госс Ч., и др. Повышение выживаемости среди молодых пациентов с муковисцидозом.Журнал Педиатр, 2003; 142: 631–6.
- ↵
Halliburton CS , Mannino DM, Olney RS. Смертность от муковисцидоза в США с 1979 по 1991 год. Анализ с использованием данных о смертности от множественных причин. Arch Pediatr Adolesc Med 1996; 150: 1181–5.
- ↵
Управление национальной статистики . Статистика смертности: причина. Обзор генерального регистратора смертей с разбивкой по причинам, полу и возрасту в Англии и Уэльсе, 2001 г.Dh3 № 28. Управление национальной статистики 2002.
- ↵
Руни К. , Дэвис Т. Тенденции смертности по причинам смерти в Англии и Уэльсе 1980–94: влияние внедрения автоматизированного кодирования и связанных с этим изменений в 1993 г. Popul Trends 1996; 86: 29–35.
- ↵
Jannsen F , Kunst AE. Изменения в кодировании по МКБ и разрывы в тенденциях смертности от конкретных причин в шести европейских странах, 1950–1999 гг.Bull WHO2004; 82: 904–13.
- ↵
Стюарт CJ , Нанн AJ. Меняются ли показатели смертности от астмы? Br J Dis Chest 1985; 79: 229–234.
- ↵
Исследовательский комитет БТА . Точность свидетельств о смерти при бронхиальной астме. Thorax1984; 39: 505–9.
- ↵
Sears MR , Rea HH, de Boer G, et al. Точность удостоверения смертей от астмы.Национальное исследование. Am J Epidemiol1986; 124: 1004–11.
- ↵
Mulholland K , Hilton S, Adegbola R, et al. Рандомизированное испытание конъюгированной вакцины против столбняка с белком Haemophilus influenzae типа b для профилактики пневмонии и менингита у младенцев в Гамбии. Lancet1997; 349: 1191–7.
- ↵
О’Брайен К.Л. , Сантошем М. Потенциальное влияние конъюгированной пневмококковой вакцины на детские пневмококковые заболевания.Am J Epidemiol2004; 159: 634–44.
- ↵
Jackson R , Sears MR, Beaglehole R, et al.

 д.), способствующих напряжению иммунной системы и приводящих к развитию вторичных иммунодефицитных состояний, что способствует хронизации инфекции, особенно вирусной (чаще герпетической).
д.), способствующих напряжению иммунной системы и приводящих к развитию вторичных иммунодефицитных состояний, что способствует хронизации инфекции, особенно вирусной (чаще герпетической). 

 Обязательно умывайтесь не менее 20 секунд теплой водой с мылом, чтобы убить вирусы или бактерии, которые могут оставаться на вашей коже.
Обязательно умывайтесь не менее 20 секунд теплой водой с мылом, чтобы убить вирусы или бактерии, которые могут оставаться на вашей коже.