История лечения ринита и хронического насморка
Насморк – это воспаление слизистой оболочки носа. Он бывает острый и хронический. В самостоятельную группу выделяют вазомоторный ринит, лечение которого — штука непростая и требует высокой квалификации врача. Вазомоторный насморк в свою очередь делится на нейровегетативный и аллергический.
Когда в результате не вылеченного насморка отмирают ворсинки слизистого эпителия и нарушаются физиологические функции, развивается атрофический ринит. Причиной любого насморка являются нарушение местного иммунитета или внешние факторы. Наша носоглотка устроена таким образом, что препятствует проникновению пыли и самых разнообразных мелких частиц, находящихся в воздухе, в которых обитает огромное количество бактерий и вирусов.
Слизистая оболочка носа покрыта эпителием с миллионами мельчайших ресничек. Реснички постоянно двигаются и выталкивают из полости носа инородные частицы. Но это еще не всё! Слизистая оболочка носа содержит активные защитные белки. Они называются иммуноглобулины класса «А». Когда иммунитет человека снижен, болезнетворные микроорганизмы переходят к активной атаке.
А внешние факторы это всё то, с чем мы сталкиваемся на протяжении всей жизни. Когда мы замерзаем, устойчивость нашего организма резко снижается, и микробы начинают активно развиваться. Кроме того, ринит часто возникает на фоне инфекционных заболеваний. К внешним факторам относят травмы и попадание чужеродных объектов в полость носа, особенно у маленьких детей.
В отдельную группу выделяют аллергические насморки, вызванные вдыханием цветочной пыльцы, тополиного пуха, домашней пыли, а также выделения из носа, возникшие в результате воздействия токсинов и химических отходов на вредных производствах.
Ринит. Симптомы болезни
Острый насморк проходит несколько стадий:
- первая, при которой наблюдается сухость в носу, чувство жжения и щекотки
- вторая, при которой появляются жидкие выделения из носа
- третья, во время которой выделения из носа сгущаются и приобретают неприятный запах.

Ринит, симптомы которого могут включать повышение температуры тела, головную боль и слезотечение, при хорошей сопротивляемости организма проходит в течение недели
Первая стадия может длиться от нескольких часов до нескольких дней. Когда сухость жжение в полости носа проходят и появляются слизистые обильные выделения, ринит, симптомы которого приобретают более ярко выраженные формы, переходит во вторую стадию. Этот период характеризуется заложенностью носа и затрудненностью дыхания. На 4-5 день от начала заболевания наступает третья стадия с гнойными и густыми выделениями. При низкой сопротивляемости организма, ринит, симптомы которого усиливаются, приобретает хроническую форму, что часто приводит к самым разнообразным осложнениям.
Как лечили насморк раньше? Сейчас страшно представить, но самым любимым лекарством в Европе был лауданум, то есть настойка опия. В обычном скромном флакончике содержалось около 10% опия в порошке. Лауданом лечили всё – от насморка и кашля до приступов эпилепсии! А героином от фирмы «Bayer» американские мамочки лечили насморк у своих деток.
Ну а как же не лечить, если героин одобрила Американская медицинская ассоциация! Кстати, тогда считалось, что это вещество не вызывает зависимости. Наркотики для лечения насморка были сняты с производства только в 1913 году. В древности, для того, чтобы вылечить насморк, люди нюхали табак и делали кровопускание.
Традиционные современные методы лечения насморка часто сводятся к бесконтрольному применению сосудосуживающих капель. Нередко врачи прибегают к хирургическому лечению. Но, ни консервативные, ни хирургические методы часто не решают проблему. Сосудосуживающие капли, которые больные закапывают годами, ведут к серьезным осложнениям, последствия которых трудно устранить.
Лечение, которое применяется в нашей клинике, не имеет ничего общего с традиционным. Мы первые в России использовали холодноплазменную хирургию — коблацию. Коблация – прорыв в лечении насморка различной этиологии даже для мировой практики.
Мы первые в России использовали холодноплазменную хирургию — коблацию. Коблация – прорыв в лечении насморка различной этиологии даже для мировой практики.
При любом хирургическом методе лечения существует риск кровотечения из носа. Метод, применяемый нами, полностью исключает этот риск, поскольку здесь не происходит повреждения слизистой оболочки. Длительность процедуры всего 10-15 минут. Необходимости в реабилитационном периоде нет, и пациент может сразу вернуться к привычному для себя образу жизни.
Мы проводим лечение с помощью уникального итальянского аппарата «QUASAR», использующего принципмолекулярно-квантового резонанса. Наши высококвалифицированные специалисты, обладающие большим опытом, выполнят магнитно-квантовую редукцию нижних носовых раковин. Совместно с холодноплазменной хирургией, этот метод является самым щадящим современным хирургическим методом.
В течение 12 месяцев после лечения мы будем бесплатно осуществлять наблюдение за состоянием вашего здоровья.
Обратившись к нам, вы навсегда избавитесь от своих проблем! Таким образом, можно сделать вывод: ринит, лечение которого – дело сугубо профильных специалистов, не так безобиден и прост, как кажется!
Установление точного диагноза «ринит», лечение заболевания и наблюдение за пациентами должны осуществлять только квалифицированные врачи! Ведь нередко не вылеченный своевременно насморк переходит в хроническую форму и ведет к серьезным осложнениям.
О клинике
Здоровье, которого вы достойны!
Новейшее оборудование, передовые технологии в диагностике и лечении, индивидуальный подход к каждому пациенту, комфортные условия пребывания и доброжелательная обстановка – это все не про клинику? А вот и нет. Это все о клинике в самом центре Краснодара, ТС клинике.
Сразу объясним название: ТС клиника от английского TS (theraphy and surgery, многопрофильная клиника с круглосуточным стационаром и реанимацией)
Пациент, а не история болезни
Частый вопрос: в чем отличие нашей клиники от множества других, в том числе муниципальных, прошедших модернизацию по государственным программам?
Отвечаем: в муниципальных клиниках, несмотря на все их преимущества, нет пациентов, а есть только истории болезни. Мы работаем для пациентов, используя в своей работе многоуровневый контроль качества оказания медицинской помощи. Персональный подход к каждому пациенту – для нас не модная фраза, а неукоснительное правило. Мы лечим именно пациента, а не симптомы болезни и не результаты его анализов.
Мы работаем для пациентов, используя в своей работе многоуровневый контроль качества оказания медицинской помощи. Персональный подход к каждому пациенту – для нас не модная фраза, а неукоснительное правило. Мы лечим именно пациента, а не симптомы болезни и не результаты его анализов.
По последнему слову техники
Оснащение клиники позволяет проводить самую тщательную диагностику и качественное лечение заболеваний. Оборудования экспертного уровня и высокотехнологичное оснащение — гарантия эффективного лечения наших пациентов.
Итак, давайте заглянем в святая святых, операционную.
ТС клиника оснащена оборудованием фирмы Storz — одним из лидеров в производстве сложнейшего эндоскопического оборудования. Качественной оснащение и высоко квалифицированный персонал позволяет выполнять хирургические вмешательства приемущественно эндоскопически. Во-первых, это меньше травмирует пациента, а это значит, процесс реабилитации проходит легче и комфортнее, что в свою очередь значительно сокращает период нетрудоспособности и позволяет нашим пациентам в кратчайшие сроки, вернуться к привычному ритму жизни, например: вместо недели в стационаре пациент может отправиться домой уже через два-три дня, а в некоторых случаях тем же вечером! Тек же, не стоит сбрасывать со счетов и косметический эффект, а для современного человека это момент немаловажный.
Научная база
Конечно, для каждой клиники самое важное – это достойная команда специалистов. Чтобы соответствовать высокому уровню наши специалисты постоянно проходят обучение и подготовку в ведущих клиниках России. На базе клиники регулярно проводятся конференции по основным направлениям.
Мы гордимся, что на базе ТС клиники проводят мастер-классы ведущие хирурги России, ближнего и дальнего зарубежья.
«Это не что-то уникальное. Это нормальная современная клиника, такая, какой должна быть любая больница для оказания своевременной квалифицированной помощи пациенту». С.Ю. Шумов, гл. врач
С.Ю. Шумов, гл. врач
Коллегиальная работа – современный подход к лечению
Главные направления работы клиники – гинекология, урология, проктология, отоларингология, хирургия по этим направлениям, лечение сопутствующих и сочетанных заболеваний, т.е. совместная работа специалистов. И это тоже своего рода уникальность клиники. Все специалисты работают в связке. Например, урологи занимаются проблемами мочеиспускания, гинекологи – опущением тазового дна. А чтобы эти проблемы решались одновременно, такое встречается крайне редко. Здесь же все проблемы пациентов рассматриваются специалистами комплексно Поскольку зачастую симптомы одного заболевания могут скрываться за другим и только комплексный подход позволяет отдифиринцировать симптоматику и установить правильный диагноз.
Возможности для пациента
Благодаря сотрудничеству с ведущими клиниками России, в самых сложных случаях специалисты ТС клиники в любой момент могут обратиться за советом к коллегам, созвать консилиум и принять коллегиальное решение. Пациенту не нужно ехать в Москву, записываться на приёмы и ждать, когда освободится тот или иной врач. Благодаря нашей программе обследования и совместной работе врачей можно поставить точный диагноз и назначить эффективную схему лечения
От и до
Как уже говорилось, клиника может оказать любую помощь, от консультативной до реабилитационной. Наличие реанимации, оснащенной высокоточным оборудованием позволяет значительно сократить риски раннего послеоперационного периода, при необходимости пациент отправляется в палату реанимации под наблюдение врачей-реаниматологов. Современное физиотерапевтическое отделение с аппаратурой мирового уровня позволяет проводить лечение и реабилитацию пациентов всех отделений.
Здоровье, которого вы достойны – вместе с ТС клиник!
Острый постстрептококковый (постинфекционный) гломерулонефрит | #01/17
Острый иммунокомплексный диффузный пролиферативный гломерулонефрит, часто связанный с инфекционными заболеваниями, называют острым постинфекционным гломерулонефритом. Ведущая роль в развитии острого гломерулонефрита принадлежит стрептококку, что определяет еще одно название этого заболевания — острый постстрептококковый гломерулонефрит. Эта наиболее изученная и распространенная форма острого гломерулонефрита, чаще поражающая детей, является темой данного обзора.
Ведущая роль в развитии острого гломерулонефрита принадлежит стрептококку, что определяет еще одно название этого заболевания — острый постстрептококковый гломерулонефрит. Эта наиболее изученная и распространенная форма острого гломерулонефрита, чаще поражающая детей, является темой данного обзора.
Этиология и эпидемиология острого гломерулонефрита
Острый постстрептококковый гломерулонефрит развивается вследствие перенесенной или на фоне персистирующей стрептококковой инфекции и имеет типичные серологические и морфологические признаки. Его возбудителем чаще является β-гемолитический стрептококк группы А, к наиболее известным нефритогенным штаммам которого относятся М-типы 1, 2, 4, 12, 18, 49, 55, 57 и 60 [1–3].
Типичен очаг стрептококковой инфекции в лимфоидных тканях ротоглотки (небные и глоточные миндалины), нередка первичная локализация стрептококка в коже при импетиго или роже, возможно развитие заболевания после отита, остеомиелита. Риск развития острого постстрептококкового гломерулонефрита после инфицирования стрептококком зависит как от конкретного штамма стрептококка, так и от локализации очага. Так, при инфицировании стрептококком серотипа 49 риск развития гломерулонефрита при кожной инфекции в 5 раз выше, чем при фарингите [4, 5].
В развитых странах Северной Америки и Центральной Европы отмечается снижение частоты острого постстрептококкового гломерулонефрита, где заболевание встречается в основном в виде спорадических случаев. В развивающихся странах Южной Америки, Африки, в Китае и Юго-Восточной Азии наблюдаются случаи групповых заболеваний в бедных районах и эпидемические вспышки в плотно населенных областях. Причиной эпидемий стрептококковой инфекции, приводящей к вспышкам острого гломерулонефрита, все чаще бывают атипичные (мутантные) штаммы β-гемолитического стрептококка группы А, резистентные к пенициллинам, макролидам и тетрациклинам, а также другие стрептококки (возбудитель коровьего мастита Streptococcus zooepidemicus и нефритогенный штамм пиогенного стрептококка — Streptococcus pyogenes M49), способные «ускользать» от иммунного ответа.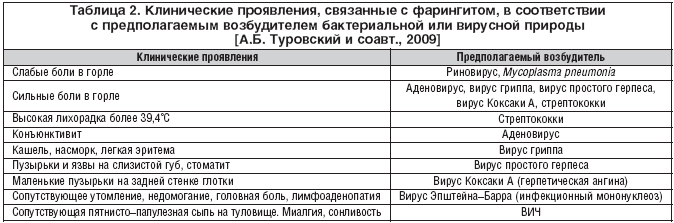 Острый гломерулонефрит, возникший вследствие инфицирования подобными штаммами, как правило, протекает более тяжело и отличается высоким процентом хронизации [6, 7]. Одной из самых известных была эпидемия острого гломерулонефрита, связанная с инфекцией Streptococcus zooepidermicus, отмеченная с декабря 1997 г. по июль 1998 г. в штате Nova Serrana в Бразилии, когда суммарное число заболевших составило 253 человека (от 4,5 до 18,1 на 1000 населения), а источником инфекции стал сыр, приготовленный из молока коров [6].
Острый гломерулонефрит, возникший вследствие инфицирования подобными штаммами, как правило, протекает более тяжело и отличается высоким процентом хронизации [6, 7]. Одной из самых известных была эпидемия острого гломерулонефрита, связанная с инфекцией Streptococcus zooepidermicus, отмеченная с декабря 1997 г. по июль 1998 г. в штате Nova Serrana в Бразилии, когда суммарное число заболевших составило 253 человека (от 4,5 до 18,1 на 1000 населения), а источником инфекции стал сыр, приготовленный из молока коров [6].
Острый постстрептококковый гломерулонефрит значительно чаще встречается у детей, чем у взрослых. Пик заболеваемости приходится на возраст от 2 до 6 лет. Около 5% случаев приходится на возраст младше 2 лет, до 10% — на взрослых старше 40–50 лет, преимущественно мужчин. Мальчики болеют чаще девочек [1, 2, 8]. Острый постстрептококковый гломерулонефрит чаще развивается в зимние месяцы спустя 10–12 дней после перенесенной стрептококковой инфекции (фарингит, ангина, скарлатина), острой инфекции дыхательных путей.
Развитие острого постстрептококкового гломерулонефрита более вероятно при наличии предрасполагающих факторов, таких как отягощенная наследственность в отношении инфекционно-аллергических заболеваний, повышенная семейная восприимчивость к стрептококковой инфекции, наличие у ребенка хронических очагов инфекции, гиповитаминоза, гельминтозов [3, 8]. Провоцирующими факторами развития острого постстрептококкового гломерулонефрита у детей-носителей гемолитического стрептококка могут стать переохлаждение и респираторные вирусные инфекции.
Помимо стрептококка, острый гломерулонефрит может развиваться вследствие других инфекций (бактериальных, вирусных, паразитарных). Среди вирусов наибольшую роль играют вирусы гриппа, кори, краснухи, гепатита А и В. Так, острый гломерулонефрит регистрируется во время эпидемий гриппа и гепатита А. В странах Африки и Азии причиной развития острого гломерулонефрита часто будут паразитарные инфекции (тропическая малярия, шистосомоз) [1, 3, 8].
Провоцировать развитие острого гломерулонефрита могут и неинфекционные факторы, что связано с высокой аллергизацией населения. К таким сенсибилизирующим агентам относятся прежде всего лекарственные препараты (антибиотики, сульфаниламиды), вакцины и сыворотки, пыльца растений, яды насекомых и других животных, пищевые продукты при индивидуальной непереносимости и другие аллергены (табл. 1).
Патогенез и патоморфология
В развитии острого постстрептококкового гломерулонефрита ведущее значение принадлежит образованию в крови растворимых иммунных комплексов. При остром постстрептококковом гломерулонефрите или другом постинфекционном нефрите нет непосредственного поражения почек инфекционным агентом, а заболевание обусловлено иммунопатологической реакцией на возбудитель и его антигены. Именно поэтому при «классическом» течении острого постстрептококкового гломерулонефрита первые признаки заболевания возникают через 1–3 нед после перенесенной ангины, в течение которых происходит сенсибилизация организма к антигенам стрептококка.
Большое значение в развитии острого постстрептококкового гломерулонефрита имеет «нефритогенность» определенных штаммов стрептококка. Нефритогенные штаммы стрептококков вырабатывают белки — эндострептолизины, имеющие выраженное сродство к структурам почечных клубочков. При попадании в циркуляцию эти белки, связываясь с участками клубочков, активируют комплемент и формируют иммунные комплексы, что приводит к повреждению эндотелия капилляров клубочков с развитием экссудативных и пролиферативных процессов, провоцирует активацию системы гемостаза и развитие локального внутрисосудистого свертывания с микротромбозами капилляров клубочков.
Другой механизм реализуется повреждением нейраминидазой стрептококков нормальных молекул IgG, которые, откладываясь в неповрежденных клубочках и связываясь с анти-IgG-антигенами, формируют иммунные комплексы, повреждающие почку [1, 3, 8].
Роль других антигенов и токсинов β-гемолитического стрептококка, таких как мембранные антигены М-типа, эндотоксин D, нефрит-ассоциированный плазминовый рецептор, эритрогенный экзотоксин В, сводится к запуску механизмов пролиферации в почечных клубочках, активации С3-фракции комплемента и ренин-ангиотензин-альдостероновой системы (РААС), что приводит в свою очередь к задержке натрия и воды и почечной вазоконстрикции [1, 2, 9–12].
Острый постстрептококковый гломерулонефрит характеризуется преимущественно субэпителиальным отложением иммунных комплексов с формированием диффузного эндокапиллярного пролиферативного гломерулонефрита, который в своем развитии может проходить несколько стадий: экссудативную, экссудативно-пролиферативную, пролиферативную и фазу остаточных явлений, сменяющих друг друга.
При иммуногистохимическом исследовании в ранние сроки заболевания обнаруживают IgG и С3, которые распределяются диффузно вдоль стенок капилляров в виде мелких гранул.
Патогномоничным признаком острого постстрептококкового гломерулонефрита, выявляемым при электронной микроскопии, будут отложения IgG- и С3-депозитов в виде «горбов» на эпителиальной стороне базальной мембраны капилляров.
Первоначально изменения носят экссудативный характер с набуханием эндотелиальных и мезангиальных клеток и инфильтрацией полиморфноядерными лейкоцитами, выраженность которой зависит от степени иммунокомплексных отложений. В дальнейшем начинают преобладать процессы пролиферации мезангиоцитов и эндотелиоцитов, тогда как количество инфильтрирующих клеток постепенно снижается. Морфологические изменения после перенесенного острого гломерулонефрита могут сохраняться в виде увеличения мезангиального матрикса, неравномерной плотности и неправильного контура гломерулярной базальной мембраны, синехий.
Поражение капилляров клубочков в дебюте острого гломерулонефрита приводит к их полнокровию, стазу, повышению проницаемости и повреждению стенок. Эритроциты проникают в полость капсулы клубочка и канальцев, что обусловливает развитие гематурии различной степени выраженности. При значительном нарушении микроциркуляции может существенно снижаться скорость клубочковой фильтрации (СКФ), что клинически будет проявляться олигурией.
Нарушения почечной гемодинамики и ишемия почек приводят к активации РААС с обратным всасыванием натрия в канальцах нефронов. Этому же способствуют активация тубулогломерулярной обратной связи и нарушение СКФ. Указанные патогенетические механизмы приводят к гипернатриемии, острой гиперволемии и объем-натрий-зависимой гипертензии с перегрузкой объемом левого желудочка миокарда.
Указанные патогенетические механизмы приводят к гипернатриемии, острой гиперволемии и объем-натрий-зависимой гипертензии с перегрузкой объемом левого желудочка миокарда.
В редких случаях развивается выраженная пролиферация париетального эпителия и накопление моноцитов экстракапиллярно. Экстракапиллярная пролиферация (пролиферативные экстракапиллярные полулуния) более чем в 30% клубочков ведет к быстропрогрессирующему острому нефриту с быстрым исходом в нефросклероз с терминальной уремией.
Ренальная острая почечная недостаточность (ОПН) осложняет другие редкие варианты тяжелого острого гломерулонефрита:
- с фибриноидным некрозом почечных артерий при неконтролируемой гипертензии;
- с миоренальным синдромом с рабдомиолизом при рецидивах почечной эклампсии.
Клиническая картина и течение заболевания
Острый постстрептококковый гломерулонефрит обычно манифестирует через 1–3 нед после перенесенной ангины или фарингита либо через 3–6 нед после кожной инфекции. Клинические проявления острого гломерулонефрита могут варьировать от скудных изменений в моче до яркой манифестации в виде остронефритического синдрома с классической триадой симптомов: гематурией, отеками, гипертензией, а также олигурией (табл. 2). При целенаправленном расспросе можно выявить симптомы в виде жажды, слабости, уменьшения количества мочи. По мере развития заболевания присоединяются одышка, сердцебиение, головная боль, тошнота, во многом обусловленные острой гипертензией. Боли в пояснице ощущают 5–10% больных. Боли тупые, симметричные, обусловлены растяжением капсулы почек в результате отека почечной паренхимы.
Гематурия — обязательный признак острого гломерулонефрита. У 2/3 больных обнаруживается микрогематурия, у остальных — макрогематурия. После увеличения диуреза макрогематурия, как правило, исчезает, в то время как микрогематурия может сохраняться в течение многих месяцев после острого периода. Отеки, вследствие задержки натрия и воды при манифестном течении, определяются у 80–90% больных. Преимущественная локализация отеков — лицо. Отеки наиболее выражены утром, днем могут спадать, сменяясь отеком лодыжек. У некоторых больных формируется facies nephritica: отеки лица, бледность кожного покрова, набухание шейных вен. Олигурия развивается в первые дни заболевания, сохраняется обычно в течение 2–3 дней. Анурия не характерна. Длительно сохраняющаяся олигурия может рассматриваться как неблагоприятный прогностический признак.
Преимущественная локализация отеков — лицо. Отеки наиболее выражены утром, днем могут спадать, сменяясь отеком лодыжек. У некоторых больных формируется facies nephritica: отеки лица, бледность кожного покрова, набухание шейных вен. Олигурия развивается в первые дни заболевания, сохраняется обычно в течение 2–3 дней. Анурия не характерна. Длительно сохраняющаяся олигурия может рассматриваться как неблагоприятный прогностический признак.
Артериальная гипертензия развивается более чем у 80% больных, чаще умеренная. В основе ее патогенеза — увеличение объема циркулирующей крови, увеличение ударного объема сердца, повышение сердечного выброса и периферического сосудистого сопротивления. Длительное и стойкое повышение артериального давления (АД) рассматривается как неблагоприятный прогностический признак и может свидетельствовать о развитии застойной сердечной недостаточности или формировании почечной эклампсии.
Протеинурия, отмечающаяся почти всегда, как правило, не достигает высоких цифр и сохраняется в среднем не более 7–10 дней. Умеренная и следовая протеинурия может выявляться дольше.
В общем анализе мочи выявляются цилиндры (гиалиновые, зернистые и эритроцитарные цилиндры), в первые дни заболевания можно обнаружить лейкоциты, представленные в основном сегментоядерными нейтрофилами, эозинофилами и лимфоцитами, отражающими иммунный воспалительный процесс в клубочках.
В общем анализе крови выявляют нейтрофильный лейкоцитоз, возможны эозинофилия, увеличение скорости оседания эритроцитов (СОЭ), анемия. Наблюдается умеренное снижение СКФ при нормальном или повышенном почечном кровотоке. Азотовыделительная функция почек чаще не нарушена либо отмечается небольшое увеличение содержания азотистых продуктов. Характерны диспротеинемия (гипер-α-2- и гипер-γ-глобулинемия), гипокомплементемия.
При серологическом исследовании крови у большинства больных обнаруживают повышенные титры антистрептолизина О, антистрептогиалуронидазы, антистрептокиназы. На первой неделе болезни выявляют циркулирующие иммунные комплексы и снижение концентрации С3-фракции комплемента. В сыворотке крови повышается концентрация IgG, IgM, редко IgA.
На первой неделе болезни выявляют циркулирующие иммунные комплексы и снижение концентрации С3-фракции комплемента. В сыворотке крови повышается концентрация IgG, IgM, редко IgA.
Нарушения в системе свертывания крови проявляются сокращением протромбинового времени, повышением протромбинового индекса, угнетением фибринолитической активности, появлением продуктов деградации фибрина и фибриногена в сыворотке крови и моче.
Остро развившаяся гиперволемия приводит к гипертензии с расширением полостей сердца. При этом расширяются границы относительной тупости сердца, часто обнаруживают тахикардию, реже — брадикардию, ослабление I тона, акцент II тона на аорте. В тяжелых случаях возможно появление ритма галопа. На электрокардиограмме отмечаются низкий вольтаж, удлинение зубца P–Q, двухфазность и уплощение зубца T, иногда смещение интервала ST. Появляется спазм сосудов глазного дна, возможны геморрагии и отек диска зрительного нерва.
В период обратного развития острого нефрита появляется полиурия, исчезают отеки и макрогематурия, нормализуется АД. Примерно через 1,5–2 мес нормализуются показатели мочи и наступает полная клинико-лабораторная ремиссия. Однако полное выздоровление с обратным развитием морфологических изменений в почках наступает через 1–2 года.
Если отдельные клинические симптомы сохраняются более 6 мес, это указывает на затяжное течение острого гломерулонефрита; длительность симптоматики более 1 года расценивают как переход в хронический нефрит. Однако у детей изолированная микрогематурия может сохраняться и более 1 года после перенесенного острого гломерулонефрита без хронизации заболевания [3, 8].
Отличительной особенностью течения современного острого гломерулонефрита является преобладание малосимптомных вариантов, которые встречаются в десятки раз чаще, чем манифестные. Такое атипичное субклиническое течение острого гломерулонефрита характеризуется изолированным мочевым синдромом (в виде гематурии) и отсутствием экстраренальных проявлений, либо они столь незначительны и кратковременны, что проходят незамеченными. «Классический» остронефритический синдром встречается редко.
«Классический» остронефритический синдром встречается редко.
Как правило, субклинические формы острого гломерулонефрита выявляются случайно при лабораторном исследовании либо констатируются постфактум при тщательном изучении анамнеза.
Осложнения острого гломерулонефрита
При тяжелом течении острого нефрита в начальный период возможны угрожающие жизни осложнения:
- почечная эклампсия с отеком мозга;
- острая сердечная недостаточность;
- отек легких;
- острая почечная недостаточность.
Наиболее тяжелое осложнение — эклампсия (ангиоспастическая энцефалопатия), всегда сопровождается повышением АД, обусловлена спазмом сосудов головного мозга и последующим его отеком. Эклампсия проявляется тонико-клоническими судорогами, возникающими после короткого периода предвестников — головной боли, тошноты, рвоты, нарушения зрения. Во время припадка сознание отсутствует, кожный покров и слизистые оболочки становятся цианотичными, дыхание — неровным, хрипящим, появляется пена изо рта, происходит непроизвольное мочеиспускание. Приступ длится несколько минут, иногда наблюдается серия приступов. При отсутствии ургентной адекватной терапии возможен летальный исход от кровоизлияния в головной мозг.
Типичной причиной ОПН являются рентгеноконтрастная нефропатия. Риск этого осложнения при выполнении внутривенной урографии или ангиографии при остром нефрите резко повышен. При остром нефрите высок риск ятрогенных нефропатий — при применении НПВС, нефротоксичных антибиотиков, циклоспорина. При наличии профузной макрогематурии, вызывающей обструкцию мочеточников, описаны случаи развития постренальной ОПН.
Острая сердечно-сосудистая недостаточность у детей возникает редко, характеризуется резким увеличением размеров печени, нарастанием периферических отеков и клинической картиной острой левожелудочковой недостаточности, прогрессирующей в кардиогенный отек легких.
Диагностика и дифференциальный диагноз
Отеки, гематурия и артериальная гипертензия составляют триаду клинических симптомов, служащую основным критерием клинической диагностики острого гломерулонефрита. Трудности в распознавании заболевания возникают при атипичном или стертом течении, когда у ребенка выявляют только микрогематурию и незначительную протеинурию. В этих случаях поставить диагноз помогают данные о недавно перенесенной стрептококковой инфекции, наблюдение за динамикой АД и почечного процесса и результаты дополнительных исследований, включающие определение титра антистрептококковых антител и концентрации компонентов комплемента в сыворотке крови.
Трудности в распознавании заболевания возникают при атипичном или стертом течении, когда у ребенка выявляют только микрогематурию и незначительную протеинурию. В этих случаях поставить диагноз помогают данные о недавно перенесенной стрептококковой инфекции, наблюдение за динамикой АД и почечного процесса и результаты дополнительных исследований, включающие определение титра антистрептококковых антител и концентрации компонентов комплемента в сыворотке крови.
Дифференциальную диагностику следует проводить с урологическими заболеваниями с гематурией (мочекаменная болезнь, нефроптоз, опухоли и туберкулез почек, тромбоз почечных вен), обострением хронического гломерулонефрита, острым пиелонефритом, острым тубулоинтерстициальным нефритом (инфекционным, лекарственным), IgA-нефритом (первичным и вторичным), синдромом Альпорта, болезнью тонких базальных мембран, гемолитико-уремическим синдромом [1, 3, 8].
Для проведения дифференциальной диагностики важно тщательно собрать анамнез, выяснить, не было ли ранее отеков, изменений в анализах мочи, повышенного артериального давления. В пользу обострения хронического нефрита свидетельствуют также снижение концентрационной способности почек, изменения на глазном дне.
Иногда вопрос дифференциальной диагностики решается путем длительного наблюдения за ребенком, а в некоторых случаях при длительно сохраняющейся симптоматике необходимо морфологическое исследование — биопсия почки. Развитие нефротического синдрома или быстропрогрессирующее течение требует исключить другую форму гломерулонефрита, манифестировавшую под маской «острого» [13–15].
Лечение
Лечение больных острым гломерулонефритом проводят в стационаре. В острый период необходимы постельный режим, покой, тепло, способствующие улучшению кровообращения в почках. Расширение режима проводят по мере исчезновения отеков, коррекции гипертензии.
Учитывая связь острого постстрептококкового гломерулонефрита со стрептококковой инфекцией, в дебюте заболевания целесообразно назначать антибиотики из группы пенициллинов (например, защищенные пенициллины), цефалоспорины в течение 10 сут. Антибактериальная терапия показана при развитии острого гломерулонефрита при фарингите, тонзиллите, поражениях кожи, особенно при положительных результатах посевов с зева или при высоких титрах антистрептококковых антител в крови.
Антибактериальная терапия показана при развитии острого гломерулонефрита при фарингите, тонзиллите, поражениях кожи, особенно при положительных результатах посевов с зева или при высоких титрах антистрептококковых антител в крови.
Диета
В острый период болезни, особенно при бурном начале с отеками, олигурией и артериальной гипертензией, необходимо резко ограничить потребление хлорида натрия и воды. В период развития олигурии суточное количество потребляемой жидкости рассчитывается по формуле: диурез за предыдущие сутки + потери на перспирацию (15 мл/(кг × сут) или 400 мл/(м2 × сут)). В дальнейшем количество потребляемой жидкости увеличивается соответственно увеличению диуреза. Бессолевой стол назначается в первую неделю заболевания, а при сохранении олигурии и/или артериальной гипертензии и на более длительный срок. Снижение повышенной концентрации натрия крови — основа патогенетической терапии нефритических отеков и артериальной гипертензии. У большинства больных с нефритическим синдромом понижение концентрации натрия крови, даже при отсутствии другой терапии, приводит к быстрому купированию отечного и гипертензионного синдромов.
После стойкой нормализации АД и диуреза разрешено добавление соли в пищу из расчета 0,5–1,0 г/сут. При благоприятном течении заболевания потребление соли восстанавливается с 4–5 недели из расчета 50 мг/(кг × сут).
Убедительных доказательств положительного влияния малобелковой диеты на течение острого гломерулонефрита не получено. Традиционно принято ограничивать потребление белка из расчета около 1,0 г/кг в сутки. Расширение рациона производится преимущественно за счет растительного белка, потребление белков животного происхождения ограничивается в течение 2–3 нед. Противопоказаны острые блюда и продукты, содержащие экстрактивные вещества и аллергены; следует избегать продуктов, богатых калием. Общая энергетическая ценность пищи должна соответствовать потребностям ребенка.
Лечение отечного синдрома
Диуретическая терапия назначается при выраженных отеках, способствует снижению гиперволемии и угрозы развития осложнений. Назначение гидрохлоротиазида эффективно только при нормальной скорости СКФ. Спиронолактон не применяется из-за риска развития гиперкалиемии. Наиболее часто назначается фуросемид, который эффективен даже при сниженной СКФ. Препарат используется в дозе 1,0–2,0 мг/кг в сутки парентерально в 1–2 приема; при необходимости доза препарата может быть увеличена. Через несколько дней пациент может быть переведен на пероральный прием препарата. При выраженных отеках, признаках левожелудочковой недостаточности с артериальной гипертензией фуросемид назначается в дозе до 4 мг/кг в сутки и более.
Антигипертензивная терапия
Антигипертензивная терапия необходима при гипертензии, не корригируемой режимом и салуретиками. Для лечения используют антагонисты кальция дигидропиридинового ряда: нифедипин (0,25–1 мг/кг в сутки), амлодипин (6–17 лет: 2,5–5 мг/сут), исрадипин, 0,15–0,8 мг/кг в сутки (до 20 мг/сут) и др.; центральные симпатолитики: метилдопа (10 мг/кг в сутки), моксонидин; кардиоселективные β-адреноблокаторы. Ингибиторы ангиотензин-превращающего фермента — эналаприл (0,1–0,5 мг/кг в сутки), каптоприл (0,3–1,5 мг/кг в сутки), лизиноприл (0,07–0,6 мг/кг в сутки) рамиприл, фозиноприл — применяют под контролем за уровнем СКФ и калия крови в сочетании с фуросемидом.
При появлении предвестников почечной эклампсии или отека легких необходим переход на интенсивную инфузионную терапию фуросемидом (до 480 мг в сут) с периферическими вазодилататорами (внутривенно капельно: нитроглицерин или нитропрусид натрия, диазоксид) и альфа-блокаторами (дигидролазин). При отсутствии эффекта с нарастанием гипертензии с энцефалопатией показан перевод в отделение интенсивной терапии с проведением сеансов изолированной ультрафильтрации, гемодиализа или интермиттирующей гемофильтрации. Экстракорпоральное удаление жидкости показано также при развитии критической гипергидратации с угрозой острой левожелудочковой недостаточности.
Экстракорпоральное удаление жидкости показано также при развитии критической гипергидратации с угрозой острой левожелудочковой недостаточности.
Иммуносупрессивная терапия
Иммуносупрессивная терапия показана больным с присоединившимся нефротическим синдромом (сохраняющимся более 2 нед), при снижении СКФ без тенденции к возвращению к норме. Для выбора схемы иммуносупрессии обязательно проведение биопсии почки. При нефротическом синдроме с экстракапиллярной пролиферацией в отдельных клубочках применяется преднизолон внутрь в дозе 1–2 мг/кг в сутки. При быстропрогрессирующем остром нефрите с выявлением экстракапиллярных пролиферативных полулуний более чем в 30% клубочков почечного биоптата применяются внутривенные метилпреднизолоновые «пульсы».
Основные принципы лечения острого постстрептококкового гломерулонефрита представлены в табл. 3.
Профилактика и прогноз
Для предупреждения острого гломерулонефрита необходимы своевременная диагностика и адекватная терапия стрептококковых заболеваний, санация очагов хронической инфекции, рациональное проведение профилактических прививок. При наличии хронического тонзиллита и/или аденоидита необходимы консультация оториноларинголога и решение вопроса о необходимости тонзилло- или аденоэктомии [8].
Диспансерное наблюдение за детьми, перенесшими острый постстрептококковый гломерулонефрит, осуществляется в течение 5 лет, а при сохранении малейших изменений в анализах мочи — до перевода во взрослую сеть.
Прогноз острого постстрептококкового гломерулонефрита у детей достаточно благоприятный. В среднем около 90% детей выздоравливают, у остальных остаточные изменения в моче могут сохраняться длительное время [3, 8]. Прогрессирование острого гломерулонефрита в терминальную хроническую почечную недостаточность у детей отмечается не более чем в 1–2% случаев. Летальный исход регистрируют крайне редко. У ребенка, у которого в течение 1 года после манифестации острого гломерулонефрита сохраняются гипертензия или отеки либо протеинурия выше 1 г/сут, следует исключить хронизацию с помощью стационарного обследования.
У взрослых риск хронизации острого гломерулонефрита с исходом в терминальную хроническую почечную недостаточность почти в 10 раз чаще, чем у детей [2–4, 8].
В настоящее время недостаточно данных о возможности трансформации острого гломерулонефрита в хронический нефрит. Поскольку биопсия почки проводится только при затяжном течении острого гломерулонефрита или развитии нефротического синдрома, в большинстве случаев невозможно судить об эволюции морфологических изменений в клубочках.
Случаи хронизации острого гломерулонефрита регистрируются при инфицировании атипичными штаммами β-гемолитического стрептококка или его другими видами, а также при развитии острого гломерулонефрита вследствие паразитарных инфекций (например, тропической малярии). Эти наблюдения касаются в основном взрослых мужчин, перенесших острый гломерулонефрит в результате эпидемических вспышек. [16, 17].
Литература
- Нефрология. Учебное пособие для послевузовского образования под ред. Е. М. Шилова. М.: ГЭОТАР-Медиа, 2007.
- Острый гломерулонефрит — все ли вопросы решены? От редакции // Клиническая нефрология. 2009. Т. 2. С. 4–9.
- Хасабов Н. Н., Малкоч А. В. Современные представления о гломерулонефритах. В кн.: Нефрология детского возраста (под ред. В. А. Таболина и др.). М.: ИД Медпрактика-М, 2005. С. 306–390.
- Jankauskiene A., Pundziene B., Vitkevic R. Postinfectious glomerulonephritis in children in Lithuania during 1995–2004: prevalence and clinical features //Medicina (Kaunas). 2007. Vol. 43. Suppl 1. P. 16–22.
- Nasr S. H., Markowitz G. S., Stokes M. B. et al. Acute postinfectious glomerulonephritis in the modern era: experience with 86 adults and review of the literature // Medicine (Baltimore). 2008. Vol. 87. № 1. P. 21–32.
- Balter S., Benin A., Pinto S. W. et al. Epidemic nephritis in Nova Serrana, Brazil // Lancet.
 2000. Vol. 355. № 9217. P. 1776–1780.
2000. Vol. 355. № 9217. P. 1776–1780. - Francis A. J., Nimmo G. R., Efstratiou A. et al. Investigation of milk-borne Streptococcus zooepidemicus infection associated with glomerulonephritis in Australia // J. Infect. 1993. Vol. 27. № 3. P. 317–23.
- Папаян А. В., Савенкова Н. Д. Клиническая нефрология. СПб: Сотис, 1997. 712 с.
- Yoshizawa N., Oshima S., Sagel I. et al. Role of a streptococcal antigen in the pathogenesis of acute poststreptococcal glomerulonephritis. Characterization of the antigen and a proposed mechanism for the disease // J. Immunol. 1992. Vol. 148. № 10. P. 3110–3116.
- Viera N., Pedreanez A., Rincon J., Mosquera J. Streptococcal exotoxin B increases interleukin-6, tumor necrosis factor alpha, interleukin-8 and transforming growth factor beta-1 in leukocytes // Pediatr. Nephrol. 2007. Vol. 22. № 9. P. 1273–1281.
- Viera N., Pedreanez A., Rincon J., Mosquera J. Streptococcal zymogen type B induces angiotensin II in mesangial cells and leukocytes //Pediatr. Nephrol. 2009. Vol. 24. № 5. P. 1005–1011.
- Gadau J., Peters H., Kastner C. et al. Mechanisms of tubular volume retention in immune-mediated glomerulonephritis // Kidney Int. 2009. Vol. 75. № 7. P. 699–710.
- Wong W., Morris M. C., Zwi J. Outcome of severe acute post-streptococcal glomerulonephritis in New Zealand children // Pediatr. Nephrol. 2009. Vol. 24. № 5. P. 1021–1026.
- Raff A., Hebert T., Pullman J., Coco M. Crescentic post-streptococcal glomerulonephritis with nephrotic syndrome in the adult: is aggressive therapy warranted? // Clin. Nephrol. 2005. Vol. 63. № 5. P. 375–380.
- El-Husseini A. A., Sheashaa H. A., Sabry A. A. et al. Acute postinfectious crescentic glomerulonephritis: clinicopathologic presentation and risk factors // Int. Urol. Nephrol. 2005. Vol. 37. № 3. P. 603–609.

- Pinto S. W., Sesso R., Vasconcelos E. et al. Follow-up of patients with epidemic poststreptococcal glomerulonephritis // Am. J. Kidney Dis. 2001. Vol. 38. № 2. P. 249–255.
- Sesso R., Pinto S. W. Five-year follow-up of patients with epidemic glomerulonephritis due to Streptococcus zooepidemicus // Nephrol. Dial Transplant. 2005. Vol. 20. № 9. P. 1808–1812.
А. В. Малкоч1, кандидат медицинских наук
А. Ю. Николаев, доктор медицинских наук, профессор
Н. Н. Филатова, кандидат медицинских наук
ФГБОУ ДПО РМАНПО МЗ РФ, Москва
1 Контактная информация: [email protected]
Streptococcus pyogenes, ДНК [реал-тайм ПЦР]
Исследование для выявления возбудителя стрептококковой инфекции (Streptococcus pyogenes), в ходе которого с помощью метода полимеразной цепной реакции в реальном времени определяется генетический материал (ДНК) стрептококка в образце биоматериала.
Синонимы русские
Пиогенный стрептококк, бета-гемолитический стрептококк группы А, БГСА, β-гемолитический стрептококк группы А, β-ГСА [полимеразная цепная реакция в реальном времени, ПЦР в реальном времени].
Синонимы английские
S. pyogenes, Group A streptococcus, GAS, β-hemolytic streptococcus group A, β-hemolytic streptococcus group A.
Метод исследования
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Мазок из зева (ротоглотки), мазок из носоглотки, соскоб урогенитальный.
Общая информация об исследовании
S. pyogenes – это грамположительная бактерия шаровидной формы, являющаяся возбудителем острого фарингита и импетиго, а также спектра более тяжелых деструктивных заболеваний, таких как пневмония, сепсис и септический артрит, синдром токсического шока, целлюлит и некротизирующий фасциит.
Традиционно для подтверждения диагноза «стрептококковая инфекция» применяют бактериологический посев биоматериала на специальные среды. В качестве биоматериала может выступать отделяемое миндалин или носоглотки (при подозрении на острый фарингит), мокрота (при пневмонии). Как правило, результат может быть получен лишь через несколько суток, что связано с промедлением в постановке точного диагноза и назначении специфического лечения. Однако выявлено, что своевременная диагностика и специфическое лечение не только уменьшают продолжительность болезни и интенсивность симптомов, но также снижают риск развития таких осложнений, как паратонзиллярный абсцесс, средний отит, острая ревматическая лихорадка и постстрептококковый гломерулонефрит (при остром фарингите), стрептококковый сепсис (при пневмонии), деструкция сустава и инвалидизация (при септическом артрите). Эмпирическая терапия антибиотиками пенициллинового ряда основана на предпосылке, что S. pyogenes является основным бактериальным возбудителем острого фарингита (5-15 % случаев у взрослых и 20-30 % у детей). Следует отметить, что острый фарингит может быть вызван другими бактериальными или вирусными агентами, при которых назначение такой эмпирической терапии не только не оправдано, но и опасно развитием резистентных штаммов микроорганизмов. Подобные диагностические трудности могут быть преодолены с помощью РТ-ПЦР – полимеразной цепной реакции – этот метод позволяет получить точный результат в более короткие сроки.
В реакции РТ-ПЦР применяются специфические праймеры к фрагменту ДНК S. pyogenes. Такая особенность позволяет выявлять только пиогенный стрептококк, а не родственные ему другие стрептококки – представители нормальной микрофлоры зева (Streptococcus mutans, Streptococcus viridians). По специфичности РТ-ПЦР не уступает бактериологическому посеву и значительно превосходит другие методы идентификации возбудителя (например, экспресс-тест для определения антигена).
Достаточно часто биоматериал на исследование берется уже на фоне лечения заболевания. В результате чувствительность методов диагностики снижается и вероятность получить ложноотрицательный результат выше. В такой ситуации метод РТ-ПЦР обладает некоторым преимуществом перед другими видами диагностики. Это объясняется тем, что для идентификации возбудителя в реакции используется генетический материал возбудителя – как геномная ДНК живого микроорганизма, так и фрагменты ДНК бактерии, подвергшейся лизису. При этом становится возможным выявление не только живых, активно размножающихся микроорганизмов, но и убитых в результате лечения бактерий. В отличие от РТ-ПЦР, обязательным условием для осуществления других методов диагностики (иммуноферментного анализа или бактериологического посева) является наличие живых микроорганизмов. Поэтому, если биоматериал сдается уже на фоне лечения, метод РТ-ПЦР следует предпочесть другим методам диагностики.
В результате чувствительность методов диагностики снижается и вероятность получить ложноотрицательный результат выше. В такой ситуации метод РТ-ПЦР обладает некоторым преимуществом перед другими видами диагностики. Это объясняется тем, что для идентификации возбудителя в реакции используется генетический материал возбудителя – как геномная ДНК живого микроорганизма, так и фрагменты ДНК бактерии, подвергшейся лизису. При этом становится возможным выявление не только живых, активно размножающихся микроорганизмов, но и убитых в результате лечения бактерий. В отличие от РТ-ПЦР, обязательным условием для осуществления других методов диагностики (иммуноферментного анализа или бактериологического посева) является наличие живых микроорганизмов. Поэтому, если биоматериал сдается уже на фоне лечения, метод РТ-ПЦР следует предпочесть другим методам диагностики.
Высокая чувствительность РТ-ПЦР позволяет использовать этот метод при диагностике осложнений острого фарингита: острой ревматической лихорадки и постстрептококкового гломерулонефрита. Осложнения острого фарингита – это аутоиммунные заболевания, при которых S. pyogenes – ассоциированный фарингит является причинным фактором патологического иммунного ответа, но на момент диагностики этих осложнений он уже проходит (самостоятельно или в результате лечения). Поэтому выявить возбудитель при бактериологическом посеве отделяемого миндалин и носоглотки у пациентов с осложнениями острого фарингита удается лишь в небольшом проценте случаев. С другой стороны, доказательство перенесенной S. pyogenes – инфекции является необходимым критерием постановки диагноза, а также значительно облегчает проведение дифференциальной диагностики заболеваний. Метод РТ-ПЦР характеризуется высокой чувствительностью и поэтому может быть использован при диагностике осложнений острого фарингита.
Выявление S. pyogenes в так называемых стерильных средах – это всегда патологический признак. С другой стороны, обнаружение этого микроорганизма в нестерильных средах (мокрота, отделяемое носоглотки) не всегда указывает на наличие заболевания. Выявлено, что около 12-20 % детей школьного возраста и 2,4-3,7 % взрослых людей являются бессимптомными носителями S. pyogenes. В таких случаях трактовку положительного результата исследования следует расценивать с учетом бактериальной нагрузки и в сочетании с некоторыми другими клиническими и лабораторными признаками. Как правило, бессимптомное носительство характеризуется меньшим количеством бактерий по сравнению с активной инфекцией. Поэтому обнаружение высокой бактериальной нагрузки S. pyogenes в мазке из зева у пациента с лихорадкой, болью в горле и болезненным регионарным лимфаденитом подтверждает диагноз «острый стрептококковый фарингит». И, наоборот, обнаружение низкой бактериальной нагрузки этого микроорганизма в мазке из зева при отсутствии жалоб и клинической картины следует расценить как бессимптомное носительство. РТ-ПЦР – это полуколичественный метод, позволяющий косвенно оценить бактериальную нагрузку. Поэтому он оказывается особенно полезным при обследовании «здоровых носителей» стрептококка. Бессимптомное носительство S. pyogenes следует заподозрить у пациента при выявлении стрептококка после адекватного курса антибиотикотерапии, а также у членов семьи пациента с частыми обострениями стрептококкового фарингита.
Выявлено, что около 12-20 % детей школьного возраста и 2,4-3,7 % взрослых людей являются бессимптомными носителями S. pyogenes. В таких случаях трактовку положительного результата исследования следует расценивать с учетом бактериальной нагрузки и в сочетании с некоторыми другими клиническими и лабораторными признаками. Как правило, бессимптомное носительство характеризуется меньшим количеством бактерий по сравнению с активной инфекцией. Поэтому обнаружение высокой бактериальной нагрузки S. pyogenes в мазке из зева у пациента с лихорадкой, болью в горле и болезненным регионарным лимфаденитом подтверждает диагноз «острый стрептококковый фарингит». И, наоборот, обнаружение низкой бактериальной нагрузки этого микроорганизма в мазке из зева при отсутствии жалоб и клинической картины следует расценить как бессимптомное носительство. РТ-ПЦР – это полуколичественный метод, позволяющий косвенно оценить бактериальную нагрузку. Поэтому он оказывается особенно полезным при обследовании «здоровых носителей» стрептококка. Бессимптомное носительство S. pyogenes следует заподозрить у пациента при выявлении стрептококка после адекватного курса антибиотикотерапии, а также у членов семьи пациента с частыми обострениями стрептококкового фарингита.
Для чего используется исследование?
Для диагностики:
- острого фарингита;
- острой ревматической лихорадки и постстрептококкового фарингита у пациентов с указанием на перенесенный эпизод острого фарингита в анамнезе или без него;
- бессимптомного носительства S. pyogenes у пациента с частыми рецидивами фарингита;
- бессимптомного носительства S. pyogenes у членов семьи пациента с частыми рецидивами стрептококкового фарингита;
- внебольничной пневмонии;
- септического артрита.
Когда назначается исследование?
- При симптомах острого фарингита: боль при глотании, отек и эритема слизистой зева, гнойное отделяемое с поверхности миндалин, болезненный регионарный лимфаденит;
- при симптомах острой ревматической лихорадки: мигрирующий полиартрит или артралгия, чувство перебоев в работе сердца, боль в области сердца, немотивированная слабость, кольцевидная эритема и подкожные узелки, а также неврологическая симптоматика в виде хореического гиперкинеза;
- при симптомах постстрептококкового гломерулонефрита: отек (периорбитальной области или генерализованный), макрогематурия, немотивированная слабость, протеинурия менее 3,5 г/сут.
 , артериальная гипертензия;
, артериальная гипертензия; - при обследовании пациента с рецидивирующим фарингитом;
- при обследовании членов семьи пациента с рецидивирующим фарингитом;
- при обследовании членов семьи пациента с частыми рецидивами острого стрептококкового фарингита;
- при наличии такого фактора риска S. pyogenes (ассоциированной пневмонии), как вирус гриппа h2N1;
- при симптомах внебольничной пневмонии: внезапное начало болезни, лихорадка, одышка, боль в грудной клетке, кашель с отхождением гнойной мокроты;
- при наличии факторов риска септического артрита: младенческий и старческий возраст, иммуносупрессивная терапия, соматические заболевания, гемодиализ;
- при симптомах септического артрита: боли в суставе в покое и при движении, эритема кожных покровов над областью сустава, нарушение подвижности в суставе, повышение температуры тела и немотивированная слабость.
Что означают результаты?
Референсные значения: отрицательно.
Причины положительного результата
В отделяемом носоглотки и миндалин:
- острый фарингит;
- острая ревматическая лихорадка;
- постстрептококковый гломерулонефрит.
В мокроте:
- пневмония;
- острый бронхит, бронхит курильщика.
Что может влиять на результат?
- Применение антибактериальных препаратов пенициллинового ряда (амоксиклав, ампициллин), цефалоспоринов (цефиксим, цефтибутен) и макролидов (азитромицин, кларитромицин) до взятия материала на анализ может привести к получению отрицательного результата.
Важные замечания
- Около 12-20 % детей школьного возраста и 2,4-3,7 % взрослых людей являются бессимптомными носителями S. pyogenes.
- Результат исследования следует оценивать вместе с некоторыми другими лабораторными анализами.

Также рекомендуется
Кто назначает исследование?
Врач общей практики, ЛОР, инфекционист, пульмонолог, эпидемиолог, травматолог.
Литература
- Lee JH, Uhl JR, Cockerill FR 3rd, Weaver AL, Orvidas LJ. Real-time PCR vs standard culture detection of group A beta-hemolytic streptococci at various anatomic sites in tonsillectomy patients. Arch Otolaryngol Head Neck Surg. 2008 Nov;134(11):1177-81.
- Uhl JR et al. Comparison of LightCycler PCR, rapid antigen immunoassay, and culture for detection of group Astreptococci from throat swabs. J Clin Microbiol. 2003 Jan;41(1):242-9.
- Chiappini E, Regoli M, Bonsignori F, Sollai S, Parretti A, Galli L, de Martino M. Analysis of different recommendations from international guidelines for the management of acute pharyngitis in adults and children. Clin Ther. 2011 Jan;33(1):48-58.
- Hill HR. Group A streptococcal carrier versus acute infection: the continuing dilemma. Clin Infect Dis. 2010 Feb 15;50(4):491-2.
- García-Arias M, Balsa A, Mola EM. Best Pract Res Clin Rheumatol. Septic arthritis. 2011 Jun;25(3):407-21.
ВИЧ-инфекция. Проявления ВИЧ в полости рта
ВИЧ-инфекция – медленно прогрессирующее заболевание, вызываемое вирусом иммунодефицита человека, который относится к семейству «медленных вирусов». Встраиваясь в ДНК клеток иммунной системы, имеющих рецепторы CD4, вирус приводит к их гибели, в первую очередь Т-лимфоцитов-хелперов. Это делает человека беззащитным перед внешними и внутренними инфекциями.
Выпадает система постоянного иммунного надзора, сдерживающего активацию условно-патогенной микрофлоры. Параллельно в организме могут запускаться и аутоиммунные реакции, при этом чужеродными воспринимаются не только инфицированные, но и здоровые клетки организма. Ослабляется система сдерживания опухолевого роста.
В результате развивается синдром приобретённого иммунного дефицита (СПИД), организм больного теряет возможность защищаться от инфекций и опухолей, возникают вторичные оппортунистические заболевания (вызванные возбудителями, которые не вызывают заболевания у человека с нормальным иммунитетом, но могут быть смертельно опасны для больных с резко сниженным иммунитетом).
Источниками инфекции являются больные люди в любой период болезни или носители вируса. Достаточная концентрация вируса для заражения ВИЧ содержится только в крови, сперме, влагалищном секрете и грудном молоке. Также вирус содержится в слюне, поте, слезах, экскрементах, моче, однако концентрация вируса там значительно меньше.
ВИЧ передается:
· Через половые контакты. Презерватив не является 100% надежным средством защиты от ВИЧ, поскольку размер вируса меньше пор в материале, из которого изготавливаются механические контрацептивы.
· Через контакт кровь-кровь (совместное использование шприцев, игл для введения наркотиков, при использовании общей посуды для приготовления наркотиков и промывания шприца; через нестерильный медицинский инструментарий, при нанесении татуировок, пирсинга нестерильными инструментами, попадании заражённой крови на повреждённую кожу или слизистые, при переливании непроверенной донорской крови, пересадке органов).
· От матери ребёнку (во время беременности, родов либо при кормлении грудью).
ВИЧ не передается:
· Через общую посуду для еды, при пользовании общим туалетом, душем, ванной комнатой, постельным бельем.
- При рукопожатиях и объятиях.
· Через поцелуй (при отсутствии повреждений слизистой полости рта у партнёров).
- Через пот или слезы.
- При кашле и чихании.
· Вирус иммунодефицита очень неустойчив во внешней среде, он способен выжить только в организме человека и погибает во внешней среде. Невозможно заразиться ВИЧ в бассейне, при занятиях спортом, через укус насекомого или общение с животными.
В развитии ВИЧ-инфекции выделяют несколько стадий:
1) Острая ВИЧ-инфекция (от 3 недель до 3 месяцев от момента заражения).
Основные признаки: острый тонзиллит и фарингит (воспаление миндалин и глотки), повышение температуры тела, протекающее с познабливанием и потливостью. Характерны боли в мышцах, суставах, головные боли, увеличение лимфоузлов, печени, селезенки, возможны высыпания на коже как при краснухе или кори. Первичные проявления могут также протекать в виде гриппоподобного варианта либо реакций, где ведущими симптомами являются головная боль, повышение температуры тела и увеличение лимфатических узлов (мононуклеозоподобный синдром).
Характерны боли в мышцах, суставах, головные боли, увеличение лимфоузлов, печени, селезенки, возможны высыпания на коже как при краснухе или кори. Первичные проявления могут также протекать в виде гриппоподобного варианта либо реакций, где ведущими симптомами являются головная боль, повышение температуры тела и увеличение лимфатических узлов (мононуклеозоподобный синдром).
2) Бессимптомная ВИЧ-инфекция (может длиться годами).
В данный период отсутствуют какие-либо симптомы болезни или ее клинические проявления.
3) Синдром генерализованной лимфаденопатии.
Увеличивается не менее 2 лимфоузлов не менее чем в двух разных областях, реакция сохраняется более 3 месяцев. Чаще всего поражаются лимфоузлы, расположенные по задней поверхности кивательной мышцы, над- и подключичные и подмышечные. Более чем в 50 % случаев реагируют подподбородочные, поднижнечелюстные, околоушные группы узлов.
4) СПИД-ассоциированный комплекс. Характеризуется 4 признаками:
− потеря массы тела 10 % и более;
− немотивированные длительные лихорадка и диарея;
− проливной ночной пот;
− синдром хронической усталости.
В данный период проявляются признаки заболевания в полости рта (грибковые, вирусные, бактериальные поражения кожи и слизистых оболочек).
5) Терминальная стадия – собственно СПИД.
Развитие угрожающих жизни инфекций и злокачественных новообразований, имеющих необратимое течение: пневмоцистная пневмония, кишечный криптоспоридиоз, токсоплазмоз мозга, кандидоз пищевода, бронхов, трахеи, легких, внелегочный криптококкоз, гистоплазмоз, атипичные микобактериозы, прогрессирующая энцефалопатия и др.
Некоторые проявления ВИЧ-инфекции в полости рта
Поражения полости рта у лиц, зараженных ВИЧ-инфекцией, относятся к числу первых симптомов заболевания!
Наиболее часто с ВИЧ связаны:
1) Кандидоз (молочница) полости рта.
Кандидоз полости рта встречается у 75 % людей со СПИД-ассо- циированным комплексом и СПИДом. Это грибковое поражения слизистой оболочки полости рта, вызываемое грибами рода Candida. Ощущения у больного могут отсутствовать или появляются жалобы на сухость во рту, ощущение жжения, боли в сосочках языка, чувство стягивания слизистой губ.
Выделяют несколько форм кандидоза:
- Псевдомембранозный (дифтерийный) кандидоз — характеризуется наличием белого или желтоватого налета на ярко-красной слизистой оболочке полости рта. При соскабливании налет снимается, обнажая красные или кровоточащие пятна. В процесс может вовлекаться любой отдел слизистой оболочки полости рта.
- Эритематозный (атрофический) кандидоз — проявляется в виде красного, плоского, едва различимого поражения спинки языка или твердого либо мягкого неба. Цвет пораженной слизистой оболочки варьирует от светло-розового до багряно-красного, налета нет. Больные жалуются на жжение во рту, чаще всего — при приеме соленой или острой пищи и употреблении кислых напитков.
- Хронический гиперпластический кандидоз – наиболее редкая форма. На слизистой появляются белые темно-коричневатые поражения, которые возвышаются над слизистой и не соскабливаются, имеют шероховатую поверхность. Поражения могут быть в виде пятна, полос, колец.
2) Волосатая лейкоплакия — чаще появляется на боковых поверхностях языка, иногда может переходить на всю спинку и даже корень языка. Вызывается вирусом Эпштейна-Барр. Поверхность слизистой оболочки неровная и покрыта разрастаниями, напоминающими волоски, длиной от нескольких миллиметров до 2–3 см. Очаги поражения имеют сморщенную, как бы «гофрированную» поверхность с нечеткими границами. Характерной особенностью разрастаний является плотное прикрепление к слизистой.
3) ВИЧ-гингивит – характеризуется острым и внезапным воспалением дёсен, как правило в переднем участке верхнего и нижнего зубного ряда, сопровождается самопроизвольными кровотечениями.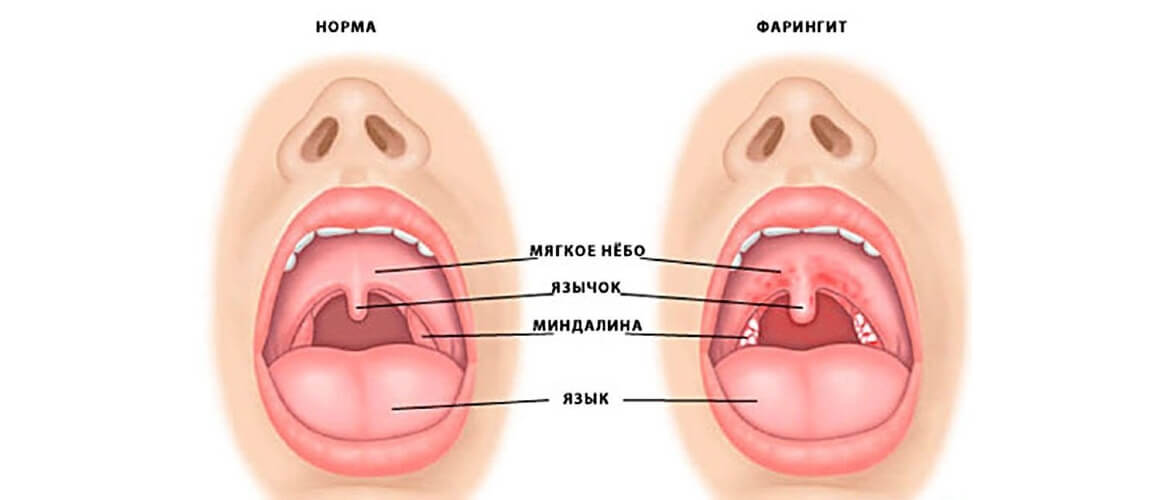 Признаки могут ненадолго исчезать, но затем возникают рецидивы. Воспаление возникает даже при хорошей гигиене полости рта и отсутствии местных факторов риска.
Признаки могут ненадолго исчезать, но затем возникают рецидивы. Воспаление возникает даже при хорошей гигиене полости рта и отсутствии местных факторов риска.
4) ВИЧ-некротизирующий гингивит – начинается внезапно (реже постепенно) с кровоточивости десен при чистке зубов, боли, неприятного запаха изо рта. Десна становится ярко-красной, отечной, краевая десна и межзубные сосочки отмирают, приобретая желто-серый цвет;
5) ВИЧ-периодонтит – любое деструктивное заболевание связочного аппарата зубов с потерей костной ткани, образованием глубоких карманов, подвижностью зубов, но без признаков изъязвления, отмирания тканей. Проводимое лечение как правило не оказывает ощутимого эффекта.
6) Саркома Капоши – злокачественное новообразование, наиболее часто развивающееся у мужчин. Связано с вирусом герпеса человека типа 8. В большинстве случаев сначала поражается кожа, а затем слизистая оболочка полости рта. Кожные поражения у ВИЧ-инфицированных лиц чаще располагаются на туловище, руках, голове и шее. На лице чаще всего поражается кожа носа. В полости рта очаги саркомы преимущественно обнаруживаются на твердом небе и деснах. Начало болезни острое, внезапное. Появляются пятна ярко-красной, багровой, фиолетовой окраски с кровоизлияниями. В более поздних стадиях элементы темнеют, увеличиваются в размерах, могут возвышаться, разделяться на дольки и изъязвляться. Изъязвления в полости рта встречаются более часто, чем на коже. На десне поражения могут проявляться в виде эпулиса (очаг разрастания соединительной ткани на десне).
7) Неходжкинские лимфомы – проявляется образованием плотного, эластичного, красноватого или слабо-фиолетового набухания, которое может изъязвляться. Наиболее частая локализация поражений – десна и слизистая оболочка твердого и мягкого неба.
8) Проявления вирусных инфекций:
- Простой герпес – отмечаются лихорадка, недомогание, увеличение лимфатических узлов.
 Через 1–2 дня появляются пузырьки на любом участке слизистой оболочки полости рта, губах, коже. В полости рта высыпания чаще локализуются на деснах и небе Пузырьки быстро вскрываются с образованием болезненных участков слизистой. Заживление наступает через 10–14 дней. В дальнейшем заболевание может рецидивировать, что провоцируется нахождением на солнце, ОРВИ, травмой, стрессом и ослаблением иммунитета. Отмечается устойчивость к проводимому лечению.
Через 1–2 дня появляются пузырьки на любом участке слизистой оболочки полости рта, губах, коже. В полости рта высыпания чаще локализуются на деснах и небе Пузырьки быстро вскрываются с образованием болезненных участков слизистой. Заживление наступает через 10–14 дней. В дальнейшем заболевание может рецидивировать, что провоцируется нахождением на солнце, ОРВИ, травмой, стрессом и ослаблением иммунитета. Отмечается устойчивость к проводимому лечению. - Опоясывающий герпес – начинается с появления покалывания, зуда, чувства «ползания мурашек», а также болей невралгического характера по ходу ветвей тройничного нерва. Через несколько дней в этой области появляется покраснение с односторонними высыпаниями в виде пузырьков. После их вскрытия образуются эрозии, покрытые сероватым налетом. Заживление наступает через 2–3 недели, но боль может сохраняться в течение нескольких месяцев. Возможно развитие язвенно-некротической формы болезни.
- Папилломавирус человека – образование на коже и слизистой папиллом, бородавок, кондилом. Это узелковые поражения, имеющие четкие границы, возвышающиеся над поверхностью слизистой оболочки и покрытые сосочковыми разрастаниями. Наиболее частая локализация — область губ, десна, твердое небо, язык. Устойчивы к хирургическому лечению.
Диагностика
Необходимы консультации большого количества специалистов, в том числе инфекциониста, иммунолога, онколога, стоматолога и других, в зависимости от специфики течения заболевания.
Группы риска заражения ВИЧ:
· лица, использующие инъекционные наркотические препараты, а также общую посуду, требуемую в приготовлении таких препаратов, сюда же причисляются и половые партнеры таких лиц;
· лица, которые вне зависимости от актуальной для них ориентации, практикуют любые незащищенные половые контакты;
· лица, которым была проведена процедура переливания донорской крови без ее предварительной проверки;
- врачи различного профиля;
- лица, больные тем или иным венерическим заболеванием;
· лица, непосредственным образом задействованные в сфере проституции, а также лица, пользующиеся их услугами.
Разнообразные клинические проявления ВИЧ-инфекции имеют общие особенности – упорное течение и устойчивость к терапии.
Должны насторожить:
· указание на недавно перенесенное острое заболевание с гриппоподобным или мононуклеозоподобным (похожим на симптомы инфекционного мононуклеоза: лихорадка, поражения носоглотки в виде синусита, ангины или фарингита, увеличение более двух групп лимфоузлов, увеличение печени, селезенки, специфические изменения показателей крови) синдромом вне эпидемии;
· продолжительная лихорадка с неясной причиной;
· увеличение лимфоузлов разных групп;
· нарастающее похудание;
· упорная диарея;
· тяжелые пневмонии;
· затяжные гнойно-воспалительные заболевания;
· волосатая лейкоплакия;
· саркома Капоши в молодом возрасте.
Лабораторные тесты:
Иммуноферментный анализ (ИФА, ELISA)
ИФА-положительный результат требует обязательной проверки с использованием другой серии тест-систем. При получении повторного ИФА-положительного результата необходимо подтверждение методом иммуноблотинга (определение антител к отдельным антигенам вируса).
Для того, чтобы пациента признали ВИЧ-инфицированным, у него должны быть получены дважды положительные результаты ИФА, подтвержденные положительным результатом иммуноблотинга.
Следует помнить, что в течение достаточно длительного времени (в среднем до 3, а иногда до 6 месяцев и более) ВИЧ-инфицированные лица остаются серонегативными (то есть результаты анализов в этот период будут отрицательными). Антигенные маркеры ВИЧ обнаруживаются в крови значительно раньше, чем антитела (до 8 недель).
Информативной может быть полимеразная цепная реакция (ПЦР), позволяющая выявить генетический материал вируса в крови.
Стадию заболевания, тактику лечения и прогноз также можно определить по уровню CD4+ Т-лимфоцитов и соотношению CD4+/CD8+.
Профилактика
· Необходимо избегать случайных половых партнеров. При любых таких сексуальных контактах нужно использовать механические средства контрацепции;
При любых таких сексуальных контактах нужно использовать механические средства контрацепции;
· Отказ от приема наркотиков. Человек под действием психоактивных веществ теряет способность критически мыслить, и может, в частности, допустить использование одного шприца среди целой группы наркоманов, где может оказаться ВИЧ-положительный;
· Для предотвращения передачи инфекции от матери к ребенку, следует соблюдать предписания лечащего врача, планировать беременность и приходить на контрольные осмотры. Лечебные мероприятия входят в план подготовки ВИЧ-инфицированной беременной к родам и последующему уходу за ребёнком. В частности, понадобится отказ от грудного вскармливания.
· Периодически необходимо проходить лабораторное обследование на ВИЧ, особенно лицам в группах риска. Если же инфекция обнаружена, нужно сразу же приступить к своевременному, адекватному лечению, назначенному врачом. Чем раньше начато лечение, тем лучше прогноз и больше вероятность предотвратить тяжёлые последствия действия вируса на организм и развитие СПИД.
Врач-интерн Веремейчик Д.В.
Случай 30: Боль в горле — AMBOSS
Последнее обновление: 3 февраля 2021 г.
Инструкции для экзаменуемых
Сценарий открытия
Алекс Сото, 19-летний мужчина, обратился в клинику неотложной помощи из-за боли в горле.
Знаки жизнедеятельности
- Температура: 102 ° F (38,9 ° C)
- Артериальное давление: 122/74 мм рт.
- ЧСС: 70 / мин
- Дыхание: 15 / мин.
Изучить задачи
- Возьмите целенаправленную историю.
- Выполните соответствующее медицинское обследование (не выполняйте рефлекс роговицы, обследования груди, таза / мочеполовой системы или ректального обследования).
- Объяснить пациенту предварительный дифференциальный диагноз и план первичного обследования.
- Напишите записи о пациенте после выхода из палаты.
Встреча с пациентом
Инструкции для пациента
- Говорите хриплым голосом.

- Когда испытуемый нащупывает лимфатические узлы у вас на шее, скажите, что он болит.
- Когда испытуемый давит вам на живот, скажите, что у вас немного болит весь живот.
- Вы не осведомлены о значениях медицинских терминов (например, ларингоскопия) и просите разъяснений, если испытуемый их использует.
- Используйте приведенные ниже контрольные списки для изучения анамнеза, физического осмотра, а также навыков общения и межличностного общения.
Задание: Когда испытуемый упоминает, что он / она хотел бы провести несколько тестов, скажите: «Не могли бы вы просто дать мне несколько антибиотиков? Я очень хочу убраться отсюда.”
Сфокусированная история
При наведении курсора на пузыри речи в списках ниже можно получить дополнительную информацию о соседнем термине. Однако нажатие на ссылки приведет к тому, что вы уйдете от текущего дела, и в этот момент ваш прогресс (то есть ваши галочки) будет утерян. Если вам действительно нужна дополнительная информация по теме, либо откройте ссылку в новой вкладке, либо подождите, пока вы и ваш партнер не завершите рассмотрение дела и не поставите галочки. Переход по ссылке на форму записи пациента не прервет ваш прогресс.
- Основная жалоба
- У меня очень болит горло.
- Расположение
- Это в основном задняя часть моего горла.
- Интенсивность (по шкале от 0 до 10)
- Я бы сказал, по крайней мере, 7, может быть, 8.
- Качество
- Это почти жгучая боль.
- Начало
- Началось прошлой ночью.
- Осадки
- Нет.
- Прогресс / постоянный / прерывистый
- Мне кажется, становится хуже.
- Предыдущие серии
- Может быть, в детстве. Но ничего в последнее время.
- Радиация
- №
- Облегчающие факторы
- Холодные напитки действительно помогают.
- Отягощающие факторы
- Больше болит при глотании.
- Сопутствующие симптомы
- Я тоже сегодня утром проснулся с очень хриплым голосом.

- Предыдущие серии с хриплым голосом
- №
- Проблемы с глотанием пищи
- Да, действительно больно есть или глотать, поэтому со вчерашнего дня я толком ничего не ел.
- Способен глотать жидкости
- Нет, у меня нет проблем с жидкостями, но это действительно больно.
- Головная боль
- №
- Тошнота / рвота
- Да, мое горло так распухло, что меня действительно немного тошнит, когда я говорю. Но меня не вырвало.
- Лихорадка / озноб
- Думаю, да. Вчера вечером у меня определенно был озноб. Когда я приехал, медсестра не измерила мне температуру?
- Усталость
- Да, вчера и сегодня весь день устал.
- Сыпь / изменения кожи
- №
- Кашель
- №
- Одышка
- №
- Аппетит
- У меня сейчас нет особого аппетита.
- Изменение веса
- №
- Недавние инфекции
- Я простудился 2 недели назад.
- Насморк
- №
- Увеличение лимфатических узлов
- Нет, не то чтобы я заметил.
- Голос меняется
- Ну я правда охрип.
- Галитоз
- Хм, не уверен, но у меня какой-то неприятный привкус во рту, и я чувствую, что он пахнет.
- Боль в животе
- У меня сегодня весь день немного болит живот. Но это очень мягко.
Важно узнать о симптомах простуды (ринита и / или головной боли) у пациентов с болью в горле, поскольку они типичны для вирусного тонзиллита, но не ожидаются при стрептококковом фарингите.
- История болезни
- Нет.
- Аллергия
- Нет.
- Лекарства
- Нет.
- Госпитализация
- Никогда.
- Больные контакты
- Моя девушка говорит, что последние пару недель у нее тоже болело горло.
- История хирургических операций
- Нет.
- Семейный анамнез
- У моего папы диабет.

- Работа
- Я учусь в колледже, специализируюсь в области уголовного правосудия, но в основном меня интересует игра в футбол за команду колледжа.
- Дом
- Я живу в общежитии на территории кампуса.
- Алкоголь
- Я пью 1–2 стакана пива по выходным. В течение недели у меня всегда есть футбольные тренировки, поэтому у меня нет времени выходить на улицу или пить.
- Рекреационные наркотики
- №
- Табак
- Никогда.
- Упражнение
- Футбольные тренировки практически каждый день.
- Ведет половую жизнь
- Да.
- С кем
- Ну вот уже 2 месяца моя подруга.А до этого в кампусе было несколько разных девушек.
- Мужчины или женщины
- Что это за вопрос? Только женщины.
- Количество партнеров за последний год
- Чувак, вы задаете довольно много вопросов по этому поводу. Может, 9? 10?
- Защита
- Да, я всегда пользуюсь презервативом. Меньше всего мне нужно, чтобы одна из этих девушек забеременела.
Получение целенаправленного сексуального анамнеза важно для пациентов с болью в горле.Незащищенный секс является фактором риска заражения ВИЧ, а острая ВИЧ-инфекция может проявляться болью в горле (синдром, подобный мононуклеозу).
Целенаправленный медицинский осмотр
Коммуникация и навыки межличностного общения
Взаимодействие с пациентом
- Обследуемый постучал в дверь.
- Examinee представился и назвал свою роль.
- Обследуемый правильно использовал имя пациента.
- Испытуемый задавал открытые вопросы.
- Обследуемый внимательно слушал (не перебивал пациента).
- Обследуемый проявил интерес к пациенту как к личности (т. Е. Проявил заботу и уважение).
- Обследуемый продемонстрировал способность поддерживать эмоции пациента (т. Е. Предлагал слова поддержки, просил разъяснений).
- Обследуемый не повторял болезненных маневров при медосмотре.
- Обследуемый обсудил с пациентом первоначальные диагностические впечатления.
- Examinee объяснил план управления.
- Экзаменуемый использовал немедицинские термины и объяснил причины запланированных шагов в управлении.
- Обследуемый оценил согласие пациента со следующими этапами диагностики.
- Испытуемый спросил о проблемах или вопросах.
Консультации и вызов
Предлагаемый ответ на вызов: «Mr. Сото, я понимаю, что ты плохо себя чувствуешь и хотел бы как можно скорее вернуться домой. Однако в настоящее время я не могу с уверенностью сказать, вызваны ли ваши симптомы бактериальной или вирусной инфекцией.Антибиотики подойдут только в том случае, если симптомы вызывают бактерии, иначе они могут принести больше вреда, чем пользы, или даже вызвать сыпь. Я хотел бы провести несколько тестов, чтобы выяснить точную причину ваших симптомов, а затем обсудить с вами подходящее лечение. Звучит нормально?
Примечание пациента
Дальнейшее обсуждение
Дифференциальные диагнозы
- Стрептококковый тонзиллофарингит: внезапно возникшая ангина, болезненная шейная лимфаденопатия, лихорадка, отсутствие кашля или других симптомов простуды у этого пациента соответствуют критериям микробиологического тестирования на стрептококковый фарингит группы А.Хотя экссудаты миндалин часто обнаруживаются при стрептококковом тонзиллофарингите, они не всегда присутствуют, и небные петехии, наблюдаемые у этого пациента, также являются типичным признаком стрептококковой ангины. Если он окажется положительным, его следует лечить антибиотиками, чтобы предотвратить ревматизм и постстрептококковый гломерулонефрит.
- Инфекционный мононуклеоз (ИМ): ИМ может проявляться аналогично бактериальному фарингиту (например, боль в горле, лимфаденопатия, лихорадка, усталость) и часто встречается у молодых людей.В данном случае это вызывает особую озабоченность из-за легкой боли в животе пациента, которая может указывать на спленомегалию, частую находку при IM. Поскольку спленомегалия может привести к опасному для жизни разрыву селезенки, а этот пациент является заядлым футболистом, ему следует отговаривать играть до тех пор, пока его IM не утихнет. Однако, поскольку у него нет генерализованной лимфаденопатии или серовато-белых отложений на миндалинах, которые обычно наблюдаются при в / м, это лишь второй наиболее вероятный диагноз.
- Вирусный фарингит: вирусный фарингит также может быть причиной боли в горле и покраснения ротоглотки у этого пациента.Однако его лихорадка и отсутствие симптомов простуды делают этот диагноз менее вероятным, чем первые два.
Диагностические исследования
Другие дифференциальные диагнозы, которые необходимо учитывать
Список литературы
Фарингит | патология | Britannica
Фарингит , воспалительное заболевание слизистых оболочек и нижележащих структур глотки (глотки). Воспаление обычно затрагивает носоглотку, язычок, мягкое небо и миндалины.Заболевание может быть вызвано бактериями, вирусами, микоплазмами, грибами и паразитами, а также признанными заболеваниями с неопределенными причинами. Заражение бактериями Streptococcus может быть осложнением, возникающим при простуде. Симптомы стрептококкового фарингита (обычно известного как стрептококковая ангина) — это обычно покраснение и отек горла, гнойничковая жидкость на миндалинах или выделения изо рта, сильная боль в горле, которая ощущается во время глотания, отек лимфатических узлов и легкое высокая температура; иногда у детей бывают боли в животе, тошнота, головная боль, раздражительность.Диагноз устанавливается на основании подробного анамнеза и медицинского осмотра; причину воспаления глотки можно определить посевом из зева. Обычно лечить можно только симптомы — леденцы от горла, чтобы контролировать боль в горле, и ацетаминофен или аспирин, чтобы контролировать лихорадку. Если диагноз стрептококковой инфекции установлен посевом, назначается соответствующая антибактериальная терапия, обычно пенициллином. Примерно через три дня лихорадка уходит; другие симптомы могут сохраняться еще два-три дня.
Британская викторина
44 вопроса из самых популярных викторин «Британника» о здоровье и медицине
Что вы знаете об анатомии человека? Как насчет медицинских условий? Мозг? Вам нужно много знать, чтобы ответить на 44 самых сложных вопроса из самых популярных викторин Britannica о здоровье и медицине.
Встречаются также инфекции вирусного фарингита. Они могут вызывать образование беловато-желтых очагов в глотке, окруженных покрасневшей тканью. Они вызывают жар, головную боль и боль в горле, которые продолжаются от 4 до 14 дней. Также может поражаться лимфатическая ткань глотки.
Ряд других инфекционных заболеваний может вызывать фарингит, включая туберкулез, сифилис, дифтерию и менингит.
Бактериальный фарингит Артикул
Непрерывное образование
Фарингит, чаще описываемый как боль в горле, представляет собой воспаление или раздражение задней части ротоглотки.Хотя большинство случаев возникает по неинфекционным или небактериальным причинам, бактерии несут ответственность за значительную часть инфекций глотки, и эти инфекции проявляются по-разному, имеют разные осложнения и требуют другого лечения. В этой статье рассматривается оценка и лечение бактериального фарингита, включая то, как оценить вероятность бактериальных причин в целом и когда рассматривать более редкие бактерии и более серьезные осложнения. В статье описывается тема для аудитории передовых и специализированных поставщиков и межпрофессиональных групп, чтобы прояснить как болезнь, так и роли отдельных членов команды в оценке и лечении этого состояния.
Цели:
- Определите этиологию бактериального фарингита, сопутствующих состояний и неотложных состояний.
- Обобщите соответствующую оценку бактериального фарингита.
- Просмотрите доступные варианты лечения бактериального фарингита.
- Обсудить стратегии межпрофессиональной группы по улучшению координации помощи и коммуникации для продвижения бактериального фарингита и улучшения результатов.
Введение
Фарингит, чаще описываемый как боль в горле, представляет собой воспаление или раздражение задней части ротоглотки. Хотя большинство случаев возникает по неинфекционным или небактериальным причинам, бактерии несут ответственность за значительную часть инфекций глотки, и эти инфекции проявляются по-разному, имеют разные осложнения и требуют другого лечения. [1] Эффективное определение бактериального фарингита и знание того, когда проводить оценку его более атипичных причин, является важным навыком для любого медицинского работника первичного звена или специалиста, позволяющего избежать как ненужного лечения, так и заболеваемости, связанной с пропущенными или неправильно пролеченными инфекциями.[2]
Этиология
Острый фарингит довольно часто встречается как у детей, так и у взрослых, обычно возникает из-за неинфекционных (например, сезонная аллергия и кислотный рефлюкс) или небактериальных (например, вирусных) причин. [1] Однако, если причина бактериальная, фарингит чаще всего вызывается бета-гемолитическим стрептококком группы A (GABHS), обычно называемым стрептококком [3]. БГСА передается воздушно-капельным путем или через рот и связан с острыми и отсроченными осложнениями, которые будут описаны позже в статье.
Другие бактерии также могут вызывать фарингит, включая стрептококки групп C и G, но из-за сложности отличить колонизацию от инфекции трудно количественно оценить относительную частоту этих бактериальных причин [4]. Инфекции, передаваемые половым путем, такие как Neisseria gonorrhea и Chlamydia trachomatis , следует рассматривать при наличии факторов риска, хотя обычно они протекают бессимптомно. [5] Более редкие инфекции, такие как Yersinia pestis и Corynebacterium diphtheriae , могут рассматриваться, если есть подозрения, что они недавно попали в эндемичные районы.[6] [7]
Эпидемиология
Боль в горле — чрезвычайно распространенная жалоба в офисах поставщиков медицинских услуг, отделениях неотложной помощи и центрах неотложной помощи. [8] Жалоба особенно распространена среди педиатрических пациентов, на которые приходится около половины всех случаев. Среди взрослых бактериальный фарингит с возрастом встречается реже, чаще всего у пациентов младше 40 лет. [9] [10] Среди бактериальных причин преобладают стрептококковые инфекции группы А, опять же чаще среди детей, которые также с большей вероятностью страдают от острых и отсроченных осложнений стрептококковых инфекций.[4] [11]
Другие бактериальные причины боли в горле встречаются реже, но тесно связаны с факторами риска. Хотя гонорея и хламидиоз часто протекают бессимптомно, глоточные ИППП присутствуют почти у 10% людей с некоторыми факторами риска [5]. Кроме того, случаи дифтерии ограничиваются невакцинированным населением или регионами мира, где болезнь остается эндемической [7].
Патофизиология
При бактериальном фарингите бактерии напрямую проникают в ткани слизистой оболочки глотки.Внеклеточные факторы, такие как протеазы, способствуют проникновению в ткани и вызывают воспаление, которое вызывает отек, экссудат, лихорадку и боль при глотании. [12] [13] Воспаление может также способствовать появлению симптомов отита и синусита, поскольку оно проявляется в более широком смысле, даже если эти области не были инфицированы теми же бактериями.
Streptococcus специфически экспрессирует капсулу гиалуроновой кислоты, которая соответствует ткани хозяина и предотвращает типичный иммунный ответ, что делает лечение особенно зависимым от антибиотиков.[14] Хотя нелеченные бактериальные инфекции могут проникать глубже, приводя к более серьезным инфекциям, таким как целлюлит, абсцесс или бактериемия, это гораздо менее вероятно, чем до обычного антибактериального лечения.
Некоторые бактерии продуцируют экзотоксины, которые могут усилить локальное разрушение тканей или вызвать серьезные системные симптомы. Местный экзотоксин может вызвать патогномоничную псевдомембрану дифтерии, а системные токсины могут вызвать скарлатину и редкий синдром токсического шока, связанный со стрептококком.[15] [16]
Вероятно, из-за молекулярного сходства между стрептококком и тканями хозяина существует дополнительный риск неинфекционных осложнений этого фарингита. Ревматическая лихорадка и гломерулонефрит могут быть следствием стрептококковой инфекции, вероятно, в результате молекулярной мимикрии и многофакторных аутоиммунных реакций соответственно [15].
История и физические данные
Как и в случае с большинством заболеваний, диагностика и лечение бактериального фарингита зависят от сбора эффективного анамнеза и проведения целенаправленного медицинского осмотра.Бактериальный фарингит чаще всего возникает остро в начале с относительно изолированной тяжелой болью в горле, потенциально с сопутствующими симптомами, такими как скарлатинообразная сыпь или боль в животе. [3] [4] Провайдеры должны собирать информацию о связанных симптомах, течении, предыдущей истории и факторах риска. Дополнительные симптомы со стороны верхних дыхательных путей, такие как заложенность носа, кашель и раздражение глаз, предполагают вирусные инфекции или сезонную аллергию как более вероятную этиологию. [2] Сезонно повторяющиеся или постоянные симптомы без лихорадки способствуют развитию аллергической этиологии.Кислотный рефлюкс в анамнезе, позиционное обострение и связь с недавней раздражающей пищей, кофеином или алкоголем способствуют развитию гастроэзофагеальной рефлюксной болезни. Факторы риска, такие как сексуальное поведение высокого риска или близкие родственники, страдающие стрептококковой ангиной, могут снизить планку потенциального тестирования.
Соответствующий медицинский осмотр должен включать оценку жизненно важных функций на предмет лихорадки и доказательств клинической нестабильности, оценку ушей, конъюнктивы и ноздрей на предмет наличия описанных симптомов или альтернативных объяснений потенциальной лихорадки.При обследовании ротоглотки и шеи необходимо выявить отек и экссудат миндалин и глотки, а также лимфаденопатию. Экссудаты или псевдомембрана благоприятствуют бактериальной этиологии, так же как и опухшие и болезненные лимфатические узлы. Более диффузный отек конъюнктивы, носовых раковин и глотки, особенно связанный с постназальным выделением жидкости, способствует небактериальной этиологии [17]. Осмотр кожи уместен, особенно у детей, для выявления красной, наждачной бумаги сыпи при скарлатине или признаков других экзантем, которые могут указывать на альтернативную инфекцию.
Оценка
Диагноз бактериального фарингита следует ставить не только на основании результатов клинического обследования, а, скорее, на основе комбинации объективного клинического обследования, ведущего к соответствующим лабораторным исследованиям. [2] [17] Доступно несколько инструментов, помогающих избавиться от субъективности при клиническом обследовании, и для подтверждения клинических показаний были разработаны различные лабораторные тесты и тесты на месте.
Первым из клинических инструментов был разработан критерий Centor, целью которого является оценка вероятности стрептококковой инфекции.Эти критерии включают экссудат миндалин, лихорадку более 100,4 F (38 C), болезненную переднюю шейную лимфаденопатию и отсутствие кашля. Пациенты с ограниченными критериями Центора (0-1) вряд ли будут иметь стрептококковую инфекцию, и в тестировании нет необходимости. Пациенты со многими критериями (3-4) с большей вероятностью будут иметь инфекцию и нуждаются в медицинском обследовании или лабораторном обследовании. [18] Критерии McIsaac изменяют исходные критерии Центра для учета возрастных различий, добавляя балл для пациентов в возрасте от 3 до 14 лет и вычитая балл для пациентов 45 лет и старше.[18] Критерии FeverPAIN включают лихорадку, экссудат миндалин, тяжелое воспаление, начало которого наступает в течение трех дней, а также отсутствие кашля или насморка. Опять же, пациенты с ограниченными критериями (0–1) вряд ли будут иметь стрептококковые инфекции, а пациенты с множеством критериев (4 или более) более вероятны [19].
Быстрый тест на обнаружение антигена (RADT) — это тест на месте оказания медицинской помощи, используемый для проверки на стрептококк у тех пациентов, чьи инфекции нельзя с уверенностью отнести к другим причинам. Его специфичность составляет около 95%, поэтому положительный результат RADT не требует дальнейшего тестирования.Однако его чувствительность составляет от 70 до 90%, поэтому у пациентов со многими признаками бактериальной инфекции отрицательный RADT должен быть подтвержден традиционным посевом из горла. [20]
Бактериальный посев из горла — золотой стандарт диагностики стрептококковой инфекции. К сожалению, результаты доступны не раньше, чем через день или два. Это особенно проблематично для пациентов, за которыми труднее наблюдать, например, пациентов отделения неотложной помощи или пациентов с нестабильной контактной информацией.
Тест амплификации нуклеиновой кислоты (NAAT) для Neisseria gonorrhea и Chlamydia trachomatis можно использовать для тестирования на инфекции глотки. Хотя он не одобрен FDA, CDC одобряет его использование для соответствующего скрининга или диагностики, поскольку он более чувствителен, чем традиционные культуры. Хотя глоточная гонорея и хламидиоз вряд ли вызовут симптомы, мазок NAAT может быть уместен у пациентов с высоким риском или в тех случаях, когда ангина не поддается должным образом стандартному лечению.[21]
Анализы крови, такие как количество лейкоцитов и С-реактивный белок, также могут быть выполнены для оценки клинической стабильности пациента или риска системного заболевания. Тестирование на антистрептококковые антитела не поможет диагностировать острые инфекции, поскольку они не обнаруживаются сразу и не являются устойчивыми [22].
Визуализация подходит только в обстоятельствах, когда пациент демонстрирует нестабильность, соответствующую абсцессу или другой тяжелой этиологии боли в горле, и в этом случае пациента следует перевести в отделение неотложной помощи или в стационар.[23]
Даже те, кто соответствует всем критериям инструментов клинической оценки, имеют только 50-65% шанс заболеть стрептококковой инфекцией. Из-за этого Американское общество инфекционных заболеваний рекомендует не полагаться только на клиническую оценку при выборе лечения. В то время как предыдущие рекомендации одобряли использование эмпирических антибиотиков для пациентов с высокими показателями, самые последние рекомендации, отмечая повышенную распространенность и точность тестирования в местах оказания помощи и потенциально ограниченную заболеваемость нелеченными инфекциями, рекомендуют подтверждать инфекции до лечения.[2] Эта рекомендация не является общепринятой, но может служить для сдерживания агрессивного использования антибиотиков без тестирования.
Лечение / менеджмент
Бактериальный фарингит следует лечить соответствующими антибиотиками после подтверждения инфекции. Симптомы любого фарингита следует дополнительно лечить нестероидными противовоспалительными препаратами или ацетаминофеном для жаропонижающего и обезболивающего.
Для GABHS антибиотиками первой линии являются пенициллины, потому что они недороги и эффективны, и не было обнаружено значительной устойчивости к антибиотикам.Типичны пенициллин V и амоксициллин. Цефалоспорины также подходят пациентам с легкой аллергией на пенициллин или когда пенициллин недоступен. Во избежание развития резистентности рекомендуется лечение цефалоспорином самого узкого спектра действия. Пациентам с более тяжелой аллергией на пенициллин может быть целесообразным лечение азитромицином, но устойчивость к макролидам растет. Наконец, когда известна устойчивость к азитромицину, клиндамицин можно использовать для лечения людей с тяжелой аллергией на пенициллин, хотя он также сталкивается с резистентностью и имеет более высокие показатели непереносимости из-за вкуса, побочных эффектов со стороны кишечника и возможных оппортунистических бактериальных инфекций, таких как Clostridium difficile.[2] [3]
Случаи глоточной гонореи или хламидиоза следует лечить так же, как и инфекции половых органов, обычно при одновременном лечении гонореи и хламидиоза назначают 250 мг цефтриаксона внутримышечно и 1000 мг азитромицина перорально. [21]
О случаях дифтерии следует сообщать в CDC, и их лучше всего лечить антибиотиками (эритромицин или пенициллин) и антитоксином (доступны через CDC). Пациентов следует поместить на респираторные капельки и изолировать контакт до тех пор, пока две последовательные культуры, взятые с интервалом в 24 часа, не станут отрицательными.[24]
Случаев Yersinia pestis следует лечить соответствующими антибиотиками (в первую очередь, аминогликозидами или тетрациклинами), а пациентам следует назначать меры предосторожности в отношении респираторных капель до тех пор, пока посевы не станут отрицательными и антибиотики не будут введены в течение не менее 48 часов.
Местные инфекционные осложнения острых фарингитов, такие как перитонзиллярный абсцесс, следует лечить в условиях больницы, где вмешательства могут проводиться при соответствующей хирургической и специальной поддержке, например, при наличии возможности быстрой интубации, если дыхательные пути пациента нарушены.[23]
Дифференциальная диагностика
Как уже отмечалось, большинство случаев острого бактериального фарингита являются неинфекционными или небактериальными. При рассмотрении возможности бактериального фарингита медработники также должны учитывать:
- Аллергическая реакция на факторы окружающей среды, такие как пыльца, загрязнители в помещении или на открытом воздухе или лекарства
- Раздражающий фарингит, вызванный гастроэзофагеальным рефлюксом или курением
- Травматический фарингит, вызванный чрезмерным криком, храпом или недавней интубацией трахеи
- Афтозные язвы
- Вирусный фарингит, вызванный распространенными вирусными патогенами верхних дыхательных путей, такими как адено-, рино- или коронавирус
- Вирусный фарингит, вызванный более серьезными патогенами, такими как инфекционный мононуклеоз, пандемический коронавирус или ВИЧ
- Грибковые инфекции, такие как кандидоз пищевода
- Бактериальные осложнения, такие как лимфангит, перитонзиллярный или заглоточный абсцесс
Прогноз
Большинство случаев острого бактериального фарингита проходят самостоятельно.Если инфекция БГСА подтверждена и проводится лечение соответствующим антибиотиком, прогноз хороший. В редких случаях у пациента может развиться одно из осложнений. [26] У некоторых пациентов может возникнуть повторная инфекция в течение одного месяца лечения антибиотиками. Часто это происходит из-за несоблюдения режима приема антибиотиков, хотя это может быть результатом повторного воздействия. Если это происходит, пациента можно лечить альтернативным антибиотиком, часто с более широким охватом, и можно подчеркнуть важность соблюдения режима лечения и предотвращения рисков.Наиболее часто используемыми антибиотиками являются амоксициллин-клавулановая кислота, клиндамицин, пенициллин G для внутримышечного введения. Если первоначально использовался цефалоспорин первого поколения, антибиотики обычно превращаются в цефалоспорин третьего поколения [2].
Инфекции глотки, передаваемые половым путем, легко поддаются лечению и чаще всего протекают бессимптомно. [21]
Редкие инфекции дифтерии и Yersinia pestis вполне поддаются лечению при наличии основных медицинских ресурсов, хотя они могут быть связаны с плохим прогнозом, так как большинство случаев развиваются в условиях ограниченных ресурсов.[24] [25] В регионах, где дифтерия встречается, смертность от дифтерии может составлять от 3 до 20%, что часто связано с миокардитом или крайне недостаточным доступом к медицинской помощи. [27] Аналогичным образом, смертность, связанная с Yersinia pestis, колеблется от менее 15% при лечении до 60–100% при отсутствии лечения [28].
Осложнения
В зависимости от бактериальной причины бактериального фарингита могут развиться различные осложнения.Как правило, бактериальная инфекция может распространяться, вызывая абсцесс, целлюлит, лимфаденит, менингит и бактериемию. Это также вызовет местный отек, который может привести к воспалению из-за окклюзии, например синуситу и среднему отиту. [12] [13]
Хотя стрептококковые инфекции обычно проходят самостоятельно, важно диагностировать и лечить их антибиотиками, поскольку инфекции GABHS могут привести к серьезным осложнениям. Экзотоксины, вырабатываемые БГСА, могут вызывать скарлатину или синдром токсического шока.Аутоиммунный ответ, вызванный инфекцией БГСА, может привести к острой ревматической лихорадке. [15] [16] Хотя постстрептококковый гломерулонефрит также является следствием дисфункционального иммунного ответа, он не предотвращается соответствующим лечением антибиотиками. [2]
Инфекции, передаваемые половым путем, такие как гонорея и хламидиоз, часто протекают бессимптомно и обычно не приводят к осложнениям для хозяина, но являются заразными, приводя к инфекциям для партнеров, которые могут быть симптоматичными и могут привести к таким осложнениям, как воспалительное заболевание органов малого таза, орхит и простатит.[29]
Первичная патология дифтерии возникает из-за выработки токсинов. Токсин вызывает некроз и воспаление, может привести к респираторной недостаточности из-за отека верхних дыхательных путей, сердечно-сосудистой недостаточности из-за токсин-индуцированного миокардита и местного или системного паралича из-за неврологической токсичности. [24] [25]
Фарингит, вызванный Yersinia pestis, представляет собой потенциальное место заражения, а не типичное начальное проявление. Чума обычно прогрессирует до тяжелого лимфаденита с последующим возможным распространением.[30]
Сдерживание и обучение пациентов
Бактериальный фарингит, как и большинство инфекционных агентов, можно предотвратить с помощью надлежащих протоколов гигиены, таких как мытье рук, отказ от еды или напитков и прикрытие рта во время чихания. Пациенты должны быть осведомлены о важности завершения курса антибиотиков в соответствии с предписаниями. Это повысит эффективность лечения, предотвратит рецидив инфекций и предотвратит устойчивость к противомикробным препаратам.
Улучшение результатов команды здравоохранения
Основными направлениями улучшения результатов лечения бактериального фарингита являются точное выявление и ответственное лечение причины фарингитов пациентов. Исходя из ожиданий пациентов, а также ограничений чувствительности и скорости текущего тестирования, в настоящее время практика часто заключается в неправильном лечении того, что является вероятным небактериальным фарингитом, с помощью антибиотиков.[31] Следуя указаниям Американского общества инфекционистов, Американской академии педиатрии и Центров по контролю и профилактике заболеваний, медицинские бригады должны принимать совместные решения со своими пациентами и семьями. [2]
Клиницисты, медсестры, фармацевты и их бригады обязаны честно обсуждать как преимущества, так и ограничения проводимых ими тестов, а также антибиотики и другие виды лечения, которые они могут назначать. Чрезвычайно важно учитывать честные проблемы со здоровьем, а также логистические трудности, связанные с посещением офиса, тестированием и отсутствием на работе или в школе.Медицинские бригады должны обсудить варианты лечения, включая только наблюдение, немедленное лечение антибиотиками и составление отсроченного рецепта, чтобы пациенты могли получать антибиотики в будущем, не обращаясь к врачу лично. Контекст этой помощи также требует расширения возможностей удаленной помощи, таких как визиты по видео или телефону. [2] [32] [33] [34]
Одних клинических признаков недостаточно для диагностики стрептококкового фарингита, и их следует дополнять RADT или посевом из зева.Положительный результат RADT не требует подтверждения. [2] [Уровень 1]
Обычное подтверждение отрицательного RADT посевом из горла взрослым не требуется. [2] [Уровень 2]
Пациенты с фарингитом вирусной этиологии с высокой вероятностью не должны проходить тестирование ни с помощью RADT, ни с посевом из горла. [2] [Уровень 1]
Ведение острого фарингита у взрослых: надежность экспресс-тестов на стрептококк и клинические результаты | Инфекционные болезни | JAMA Internal Medicine
Фон Как использовать клиническую оценку, экспресс-тест на стрептококковый антиген (RSAT) и результаты посева неясно для эффективного лечения острого фарингита у взрослых.
Методы В это проспективное когортное исследование вошли 372 взрослых пациента с фарингитом, пролеченных в клинике первичной медицинской помощи при университете Швейцарии. У подходящих пациентов с 2–4 клиническими симптомами и признаками (температура ≥38 ° C, миндалинный экссудат, болезненная шейная лимфаденопатия, отсутствие кашля или ринита) мы выполнили RSAT и получили посев из горла. Мы измерили чувствительность и специфичность RSAT с посевом в качестве золотого стандарта и сравнили соответствующее использование антибиотиков с затратами на пациента, получившего соответствующее лечение, по следующим 5 стратегиям: симптоматическое лечение, систематический RSAT, селективный RSAT, эмпирическое лечение антибиотиками и систематическое культивирование.
Результаты RSAT имел высокую чувствительность (91%) и специфичность (95%) для диагностики стрептококкового фарингита. Систематический посев из горла привел к максимальному использованию антибиотиков у 38% пациентов со стрептококковым фарингитом. Систематическая RSAT привела к почти оптимальному лечению (94%) и назначению антибиотиков (37%) с минимальным чрезмерным использованием антибиотиков (3%) и недостаточным использованием (3%). Эмпирическое лечение антибиотиками у пациентов с 3 или 4 клиническими симптомами или признаками привело к более низкому уровню соответствующей терапии (59%), но более высокому уровню использования антибиотиков (60%), чрезмерного использования (32%) и недостаточного использования (9%).Систематическая RSAT была более рентабельной, чем стратегии, основанные на эмпирическом лечении или культуре: 15, 26 и 32 доллара соответственно на каждого пациента, прошедшего соответствующее лечение.
Выводы RSAT, который мы использовали, является действительным тестом для диагностики фарингита у взрослых. Клинический подход, сочетающий этот RSAT и клинические данные, эффективно сокращает количество случаев неправильного назначения антибиотиков у взрослых пациентов с острым фарингитом. Эмпирическая терапия у пациентов с 3 или 4 клиническими симптомами или признаками приводит к чрезмерному употреблению антибиотиков.
Фарингит — распространенный симптом, на который приходится от 1% до 2% посещений врачей первичного звена. 1 Острый фарингит у взрослых в основном вызывается вирусом; только около 10% случаев являются бактериальными, в основном вызванными β-гемолитическими стрептококками группы А, что является единственным показанием для противомикробной терапии. 2 При стрептококковом фарингите группы А (GASP) пенициллин V эффективно сокращает продолжительность симптомов на 1-2 дня, распространение болезни и частоту гнойных осложнений и ревматической лихорадки, что является исключительным явлением в развитых странах. 3 -7 Антибактериальная терапия обеспечивает умеренный клинический эффект у меньшинства пациентов с фарингитом, который является самоограничивающимся заболеванием с низкой частотой осложнений. 3 , 4 Хотя антибиотикотерапию следует назначать только нескольким пациентам с ГАСП, врачи назначают антибиотики 73% пациентов с фарингитом. 8 Широкое применение антибиотиков часто вызывает побочные эффекты (например, аллергию или диарею), увеличивает использование медицинских услуг и увеличивает расходы, а также способствует устойчивости к бактериям. 3 , 9
Клинический диагноз GASP, поставленный врачом, имеет низкую чувствительность и специфичность, поскольку ни один элемент в истории болезни или клиническом обследовании не является достаточно точным. 10 -12 Клинические оценки Centor et al. 11 и McIsaac et al. 13 , основанные на 4 клинических результатах, являются действительными и надежными инструментами, которые позволяют клиницистам оценить вероятность GASP у взрослых. Недавние быстрые тесты на стрептококковый антиген (RSAT) с использованием оптических иммуноанализов дают немедленные результаты с более высокой средней чувствительностью (80% -90%) и специфичностью (≥95%). 4 , 14 -17 Диагностика, основанная на результатах RSAT, может снизить ненужное назначение антибиотиков и затраты и не увеличивает частоту осложнений даже без подтверждающих посев отрицательных результатов RSAT. 13 , 15 -19 Тем не менее, посев из горла остается золотым стандартом для диагностики GASP, несмотря на его неоптимальную эффективность, стоимость и задержку результатов в клинической практике. 3 , 4,15
Недавние исследования у взрослых показывают, что клинический подход, основанный на посеве из горла, лучше, чем RSAT или эмпирическое лечение, для оптимизации назначения антибиотиков и экономической эффективности. 16 , 20 Поскольку ни одно клиническое исследование еще не сравнивало эффективность, осуществимость и стоимость различных клинических подходов, нет основанного на фактических данных консенсуса относительно наилучшего клинического подхода к лечению острого фарингита у взрослых, когда ключевой проблемой является диагностика и антимикробная терапия ГАСП. Руководства США, основанные на мнениях экспертов, рекомендуют 4 альтернативные стратегии с использованием клинической оценки, результатов RSAT или результатов посева из горла, чтобы ограничить назначение антибиотиков пациентам, у которых с наибольшей вероятностью будет GASP, и получить пользу от антимикробной терапии. 3 , 4
Это наблюдательное исследование, проведенное в когорте взрослых амбулаторных пациентов с фарингитом, преследовало 2 цели: измерить эффективность RSAT по различным клиническим показателям и сравнить назначение антибиотиков с прямыми затратами на различные рекомендуемые стратегии с использованием клинической оценки, результатов RSAT и результатов посева для лечения острого фарингита у взрослых амбулаторно.
Дизайн, сеттинг и участники
Мы провели проспективное когортное исследование в амбулаторной клинике университетского центра первичной медико-санитарной помощи в Женеве, Швейцария, с 1 марта 1999 г. по 30 сентября 2001 г.Медицинскую помощь оказывали 15 медицинских ординаторов и 8 лечащих врачей, среди которых многие меняются ежегодно, некоторые работают неполный рабочий день, а замены и ротации являются обычным явлением. Мы включили всех последовательных пациентов старше 15 лет с фарингитом, по крайней мере, с 2 из 4 клинических данных Centor et al. 11 : температура 38 ° C или выше, миндалинный экссудат, болезненная шейная лимфаденопатия, а также отсутствие кашля или ринита. Пациенты с отсутствием или 1 симптомом или признаком были исключены, поскольку большинство экспертов согласны с тем, что им не требуется дальнейшее тестирование или антибактериальная терапия, поскольку распространенность GASP ниже 5%. 3 , 4 Ни один пациент не отказался от участия в исследовании. Исследование соответствовало этическим нормам Университетской клиники Женевы, Женева, Швейцария.
Для каждого включенного пациента врач собирал историю болезни, проводил клиническое обследование и определял балл Centor, соответствующий сумме 4 клинических результатов. Для всех пациентов с оценкой от 2 до 4 врачи взяли 2 мазка из зева: 1 для RSAT и 1 для посева.Врачи были обучены выполнять RSAT, оптический иммуноферментный анализ (TestPack Plus Strep A w / OBC [On-Board Controls] II; Abbott Laboratories, Abbott Park, Ill) в соответствии с инструкциями производителя. Сравнительное исследование показало, что этот RSAT имеет самую высокую чувствительность и специфичность в амбулаторной медицинской практике. 21 Горловые культуры инкубировали на 2 чашках с кровяным агаром в анаэробной среде без ингибитора и считывали через 48 часов в лаборатории бактериологии университетской больницы Женевы.Врачи прописали лечение антибиотиками сразу всем пациентам с положительным результатом RSAT или в течение 48 часов пациентам с положительным посевом из горла. Наши местные правила рекомендуют в качестве первого выбора пенициллин V по 1 миллиону единиц 3 раза в день в течение 10 дней или макролид для пациентов с аллергией на пенициллин.
Мы сравнили производительность RSAT с культурой из зева, считающейся золотым стандартом. Для всей выборки и каждой клинической оценки мы определили чувствительность, специфичность, положительные и отрицательные прогностические значения с использованием метода Ньюкомба-Уилсона без поправки на непрерывность, 22 и положительных и отрицательных отношений правдоподобия с их 95% доверительными интервалами. 23
Используя клинические данные и результаты тестов, мы построили модель анализа решений (Data 3.5; Treeage Software, Williamstown, Mass), сравнивая назначение антибиотиков для 5 стратегий лечения острого фарингита у взрослых:
Симптоматическое лечение без тестирования или лечения.
Систематическая RSAT с антибактериальной терапией у пациентов с положительными результатами.
Селективный RSAT у пациентов с 2 или 3 клиническими критериями и эмпирическая антибактериальная терапия у пациентов с 4 баллами.
Эмпирическая антибактериальная терапия без тестирования у пациентов с 3 или 4 клиническими критериями.
Систематический посев с лечением антибиотиками у пациентов с положительными результатами.
Для оценки эффективности каждого клинического подхода мы использовали модель принятия решений для расчета следующих показателей: использование антибиотиков во всей когорте, соответствующее использование антибиотиков у пациентов с GASP, чрезмерное использование антибиотиков у пациентов без GASP, недостаточное использование антибиотиков у пациентов с GASP, и соответствующее лечение антибиотиками у пациентов с ГАСП и без антибиотиков у пациентов без ГАСП.Мы не оценивали качество жизни, осложнения и побочные эффекты лекарств.
Для каждого клинического подхода мы рассчитали медицинские затраты на пациента, получившего соответствующее лечение. В анализе базового случая с использованием цен 2002 г. в швейцарских франках, конвертированных в доллары США, затраты составили 25 долларов США за 10-дневный курс лечения пенициллином, 5 долларов США за RSAT и 18 долларов США за посев из горла. Стоимость консультации и симптоматического лечения была исключена, поскольку предполагалось, что они идентичны для каждого клинического подхода.Чтобы проверить надежность наших результатов, мы провели анализ чувствительности, чтобы оценить, будут ли распространенность GASP, чувствительность и специфичность RSAT, стоимость RSAT, стоимость антибиотиков и чувствительность посева влияют на рентабельность каждого клинического подхода.
Мы включили 372 последовательных амбулаторных пациента с фарингитом, большинство из которых были молодыми, с небольшим преобладанием женщин (таблица 1). Частота клинических результатов Centor et al. 11 была довольно схожей (60% -75%).Более 80% пациентов имели заболевание средней степени тяжести с клиническими показателями 2 и 3. Общая распространенность ГАСП, основанная на культуре из горла, составляла 37,6% и постоянно увеличивалась с увеличением клинической оценки (23,6%, 41,0% и 60,3% соответственно. , для 2, 3 и 4 критериев). Распространенность стрептококков группы G составила 5,1%, а стрептококков группы C — 3,8%, при этом 1 пациент в каждой группе имел положительные результаты RSAT. Восемьдесят восемь врачей вылечили в среднем 4,2 пациента в течение трех последовательных академических лет.
По сравнению с посевом из зева, RSAT достиг высокой глобальной чувствительности (91.4%; 95% доверительный интервал, 85,6% -95,0%) и специфичность (95,3%; 95% доверительный интервал, 91,7% -97,3%). Показатели RSAT были хорошими, с высокой положительной прогностической ценностью (92%), отрицательной прогностической ценностью (95%) и положительным отношением правдоподобия (19,3) (таблица 2). Чувствительность и положительная прогностическая ценность прогрессивно увеличивались с увеличением клинической оценки, что свидетельствует о возможном смещении спектра, которое не было значимым, поскольку доверительные интервалы перекрываются. Специфичность и отрицательная прогностическая ценность оставались довольно постоянными независимо от клинической оценки.
Систематический посев из горла дает самые высокие показатели соответствующего лечения и использования антибиотиков, но также является наиболее дорогостоящим клиническим подходом (Таблица 3). При систематическом использовании RSAT частота соответствующего лечения и назначения антибиотиков была почти оптимальной с минимальным чрезмерным и недостаточным использованием антибиотиков. Более того, этот клинический подход стоит вдвое дешевле и позволяет незамедлительно принимать решения о назначении антибиотиков. Селективный RSAT у пациентов с клиническими показателями 2 или 3 и эмпирическое лечение у пациентов с клиническими показателями 4 увеличивали чрезмерное использование антибиотиков при более высоких затратах.Эмпирическая терапия антибиотиками у пациентов с клиническими показателями 3 или 4 привела к высокому показателю назначения антибиотиков с более частым их чрезмерным использованием у пациентов без GASP, чем у пациентов с GASP. При таком клиническом подходе менее 60% пациентов получали соответствующее лечение с более высокими затратами. Симптоматическое лечение без тестирования или антибиотикотерапии было наименее дорогостоящим клиническим подходом, но только 62% пациентов получили соответствующее лечение из-за недостаточного использования антибиотиков у всех пациентов с ГАСП.
В анализе экономической эффективности можно рассматривать только 3 стратегии (Таблица 3). Симптоматическое лечение было наименее затратным и менее эффективным вариантом, систематическая RSAT имела самое низкое соотношение затрат и эффективности, а систематическая культура была наиболее эффективным, но наиболее дорогостоящим вариантом.
Эти результаты не были чувствительны к вариациям распространенности ГАСП. Когда распространенность была менее 41%, систематический RSAT был наименее затратным клиническим подходом по сравнению с систематическим культивированием.При более высокой распространенности эмпирическое лечение пациентов с клиническими показателями 3 или 4 было менее затратным, но также менее эффективным, чем систематическое RSAT (расширенное преобладание).
При стоимости антибиотиков от 5 до 50 долларов систематическая RSAT снова была лучшим вариантом. Другие стратегии были либо менее эффективными для аналогичных затрат (прямое доминирование), либо имели более высокие показатели предельной эффективности затрат (расширенное доминирование). Пока стоимость антибиотиков составляла менее 22 долларов, эмпирическое лечение пациентов с клиническими показателями 3 или 4 было наименее затратным вариантом, но было менее эффективным, чем эмпирическое лечение (прямое преобладание).
Изменение стоимости RSAT от 1,00 до 20,00 долларов не повлияло на эти результаты. Систематический RSAT оставался наименее дорогим вариантом, пока его стоимость не превышала 5,70 долларов. После этого эмпирическое лечение пациентов с клиническими показателями 3 или 4 и селективным RSAT стало менее затратным, но было менее эффективным, чем систематическое RSAT (расширенное доминирование).
ХарактеристикиRSAT не изменили наших результатов, потому что систематический RSAT был лучшим вариантом, когда чувствительность RSAT была больше 37%, а его специфичность была больше 77%.Наконец, изменение чувствительности культуры до 90% не повлияло на эти результаты.
Наше исследование показывает, что RSAT может быть действенным диагностическим тестом для диагностики GASP у взрослых с фарингитом, особенно в сочетании с клинической шкалой Centor и используется у пациентов с высокой вероятностью GASP. Согласно нашим результатам, лучшим клиническим подходом к диагностике и лечению фарингита у взрослых является систематическая RSAT у пациентов с минимум 2 клиническими признаками, указывающими на GASP.Среди различных вариантов, рекомендованных в руководствах, этот клинический подход оптимизирует назначение антибиотиков, ограничивая как чрезмерное, так и недостаточное использование, и является рентабельным. Сильные стороны этого исследования включают дизайн, основанный на довольно большой и реальной когорте взрослых пациентов первичной медико-санитарной помощи, сравнение соответствующих стратегий, рекомендованных в текущих руководствах, 3 , 4 и анализ экономической эффективности с надежными результатами.
У нашего исследования есть несколько потенциальных ограничений.Мы оценили теоретические эффекты различных стратегий на использование антибиотиков и затраты на модели анализа решений, но не на основе клинических испытаний, оценивающих перспективные реальные практики и их влияние на симптомы, качество жизни, осложнения, использование здравоохранения и долгосрочные затраты. Поскольку пациенты были набраны из поликлиники университетской больницы, наше исследование могло включать в себя отобранную выборку с более тяжелым заболеванием, чем пациенты, наблюдаемые в практике первичной медико-санитарной помощи. Диагностические тесты не смогли отличить пациентов с ГАСП от носителей стрептококков, распространенность которых минимальна среди взрослых.Возможное присутствие отобранной популяции и носителей стрептококка может переоценить распространенность ГАСП. Однако маловероятно, что выбор наилучшего клинического подхода изменится, поскольку анализ чувствительности показал, что более низкая распространенность GASP не влияет на использование антибиотиков и экономическую эффективность.
Систематическая RSAT не учитывает большинство случаев стрептококкового фарингита групп C и G. Однако это, вероятно, мало влияет на наиболее эффективный клинический подход, поскольку распространенность этих типов фарингита составляет менее 10%, они не вызывают серьезных осложнений, и нет убедительных доказательств того, что антибактериальная терапия эффективна. 2
Посев из одного горла не является оптимальным стандартом, поскольку его чувствительность составляет от 90% до 95%. Использование двух разных культур в качестве стандарта могло повлиять на производительность RSAT; однако этот эффект, вероятно, невелик, поскольку методика выборки для обоих тестов идентична и выполнялась одновременно одним и тем же человеком. Анализ чувствительности показал, что чувствительность посева не влияла на соответствующее лечение и экономическую эффективность. Использование двух культур в качестве стандарта является спорным и не отражает реальных условий клинической практики или аналогичных исследований в первичной медико-санитарной помощи. 15 -17
Сравнение эффективности RSAT ограничено различиями в тестах, популяциях и профилях болезни между исследованиями. В более ранних исследованиях производительность RSAT была ниже и более изменчивой; однако недавние исследования, посвященные тестированию RSAT на основе высокочувствительных оптических иммуноанализов, показали аналогичную специфичность, но более низкую чувствительность. 14 -16 Большинство исследований тестировали RSAT у детей и включали всех пациентов с фарингитом независимо от клинической оценки.Многие ложноотрицательные результаты RSAT могут быть связаны с меньшей бактериальной нагрузкой у пациентов с более низким клиническим баллом. Эта возрастающая чувствительность с более высокими клиническими показателями предполагает смещение спектра, о котором сообщают другие с аналогичной чувствительностью. 24 Этот эффект мог повысить чувствительность нашего исследования, в которое были включены только пациенты с клиническими показателями от 2 до 4 и более высокой распространенностью ГАСП. Следовательно, клинический подход, основанный на RSAT, у пациентов с более высокими клиническими показателями увеличивал частоту диагностики GASP и соответствующее назначение антибиотиков.Ложноположительные результаты RSAT не связаны с клинической оценкой, отдельными врачами или группой резидентов, и только некоторые из них связаны с перекрестными реакциями со стрептококками, не принадлежащими к группе А. Они могут быть вызваны проблемами при транспортировке или хранении некоторых культур. Наш анализ чувствительности подтверждает, что систематический RSAT, вероятно, является наиболее эффективным клиническим подходом, поскольку на него не влияют правдоподобные вариации чувствительности и специфичности RSAT.
В аналогичном исследовании стратегии, основанные на культуре, дали несколько лучшие результаты, чем стратегии, использующие RSAT для диагностики GASP с соответствующей антибактериальной терапией. 16 Эти противоречивые результаты можно объяснить разной распространенностью GASP в двух исследованиях (21,9% против 37,6%). Это несоответствие может быть результатом различных методов оценки, настроек, характеристик пациентов и смещения спектра, предложенного нашими выводами. Однако оба исследования показали, что эмпирическое лечение пациентов с более высокими клиническими показателями приводит к массовому злоупотреблению антибиотиками. 16 Neuner et al. 20 недавно сообщили, что культивирование было немного более рентабельным, чем RSAT.Однако их исследование было основано не на клинических наблюдениях, а на модели принятия решений с использованием предположений, взятых из литературы. Кроме того, некоторые из их предположений отличались от наших данных, например, стратегии, проверенные у всех пациентов, независимо от клинической оценки, более низкая распространенность GASP и стоимость RSAT в 2,7 раза выше.
Наши результаты показывают, что сочетание систематического RSAT с клинической оценкой является наиболее эффективным клиническим подходом к диагностике и лечению острого фарингита у взрослых.Они не поддерживают подходы, основанные на результатах посева из горла или эмпирического лечения, которые рекомендованы в недавнем руководстве. 3 Клинический подход, основанный на клинической шкале и RSAT, ограничивает назначение антибиотиков в основном пациентам с GASP, которым это лечение приносит пользу. 3 , 4 Ориентация на этих пациентов делает антибактериальную терапию более эффективной и сокращает продолжительность симптомов и частоту гнойных осложнений. 5 , 6 Клиническая польза может быть небольшой для отдельных пациентов, но значительной для популяции, в которой заболевание является обычным.Этот клинический подход также удобен в клинической практике, поскольку он позволяет принимать немедленные терапевтические решения и ограничивает чрезмерное назначение антибактериальной терапии. 13 , 17 Предотвращает отсрочки лечения, что снижает влияние на облегчение симптомов и увеличивает нагрузку на последующие телефонные звонки. Клинический подход, основанный на RSAT, также может снизить побочные эффекты и затраты на ненужную антибактериальную терапию. 3 Поскольку врачи назначают противомикробную терапию, обычно не рекомендуемые антибиотики широкого спектра действия, для большинства пациентов с фарингитом, систематическая RSAT может способствовать ограничению развития устойчивости к антибиотикам в общинах. 3
Наш анализ экономической эффективности применим к другим странам с другим экономическим статусом, потому что наш анализ чувствительности показывает, что RSAT является предпочтительным клиническим подходом для широкого диапазона затрат. Например, результаты остаются неизменными для розничной цены в США 10-дневного курса лечения пенициллином (5–20 долларов), который рекомендуется в более низких дозах, чем в Швейцарии. 3 , 20
Хотя наши результаты предполагают, что один клинический подход более эффективен, недавние исследования, в том числе наше, не использовали экспериментальный дизайн и, следовательно, пришли к другим выводам.Чтобы определить оптимальный подход к лечению фарингита у взрослых, рандомизированные контролируемые испытания могут протестировать и сравнить различные стратегии лечения в первичной медико-санитарной помощи и измерить их влияние на реальной практике на назначение антибиотиков, симптомы, качество жизни, осложнения, побочные эффекты терапии, здравоохранение. использование и затраты.
Мы пришли к выводу, что RSAT — действительный тест для диагностики фарингита у взрослых. Сочетание RSAT с клинической оценкой представляется эффективным и экономичным клиническим подходом для ограничения назначения антибиотиков и надлежащего лечения острого фарингита у взрослых.
Для корреспонденции: Жан-Поль Хумэр, MD, MPH, Медицинская поликлиника, Отделение общественной медицины, Университетская больница Женевы, 24 rue Micheli-du-Crest, CH-1211, Geneva 14, Switzerland (Jean-Paul.Humair @ hcuge.ch).
Принята к публикации: 17 августа 2005 г.
Раскрытие финансовой информации: Нет.
Предыдущие презентации: Это исследование было частично представлено на 16-й Всемирной конференции семейных врачей; 14 мая 2001 г .; Дурбан, Южная Африка; и на 25-м ежегодном собрании Общества общей внутренней медицины; 4 мая 2002 г .; Атланта, Джорджия
1.Армстронг GLPinner RW Амбулаторные визиты по поводу инфекционных заболеваний в США, 1980–1996 гг. Arch Intern Med 1999; 1592531-2536PubMedGoogle ScholarCrossref 3.Cooper Р.Дж.Хоффман JRBartlett JG и другие. Принципы правильного применения антибиотиков при остром фарингите у взрослых: история вопроса. Ann Intern Med 2001; 134509-517PubMedGoogle ScholarCrossref 4.Bisno ALGerber MAGwaltney JM JrKaplan Э.Л.Шварц Американское общество инфекционных заболеваний, Практическое руководство по диагностике и лечению стрептококкового фарингита группы А. Clin Infect Dis 2002; 35113-125PubMedGoogle ScholarCrossref 5. Дел Мар CBGlasziou PPSpinks AB Антибиотики от боли в горле. Cochrane Database Syst Rev 2004; (4) CD000023PubMedGoogle Scholar6.Zwart SSachs APRuijs GJGubbels JWHoes AWde Melker Пенициллин RA при острой боли в горле: рандомизированное двойное слепое исследование, продолжающееся семь дней по сравнению с трехдневным лечением или плацебо у взрослых. BMJ 2000; 320150-154PubMedGoogle ScholarCrossref 7.Дагнели CFvan der Graaf Ю.Дэ Мелькер РА Есть ли польза от пенициллина у пациентов с ангиной? рандомизированное двойное слепое плацебо-контролируемое клиническое исследование пенициллина V в общей практике. Br J Gen Pract 1996; 46589-593PubMedGoogle Scholar8.Linder Дж.А.Стаффорд RS Антибиотикотерапия взрослых с болью в горле врачами первичной медико-санитарной помощи. JAMA 2001; 2861181-1186PubMedGoogle ScholarCrossref 9. Little PGould CWilliamson IWarner GGantley MKinmonth А.Л. Повторная посещаемость и осложнения в рандомизированном исследовании стратегии назначения при боли в горле: лечебный эффект назначения антибиотиков. BMJ 1997; 315350-352PubMedGoogle ScholarCrossref 10.Komaroff ALPass TMAronson MD и другие. Прогнозирование стрептококкового фарингита у взрослых. J Gen Intern Med 1986; 11-7PubMedGoogle ScholarCrossref 11.Centor RMWhitherspoon JMDalton HPBrody CELink K Диагноз ангины у взрослых в отделении неотложной помощи. Принятие решений в медицине 1981; 1239–246PubMedGoogle ScholarCrossref 12.Ebell MHSmith МАБарри HCIves KCarey M Рациональное клиническое обследование: у этого пациента ангина? JAMA 2000; 2842912-2918PubMedGoogle ScholarCrossref 13.McIsaac WJGoel VTo TLow DE Достоверность оценки боли в горле в семейной практике CMAJ 2000; 163811-815PubMedGoogle Scholar14.Gerber MATanz РРКабат W и другие. Оптический иммуноферментный тест на β-гемолитический стрептококковый фарингит группы А: многоцентровое исследование на базе кабинета. JAMA 1997; 277899-903PubMedGoogle ScholarCrossref 15. Гербер М.А.Шульман ST Экспресс-диагностика фарингита, вызванного стрептококками группы А. Clin Microbiol Rev 2004; 17571-580PubMedGoogle ScholarCrossref 16.McIsaac WJKellner JDAufricht П.В.анджака Сейчас Д.Э. Эмпирическая проверка рекомендаций по лечению фарингита у детей и взрослых. JAMA 2004; 2911587-1595 [опубликованное исправление появляется в JAMA . 2005; 294: 2700] PubMedGoogle ScholarCrossref 17.Atlas SJMcDermott SMMannone CBarry MJ Роль пункта оказания медицинской помощи пациентам с острым фарингитом. J Gen Intern Med 2005; 20759-761PubMedGoogle ScholarCrossref 18.Webb KH Имеет ли смысл подтверждение посева высокочувствительных экспресс-тестов на стрептококк? анализ медицинского решения. Педиатрия 1998; 101e2PubMedGoogle ScholarCrossref 19.Webb KH Использование высокочувствительного экспресс-теста без подтверждения отрицательных результатов посевом. J Fam Pract 2000; 4934-38 [опубликованное исправление есть в J Fam Pract . 2000; 49: 378] PubMedGoogle Scholar20.Нойнер JMHamel MBPhillips RSBona Каронсон MD Диагностика и лечение взрослых с фарингитом. Ann Intern Med 2003; 139113-122PubMedGoogle ScholarCrossref 21.Morandi PADeom AMauris ARohner P Внешний контроль качества прямых тестов на антиген для обнаружения стрептококкового антигена группы А. Eur J Clin Microbiol Infect Dis 2003; 22670-674PubMedGoogle ScholarCrossref 22.Newcombe РГ Двусторонние доверительные интервалы для одной пропорции: сравнение семи методов. Stat Med 1998; 17857-872PubMedGoogle ScholarCrossref 23.Simel DLSamsa GPMatchar DB Отношения правдоподобия с уверенностью: оценка размера выборки для диагностических тестовых исследований. J Clin Epidemiol 1991; 44763-770PubMedGoogle ScholarCrossref 24.Dimatteo Л.А.Ловенштейн SRBrimhall BReiquam WGonzales R Взаимосвязь между клиническими признаками фарингита и чувствительностью экспресс-теста на антиген: свидетельство смещения спектра. Ann Emerg Med 2001; 38648-652PubMedGoogle ScholarCrossrefПример использования стрептококкового фарингита
1. Shulman ST, Bisano AL, Clegg HW, et al. Руководство по клинической практике по диагностике и лечению стрептококкового фарингита группы А: Обновление 2012 г., подготовленное Американским обществом инфекционных болезней. Clin Inf Dis. 2012; 55 (10): e86-e102.
2. Эбелл М. Х., Смит М. А., Барри Х. К., Айвз К., Кэри М. Рациональное клиническое обследование. У этого пациента ангина? ДЖАМА.2000; 284: 2912–8.
3. McIsaac WJ, Kellner JD, Aufricht P, Vanjaka A, Low DE. Эмпирическая проверка рекомендаций по лечению фарингита у детей и взрослых. JAMA 2004; 291: 1587–95.
4. Гербер М.А. Диагностика фарингита: методика посева из зева. В кн .: Шульман С.Т., под ред. Фарингит: лечение в эпоху спада ревматической лихорадки. Нью-Йорк: Praeger, 1984: 61–72.
5. Брайен Дж. Х., Бас Дж. У. Стрептококковый фарингит: оптимальное место для посева из зева.J Pediatr. 1985; 106: 781–3.
6. Kellogg JA. Пригодность процедур посева из горла для обнаружения стрептококков группы А и в качестве эталонных стандартов для оценки наборов для обнаружения стрептококкового антигена. J Clin Microbiol. 1990; 28: 165–9.
7. Гербер М.А., Шульман СТ. Экспресс-диагностика фарингита, вызванного стрептококками группы А. Clin Microbiol Rev.2004; 17: 571–80.
8. Танц Р. Р., Гербер М. А., Кабат В., Риппе Дж., Сешадри Р., Шульман СТ. Проведение экспресс-теста на выявление антигенов и посев из горла в педиатрических отделениях по месту жительства: значение для лечения фарингита.Педиатрия. 2009; 123: 437–44.
9. Найквист А.С., Гонсалес Р., Штайнер Дж. Ф., Санде М. А.. Назначение антибиотиков детям при простуде, инфекциях верхних дыхательных путей и бронхите. ДЖАМА. 1998; 279: 875–7.
10. Пелуччи К., Григорян Л., Галеоне С. и др. Руководство по лечению острой ангины. Clin Microbiol Infect. 2012; 18 (Дополнение 1): 1-27.
11. Бринк В.Р., Раммелкамп СН-младший, Денни Ф.В., Ваннамейкер Л.В. Влияние пенициллина и ауреомицина на естественное течение стрептококковой ангины и фарингита.Am J Med. 1951; 10: 300.
% PDF-1.4 % 1 0 объект > поток конечный поток эндобдж 2 0 obj > поток х +
Фарингит
1.Определите гнойные и негнойные последствия стрептококков группы А. фарингит, который беспокоит врачей и пациентов.
2. Опишите методы лечения, рекомендованные для лечения стрептококкового фарингита группы А.
3. Перечислите симптомы, кроме боли в горле, которые могут быть связаны с клиническими проявлениями. проявление стрептококкового фарингита.
4. Сравните чувствительность и специфичность скрининга Strep с клиническим экзамен в диагностике острого стрептококкового фарингита.
5. Просмотрите историю риска ревматической лихорадки, связанной со стрептококками.
6. Опишите результаты физического обследования, диагностическое обследование и лечение следующего:
А. Афтозный стоматит.
Б. Надгортанник.
C. Фузоспирохетальный стоматит (стенокардия Винсента).
D. Гонококковый стоматит.
E. Герпетический стоматит.
F. Мононуклеоз.
Г. Тонзиллит.
H. Вирусный фарингит.
7. Перечислите признаки и симптомы фарингита, которые указывают на необходимость направления к специалисту.
- Источник: Семейная медицина: Амбулаторная помощь и профилактика, Глава 57, страницы 389-395
Основы семейной медицины, Глава 18, страницы 207-216
Признаки и симптомы в семейной медицине, Глава 40, страницы 505 -513
Дополнительные статьи см.


 2000. Vol. 355. № 9217. P. 1776–1780.
2000. Vol. 355. № 9217. P. 1776–1780.
 , артериальная гипертензия;
, артериальная гипертензия;
 Через 1–2 дня появляются пузырьки на любом участке слизистой оболочки полости рта, губах, коже. В полости рта высыпания чаще локализуются на деснах и небе Пузырьки быстро вскрываются с образованием болезненных участков слизистой. Заживление наступает через 10–14 дней. В дальнейшем заболевание может рецидивировать, что провоцируется нахождением на солнце, ОРВИ, травмой, стрессом и ослаблением иммунитета. Отмечается устойчивость к проводимому лечению.
Через 1–2 дня появляются пузырьки на любом участке слизистой оболочки полости рта, губах, коже. В полости рта высыпания чаще локализуются на деснах и небе Пузырьки быстро вскрываются с образованием болезненных участков слизистой. Заживление наступает через 10–14 дней. В дальнейшем заболевание может рецидивировать, что провоцируется нахождением на солнце, ОРВИ, травмой, стрессом и ослаблением иммунитета. Отмечается устойчивость к проводимому лечению.

