инструкция по применению, классификация, статьи » Справочник ЛС
Нежелательные явления, представленные ниже, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости.
Частота встречаемости определяется следующим образом: очень часто (> 1/10), часто (> 1/100 и < 1/10), нечасто (> 1/1 000 и < 1/100). редко (> 1/10 000 и < 1/1 000), очень редко (< 1/10 000. включая отдельные случаи). Категории частоты были сформированы на основании клинических исследований препарата.
Частота встречаемости нежелательных явлений
Нарушения со стороны нервной системы
Часто: головная боль.
Нарушения со стороны кожи и подкожных тканей
Часто: потливость.
Нарушения со стороны костно-мышечной системы и соединительной ткани Часто:миалгия, артралгия.
Общие расстройства и нарушения в месте введения
Часто: повышение температуры, недомогание, озноб, слабость.
Покраснение, отек в области инъекции, болезненность, кровоподтек, уплотнение в месте инъекции.
Указанные явления обычно проходят самостоятельно через 1-2 дня.
Нежелательные явления, отмечавшиеся в ходе постмаркетингового наблюдения
Нарушения со стороны кроветворной и лимфатической системы:тромбоцитопения, транзиториая лимфаденопатия.
Нарушения со стороны иммунной системы: аллергические реакции, в редких случаях приводящие к развитию шока, ангионевротический отек.
Нарушения со стороны нервной системы: невралгия, парестезия (необычные ощущения, такие как жжение, онемение и т.д.), фебрильные судороги, неврологические расстройства, такие как энцефаломиелит, неврит, синдром Гийена-Барре (острая полинейропатия).
Сосудистые нарушения: васкулит, в очень редких случаях с преходящим вовлечением почек.
Нарушения со стороны кожи и подкожных тканей:

При появлении нежелательных явлений следует обратиться к врачу.
Пациент также должен быть проинформирован о необходимости сообщить врачу обо всех необычных нежелательных явлениях, не описанных в данной инструкции.
Вакцина агриппал s1: описание, инструкция, цена
Вакцина Агриппал S1(шприц 0,5мл N1) Италия Chiron S.p.A
Состав и форма выпуска: 1 доза трехвалентной инактивированной очищенной субъединичной вакцины (0,5 мл) содержит гемагглютинин и нейроминидазу следующих штаммов вируса гриппа типа:
A/New Caledonia (h2N1), (A/20/99) — 15 мкг гемагглютинина,
A/Moscow/10/99(h4N2), подобный A/Panama/2007/99 — RESVIR-17 — 15 мкг гемагглютинина,
B/Beijing/184/93, подобный Yamanashi/166/98 — 15 мкг гемагглютинина.
Антигенный состав вакцины ежегодно обновляется согласно рекомендациям ВОЗ.
Суспензия для инъекций — в одноразовом шприце или ампуле по 1 дозе (0,5 мл).
Характеристика: Вакцина для профилактики гриппа.
Фармакологическое действие: Иммуностимулирующее. Формирует специфический иммунитет к вирусам гриппа.
Показания: Профилактика гриппа у взрослых и детей старше 6 мес.
Противопоказания: Гиперчувствительность, в т.ч. к белку куриных яиц и др. компонентам вакцины в анамнезе. Вакцинация должна быть отложена при острых инфекционных заболеваниях.
Побочные действия: Могут наблюдаться аллергические реакции, местные реакции, недомогание, головная боль, повышение температуры тела, потливость, миалгия, артралгия; в очень редких случаях, как и при любой вакцинации, возможно развитие незначительных неврологических осложнений.
Способ применения и дозы: В/м, п/к, перед употреблением встряхнуть. Детям от 6 мес до 3 лет — 0,25 мл, от 3 лет и взрослым — 0,5 мл однократно; детям до 3 лет, которые не были вакцинированы в предыдущие годы, рекомендуется двукратная вакцинация по 0,25 мл с интервалом 4 нед.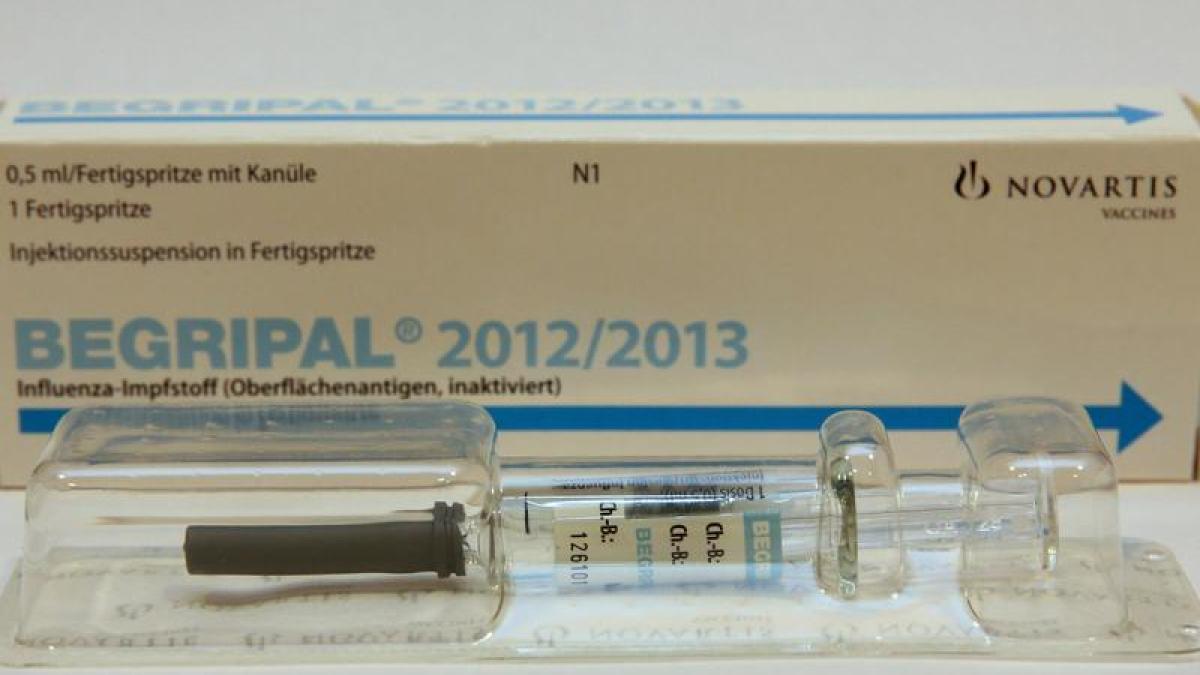
Меры предосторожности: Нельзя вводить в/в.
Срок годности: 1 г.
Условия хранения: При температуре 2-8 °C (не замораживать)
ФАРМАТЕКА » Вакцинация беременных против гриппа препаратом Агриппал S1
Четырнадцати здоровым беременным женщинам в возрасте 18–38 лет на сроке гестации 22–36 недель была проведена вакцинация против гриппа препаратом АГРИППАЛ S1, содержащим следующие штаммы: A/Brisbane/59/2007 (h2Nl), A/Brisbane/10/2007 (h4N2), B/Florida/4/2006. В поствакцинальном периоде общих и местных реакций не отмечено. Через месяц после вакцинации уровень антител в защитных значениях ко всем трем штаммам вируса гриппа регистрировался у 13 из 14 беременных женщин.
Вакцинация беременных женщин обеспечивает появление у матери специфических антител, которые транспортируются через плаценту к плоду и новорожденному, что создает у ребенка защитный уровень антител к определенным инфекциям. В зарубежной литературе имеются многочисленные данные, свидетельствующие о передаче материнских антител плоду и новорожденному при вакцинации женщин во время беременности от управляемых инфекций, в т.
Совещательный комитет по практике иммунизации (ACIP) рекомендует проводить вакцинацию здоровых беременных женщин против гриппа [3]. Взвесив все “за” и “против” в отношении вакцинации беременных, Американское агентство профилактики и контроля заболеваемости (CDC)
и Американский институт акушеров и гинекологов (ACOG) выступают за проведение вакцинации в следующих случаях: 1) при высоком риске контакта с заболевшими; 2) когда инфекция представляет опасность для матери или плода; 3) если вакцинация не принесет вреда. Поскольку ежегодно гриппом болеют 10 % взрослых и до 30 % детей, избежать контакта с заболеванием практически невозможно. В связи с этим определение соотношения между риском, который несет грипп для беременной женщины и плода, и риском, связанным с применением вакцины, является ключевым моментом при принятии решения относительно иммунизации.
Физиологические изменения, происходящие при беременности, предрасполагают к развитию серьезных осложнений при любой респираторной инфекции. В послеродовом периоде у женщин резервы легких снижены: потребление кислорода повышается на 15–25 %, а функциональная остаточная емкость легких снижается. После 10 недель беременности объем сердечного выброса повышается на 1,5 л/мин, при этом увеличиваются частота сердечных сокращений и ударный объем у матери. Показано, что даже у женщин с неосложненной беременностью пневмония повышает риск преждевременных родов [4, 5].
В послеродовом периоде у женщин резервы легких снижены: потребление кислорода повышается на 15–25 %, а функциональная остаточная емкость легких снижается. После 10 недель беременности объем сердечного выброса повышается на 1,5 л/мин, при этом увеличиваются частота сердечных сокращений и ударный объем у матери. Показано, что даже у женщин с неосложненной беременностью пневмония повышает риск преждевременных родов [4, 5].
Материнское инфицирование вирусом гриппа является одной из причин антенатальной гибели плода и новорожденного [5]. В период предэпидемии гриппа увеличивается частота госпитализаций и происходит снижение показателей здоровья беременных женщин [1, 4]. Описано существенное увеличение числа госпитализаций, связанных с болезнями дыхательных путей, среди женщин, беременных в течение сезона гриппа, в сравнении с годом до зачатия [1]. Это свидетельствует о том, что беременность является независимым фактором риска развития гриппозной инфекции. Перенесенный во время беременности грипп может привести к преждевременным родам и рождению детей с низкой массой тела.
Младенцы входят в группу повышенного риска по развитию осложнений и смерти от гриппа, но им противопоказана вакцинация против этой инфекции до 6 месяцев жизни в связи с тем, что их организм не может выработать достаточный уровень защитных антител. Во время эпидемии гриппа треть младенцев может заразиться в течение первого полугода жизни – в период, когда материнские антитела еще могут осуществлять защиту [1]. Было установлено, что более высокие уровни антител против гриппа обнаруживаются в образцах пуповинной крови младенцев, рожденных матерями, привитыми в течение беременности, по сравнению с новорожденными от невакцинированных матерей [6].
Безопасность инактивированной вакцины против гриппа была доказана при вакцинации беременных на разных сроках гестации [2]. При введении в течение 7 лет 2291 дозы инактивированной вакцины против гриппа беременным пациенткам не наблюдалось существенного увеличения неблагоприятных реакций среди матерей или младенцев [7].
В России проблеме вакцинации беременных против гриппа не уделяется должного внимания со стороны как органов здравоохранения, так и медицинского персонала. Только сложившаяся в 2009 г. сложная эпидситуация по гриппу А(h2Nl)v с многочисленными летальными исходами заставила обратить серьезное внимание на проблему вакцинопрофилактики беременных в соответствии с давно существующими рекомендациями различных медицинских сообществ и ВОЗ. В связи с этим целью настоящего исследования явилась оценка переносимости и иммуногенности субъединичной вакцины против гриппа Агриппал S1 у беременных.
Материал и методы
В период с октября 2008 по декабрь 2009 г. вакциной Агриппал S1 (вакцина противогриппозная трехвалентная субъединичная очищенная инактивированная, Новартис вакцинс энд диагностик, Италия) были провакцинированы 29 беременных во II и III триместрах беременности в возрасте от 18 до 38 лет. В 0,5 мл препарата содержатся культивированные на куриных эмбрионах расщепленные вирусы гриппа, представленные штаммами A/Brisbane/59/2007(h2Nl), A/Brisbane/10/2007(h4N2), B/Florida /4/2006. Вакцина вводилась внутримышечно в дельтовидную мышцу. Перед употреблением содержимое шприца доводилось до комнатной температуры. До вакцинации все женщины подписали информированное согласие на ее проведение. Перед вакцинацией беременную осматривали врачакушер-гинеколог, терапевт, оториноларинголог, иммунолог-аллерголог. Было проведено измерение температуры тела, артериального давления. У женщин, подлежавших вакцинации, беременность не была отягощенной гинекологическим статусом и протекала без осложнений.
В 0,5 мл препарата содержатся культивированные на куриных эмбрионах расщепленные вирусы гриппа, представленные штаммами A/Brisbane/59/2007(h2Nl), A/Brisbane/10/2007(h4N2), B/Florida /4/2006. Вакцина вводилась внутримышечно в дельтовидную мышцу. Перед употреблением содержимое шприца доводилось до комнатной температуры. До вакцинации все женщины подписали информированное согласие на ее проведение. Перед вакцинацией беременную осматривали врачакушер-гинеколог, терапевт, оториноларинголог, иммунолог-аллерголог. Было проведено измерение температуры тела, артериального давления. У женщин, подлежавших вакцинации, беременность не была отягощенной гинекологическим статусом и протекала без осложнений.
Уровень противогриппозных антител определяли до вакцинации и спустя месяц при помощи реакции торможения гемагглютинации (РТГА), как описано в МУ 3.3.2 1758-03.
Иммуногенность оценивали в соответствии с требованиями Европейского комитета к противогриппозным вакцинам (CPMP/BWP/214/96), согласно которым она должна соответствовать по крайней мере одному из трех критериев:
1. Сероконверсия (доля лиц с четырехкратным приростом титра антител после вакцинации) не менее 40 %.
Сероконверсия (доля лиц с четырехкратным приростом титра антител после вакцинации) не менее 40 %.
2. Серопротекция (доля лиц с защитным титром антител до и через 21–28 дней после вакцинации) не менее 70 %.
3. Кратность нарастания титров антител по сравнению с фоновой сывороткой не менее 2,5.
Результаты исследования статистически обрабатывались с использованием t-критерия Стьюдента. Вариационный анализ полученных результатов проводили с применением пакета прикладных программ Statistica 6.0.
Результаты и обсуждения
В поствакцинальном периоде не было отмечено ни местных, ни общих реакций. Беременность протекала физиологически, женщины чувствовали себя хорошо. В течение настоящей беременности до вакцинации у каждой женщины отмечено от 2 до 4 острых респираторных вирусных инфекций (ОРВИ). После вакцинации число эпизодов ОРВИ сократилось и наблюдалось всего у 20,6 % беременных. Инфекция протекала в легкой форме с однократным подъемом температуры от 37 до 37,4 °С, длительность заболевания не превышала 4 дней. Терапия ОРВИ включала орошение зева антисептическим раствором (мирамистином), очищение полости носа и носоглотки изотоническим стерильным раствором морской воды (Маример, Аквалор, Физиомер, Отривин). С целью повышения местного иммунитета полости рта и зева этим женщинам назначался препарат Лизобакт согласно инструкции по применению.
Терапия ОРВИ включала орошение зева антисептическим раствором (мирамистином), очищение полости носа и носоглотки изотоническим стерильным раствором морской воды (Маример, Аквалор, Физиомер, Отривин). С целью повышения местного иммунитета полости рта и зева этим женщинам назначался препарат Лизобакт согласно инструкции по применению.
Серологическое обследование с целью оценки иммунологической эффективности вакцинации проводилось при сравнении уровня антител в парных сыворотках, взятых до прививки и на 28-й день после вакцинации. Защитные титры антител ко всем трем штаммам вируса гриппа зарегистрированы у 13 из 14 вакцинированных (табл. 1, 2).
Таблица 1. Уровень серопротекции после вакцинации беременных препаратом Агриппал S1.
Таблица 2. Уровень сероконверсии и кратность нарастания титра антител по группам.
Подсчеты числа лиц с защитными титрами антител (≥ 1 : 40; серопротекция) показали, что у всех вакцинированных беременных уровень этих антител соответствует критерию CPMP. Наиболее иммуногенными оказались штамм гриппа А/h2N1 и B, при применении которых уровень серопротекции составил 71,4 и 100 % соответственно. Кратность нарастания антител и доля лиц с 4-кратным и более приростом титра антител (уровень серопротекции) являются важными характеристиками иммунного ответа на вакцинацию. Из результатов следует, что для всех подтипов вируса гриппа наблюдалось увеличение титров антител, значительно превышающее критерий CPMP. Частота сероконверсий к подтипу A/h2N1 составила 57,2 %; для подтипа A/h4N2 – 71,4 %; для типа B – 71,4 %. Кратность прироста титра антител для всех штаммов вируса гриппа превысила критерий CPMP (табл. 2).
Наиболее иммуногенными оказались штамм гриппа А/h2N1 и B, при применении которых уровень серопротекции составил 71,4 и 100 % соответственно. Кратность нарастания антител и доля лиц с 4-кратным и более приростом титра антител (уровень серопротекции) являются важными характеристиками иммунного ответа на вакцинацию. Из результатов следует, что для всех подтипов вируса гриппа наблюдалось увеличение титров антител, значительно превышающее критерий CPMP. Частота сероконверсий к подтипу A/h2N1 составила 57,2 %; для подтипа A/h4N2 – 71,4 %; для типа B – 71,4 %. Кратность прироста титра антител для всех штаммов вируса гриппа превысила критерий CPMP (табл. 2).
Выводы
Вакцинация беременных против гриппа субъединичной очищенной инактивированной вакциной Агриппал S1 не сопровождается развитием общих и местных реакций. Вакцинация способствует уменьшению частоты присоединения респираторных инфекций более чем у 70 % беременных.
У 13 из 14 беременных в поствакцинальном периоде выработался защитный уровень антител, что может способствовать защите рожденных ими детей от вируса гриппа в течение первых месяцев жизни.
1. Dodds L, McNeil SA, Fell DB, et al. Impact of influenza exposure on rates of hospital admissions and physician visits because of respiratory illness among pregnant women. CMAJ 2007;176:463–68.
2. Englund JA. Maternal immunization with inactivated influenza vaccine: rationale and experience.
Vaccine 2003;21:3460–64.
3. CDC. General recommendations on immunization: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR 2006;55 (No. RR-15):32–33.
4. Harris JW. Influenza occurring in pregnant women. JAMA 1919;14:978–80.
5. Hartern TV, Neuzil KM, Shintani AK, et al. Marenal morbidity and perinatal outcomes among pregnant women with respiratory hospitazations during influenza season. Am J Obstet Gynecol 2003;189(6):1705–12.
6. Reuman PD, Ayoub EM, Small PA. Effect of passive maternal antibody on influenza illness in children: a prospective study of influenza A in mother–infant pairs. Pediatr Infect Dis J 1987;6:398–403.
7. Heinonen O, Slone D, Shapiro S. Immunizing agents. Littleton (MA): Publishing Sciences Group; 1977.
Heinonen O, Slone D, Shapiro S. Immunizing agents. Littleton (MA): Publishing Sciences Group; 1977.
8. Yawn DH, Pyeatte JC, Joseph JM, et al. Transplacental transfer of influenza virus. JAMA 1971;216:1022–23.
Возможности специфической иммунопрофилактики гриппа во время беременности с использованием вакцины Аагриппал S1
14 здоровым беременным женщинам в возрасте 18–38 лет на сроке гестации 22–36 недель была проведена вакцинация против гриппа препаратом АГРИППАЛ S1, содержащим следующие штаммы: A/Brisbane/59/2007 (h2Nl), A/Brisbane/10/2007 (h4N2), B/Florida/4/2006. В поствакцинальном периоде общих и местных реакций не отмечено. Через 1 месяц после вакцинации уровень антител в защитных значениях ко всем трем штаммам вируса гриппа регистрировался у 13 из 14 беременных женщин.Таблица 1. Уровень серопротекции после вакцинации беременных препаратом Агриппал S1
Таблица 2. Уровень серопротекции и кратность нарастания титра антител по группам
Уровень серопротекции и кратность нарастания титра антител по группам
Актуальность проблемы
Инфицирование вирусом гриппа во время беременности часто является причиной антенатальной гибели плода и новорожденного (5). В период, предшествующий эпидемии гриппа, увеличивается частота госпитализаций и снижение показателей здоровья беременных женщин (1, 4). Описано существенное увеличение госпитализаций, связанных с болезнями дыхательных путей среди женщин, которые были беременны в течение сезона гриппа в сравнении с годом до зачатия (1). Это свидетельствует о том, что беременность является независимым фактором риска для развития гриппозной инфекции. Перенесенный во время беременности грипп может привести к преждевременным родам и рождению детей с низкой массой тела. Недавно проведенное исследование установило также связь между гриппом у беременных женщин и частотой опухолей мозга или нейробластом у детей.
Физиологические изменения, происходящие при беременности, предрасполагают к развитию серьезных осложнений при любой респираторной инфекции. В послеродовом периоде у женщин резервы легких снижены: потребление кислорода повышается на 15–25%, а функциональная остаточная емкость легких снижается. После 10 недель беременности объем сердечного выброса повышается на 1,5 л/мин, при этом увеличиваются частота сердечных сокращений и ударный объем у матери. Показано, что даже у женщин с неосложненной беременностью пневмония повышает риск преждевременных родов (4, 5).
В послеродовом периоде у женщин резервы легких снижены: потребление кислорода повышается на 15–25%, а функциональная остаточная емкость легких снижается. После 10 недель беременности объем сердечного выброса повышается на 1,5 л/мин, при этом увеличиваются частота сердечных сокращений и ударный объем у матери. Показано, что даже у женщин с неосложненной беременностью пневмония повышает риск преждевременных родов (4, 5).
Новорожденные и дети раннего возраста входят в группу повышенного риска по развитию осложнений и смерти от гриппа, но им противопоказана вакцинация против гриппа до 6 месяцев жизни в связи с тем, что они не могут выработать достаточный уровень защитных антител. Поэтому во время эпидемии гриппа примерно одна треть младенцев оказываются инфицированными вирусом гриппа в течение первых 6 месяцев жизни – в период, когда материнские антитела еще могут осуществлять защиту (1). Было установлено, что более высокие уровни антител против гриппа обнаруживаются в образцах пуповинной крови младенцев, рожденных матерями, которые были привиты в течение беременности, по сравнению с новорожденными от невакцинированных матерей (6).
В зарубежной литературе имеются многочисленные данные, свидетельствующие о передаче материнских антител плоду и новорожденному при вакцинации женщин во время беременности от управляемых инфекций, в том числе гриппа (1, 2). Вакцинация беременных обеспечивает появление у матери специфических антител, которые транспортируются через плаценту к плоду и новорожденному, что создает у ребенка защитный уровень антител к определенным инфекциям.
Однако единодушного мнения по вопросу необходимости плановой вакцинации беременных против гриппа нет. Совещательный комитет по практике иммунизации (ACIP) рекомендует проводить вакцинацию против гриппа здоровых беременных женщин (3). Взвесив все «за» и «против» вакцинации беременных, Американское агентство профилактики и контроля заболеваемости (CDC) и Американский институт акушеров и гинекологов (ACOG) выступают за проведение вакцинации в следующих случаях: 1) при высоком риске контакта с заболевшими; 2) когда инфекция представляет опасность для матери или плода; 3) если вакцинация не принесет вреда. Поскольку ежегодно гриппом болеют 10% взрослых и до 30% детей, избежать контакта с заболеванием практически невозможно. В связи с этим определение соотношения между риском, который несет грипп для беременной женщины и плода, и риском, связанным с применением вакцины, является ключевым моментом при принятии решения относительно иммунизации.
Поскольку ежегодно гриппом болеют 10% взрослых и до 30% детей, избежать контакта с заболеванием практически невозможно. В связи с этим определение соотношения между риском, который несет грипп для беременной женщины и плода, и риском, связанным с применением вакцины, является ключевым моментом при принятии решения относительно иммунизации.
Безопасность инактивированной вакцины против гриппа была доказана при вакцинации беременных на разных сроках гестации (2). При введении в течение 7 лет 2291 дозы инактивированной вакцины против гриппа беременным пациенткам не наблюдалось никакого существенного увеличения неблагоприятных реакций среди матерей или младенцев (7). Проведенные исследования напряженности поствакцинального иммунитета при заборе крови беременных показывают, что иммунный ответ на введение противогриппозных вакцин у беременных не снижен и аналогичен таковому у небеременных женщин (8, 3).
В России проблеме вакцинации беременных против гриппа не уделяется должного внимания как со стороны органов здравоохранения, так и со стороны медицинского персонала. Только сложившаяся в 2009 г. сложная эпидситуация по гриппу А(h2Nl)v и многочисленные случаи летального исхода заставили обратить серьезное внимание на проблему вакцинопрофилактики беременных в соответствии с давно существующими рекомендациями различных медицинских сообществ и ВОЗ. В связи с этим целью настоящего исследования явилась оценка переносимости и иммуногенности субъединичной вакцины против гриппа АГРИППАЛ S1 у беременных.
Только сложившаяся в 2009 г. сложная эпидситуация по гриппу А(h2Nl)v и многочисленные случаи летального исхода заставили обратить серьезное внимание на проблему вакцинопрофилактики беременных в соответствии с давно существующими рекомендациями различных медицинских сообществ и ВОЗ. В связи с этим целью настоящего исследования явилась оценка переносимости и иммуногенности субъединичной вакцины против гриппа АГРИППАЛ S1 у беременных.
Материалы и методы
В период с октября 2008 г. по декабрь 2009 г. было провакцинировано вакциной АГРИППАЛ S1 (вакцина противогриппозная трехвалентная субъединичная очищенная инактивированная, «Новартис вакцинс энд диагностик», Италия) 29 беременных во 2 и 3 триместре беременности в возрасте от 18 до 38 лет.
В 0,5 мл препарата содержатся культивированные на куриных эмбрионах расщепленные вирусы гриппа, представленные штаммами: A/Brisbane/59/2007(h2Nl), A/Brisbane/10/2007(h4N2), B/Florida/4/2006. Вакцина вводилась внутримышечно в дельтовидную мышцу. Перед употреблением содержимое шприца доводилось до комнатной температуры. До вакцинации все женщины подписали информированное согласие. Перед вакцинацией беременную осматривал врач акушер-гинеколог, терапевт, оториноларинголог, иммунолог-аллерголог. Было проведено измерение температуры тела, артериального давления. У женщин, подлежащих вакцинации, беременность не была отягощена гинекологическим статусом и протекала без осложнений.
Вакцина вводилась внутримышечно в дельтовидную мышцу. Перед употреблением содержимое шприца доводилось до комнатной температуры. До вакцинации все женщины подписали информированное согласие. Перед вакцинацией беременную осматривал врач акушер-гинеколог, терапевт, оториноларинголог, иммунолог-аллерголог. Было проведено измерение температуры тела, артериального давления. У женщин, подлежащих вакцинации, беременность не была отягощена гинекологическим статусом и протекала без осложнений.
Уровень противогриппозных антител определяли до и спустя 1 месяц после вакцинации при помощи реакции торможения гемагглютинации (РТГА), как описано в МУ 3.3.2 1758-03. Иммуногенность оценивали в соответствии с требованиями Европейского комитета к противогриппозным вакцинам (CPMP/BWP/214/96), согласно которым должен выполняться по крайней мере один из трех критериев:
- Сероконверсия (процент лиц с четырехкратным приростом титра антител после вакцинации) не менее 40%;
- Серопротекция (процент лиц с защитным титром антител до и через 21–28 дней после вакцинации) не менее 70%;
- Кратность нарастания титров антител по сравнению с фоновой сывороткой не менее 2,5.

Результаты исследования статистически обработаны с использованием t-критерия Стьюдента. Вариационный анализ полученных результатов проводили с применением пакета прикладных программ Statistica 6.0.
Результаты и обсуждения
В поствакцинальном периоде не было отмечено ни местных, ни общих реакций. Беременность протекала физиологически, женщины чувствовали себя хорошо. В течение настоящей беременности до вакцинации у каждой женщины отмечалось от 2 до 4 острых респираторных вирусных инфекций. После вакцинации число эпизодов ОРВИ сократилось и наблюдалось всего у 20,6% беременных. Инфекция протекала в легкой форме, с однократным подъемом температуры от 37 до 37,4 °С, длительность заболевания не превышала 4 дней. Терапия ОРВИ включала орошение зева антисептическим раствором (Мирамистин), очищение полости носа и носоглотки изотоническим стерильным раствором морской воды (Маример, Аквалор, Физиомер, Отривин). С целью повышения местного иммунитета полости рта и зева этим женщинам назначался препарат Лизобакт согласно инструкции по применению. Серологическое обследование с целью оценки иммунологической эффективности вакцинации проводили, сравнивая уровень антител в парных сыворотках, взятых до прививки и на 28-й день после вакцинации. Защитные титры антител ко всем трем штаммам вируса гриппа регистрировались у 13 из 14 вакцинированных (таблицы 1, 2).
Серологическое обследование с целью оценки иммунологической эффективности вакцинации проводили, сравнивая уровень антител в парных сыворотках, взятых до прививки и на 28-й день после вакцинации. Защитные титры антител ко всем трем штаммам вируса гриппа регистрировались у 13 из 14 вакцинированных (таблицы 1, 2).
Подсчеты числа лиц с защитными титрами антител (≥1:40) (серопротекция) показали, что у всех вакцинированных беременных уровень этих антител соответствует критерию CPMP. Наиболее иммуногенными оказались штаммы гриппа A/h2N1 и B, где уровень серопротекции составил 71,4% и 100% соответственно. Кратность нарастания антител и доля лиц с 4-кратным и более приростом титра антител (уровень серопротекций) являются важными характеристиками иммунного ответа на вакцинацию. Из результатов следует, что для всех подтипов вируса гриппа наблюдалось увеличение титров антител значительно превышающее критерий CPMP. Число сероконверсий к подтипу A/h2N1 составило 57,2%; для подтипа A/h4N2 – 71,4%; для типа B – 71,4%. Кратность прироста титра антител для всех штаммов вируса гриппа превышала критерий CPMP (таблица 2).
Кратность прироста титра антител для всех штаммов вируса гриппа превышала критерий CPMP (таблица 2).
Выводы
Вакцинация беременных против гриппа субъединичной очищенной инактивированной вакциной АГРИППАЛ S1 не сопровождается развитием общих и местных реакций.
Вакцинация способствовала уменьшению частоты присоединения респираторных инфекций более чем у 70% беременных.
У 13 из 14 беременных в поствакцинальном периоде выработался защитный уровень антител, что может способствовать защите их младенцев от вируса гриппа в течение первых месяцев жизни.
В данной работе проведен анализ клинико-лабораторных особенностей вакцинации беременных женщин отечественной инактивированной пандемической субъединичной адъювантной моновакциной Гриппол плюс.
Для оценки возможного влияния вакцины на системы метаболического и иммунологического гомеостаза проводилось изучение основных биохимических маркеров крови и уровень ключевых цитокинов в спонтанном и стимулированном тестах в поствакцинальном периоде. Анализ клинической переносимости вакцины против пандемического гриппа штамма
Анализ клинической переносимости вакцины против пандемического гриппа штамма
A/Калифорния/07/2009(h2N1)v МоноГриппол плюс у беременных демонстрирует высокую степень биологической и физиологической безопасности при иммунизации беременных.
Памятка «Профилактика гриппа»
ГРИПП – чрезвычайно заразное инфекционное заболевание, передается воздушно-капельным путем, поражает верхние дыхательные пути, характеризуется симптомами специфической интоксикации и катаром дыхательных путей.
По своей социальной значимости грипп находится на первом месте среди всех болезней человека. Практически каждый человек хотя бы раз в жизни болел гриппом. Это единственное инфекционное заболевание, вызывающее ПАНДЕМИИ. Эпидемии гриппа регистрируются каждый год и поражают до 15% населения земного шара.
Человек, периодически болея гриппом, теряет суммарно около 1 года своей жизни. Средняя продолжительность жизни человека сокращается благодаря гриппу и ОРЗ на несколько лет. Это происходит из-за подрыва сердечно-сосудистой системы. Так, при тяжелом течении гриппа часто появляются необратимые поражения сердечно-сосудистой системы, дыхательных органов, центральной нервной системы, провоцирующие заболевания сердца и сосудов, пневмонии, трахеобронхиты, менингоэнцефалиты.
Это происходит из-за подрыва сердечно-сосудистой системы. Так, при тяжелом течении гриппа часто появляются необратимые поражения сердечно-сосудистой системы, дыхательных органов, центральной нервной системы, провоцирующие заболевания сердца и сосудов, пневмонии, трахеобронхиты, менингоэнцефалиты.
Антивирусные препараты признаны эффективными, однако указывается, что растущая резистентность к ним вирусов, высокая стоимость, побочные эффекты, а также ограниченная доступность этих средств при массовых вспышках делают еще более значимой роль вакцинации как первичной превентивной меры против гриппа.
Ежегодная вакцинация признана основной мерой борьбы с эпидемиями гриппа. Целью вакцинации как массового мероприятия является снижение заболеваемости, особенно тяжелыми формами гриппа (современные вакцины, по оценке ВОЗ, обеспечивают 70–90%–е снижение заболеваемости среди взрослых) и риска серьезных осложнений, в первую очередь у пожилых (по данным ВОЗ – на 70–85%)..jpg)
В России с 2006 г. вакцинация против гриппа включена в Национальный календарь прививок. Вакцинация, или как ее еще называют, прививка – это процесс введения в организм вакцин для искусственного воспроизведения иммунного ответа с целью создания невосприимчивости к инфекции. Вакцины – это препараты, способствующие созданию искусственного специфического иммунитета, приобретенного в процессе прививания и необходимого для защиты организма от конкретного возбудителя болезни.
Для профилактики гриппа применяются живые и инактивированные вакцины, которые относятся к наиболее безопасным.
Инактивированные вакцины – это очищенные вирусы гриппа от чужеродных белков, а живые вакцины — это ослабленные штаммы вируса. Живые вакцины вводятся интраназально, инактивированные – внутримышечно. К живым вакцинам относится вакцина – гриппозная живая интраназальная. К инактивированным вакцинам относятся: Гриппол, Гриппол Плюс, Грипповак, Ваксигрип, Бегривак, Флюарикс, Инфлювак, Агриппал.
Эффективность вакцинации против гриппа
Чем шире охват населения профилактическими прививками, тем меньше процент заболевших, так как создается коллективный иммунитет против инфекционного заболевания.
Эффективность вакцинации и ее приемлемость в качестве рутинной профилактической меры определяется тремя ключевыми факторами:
Совпадение антигенов — сходство циркулирующего вируса гриппа с вирусом, использованным для изготовления вакцины;
Иммуногенность – выработка после введения вакцины антител (титр 1:40 и выше), которые обеспечивают защиту от серьезных и смертельных осложнений гриппа;
Реактогенность — связанные с вакциной побочные эффекты, вызванные действием белков вируса и примесей невирусного происхождения. Вакцины, применяемые для профилактики гриппа слабореактогенны, т.е. осложнений при их введении не наблюдается. Однако возможны прививочные реакции в виде кратковременной температуры до 37,5 С0 в первые 3-е суток, недомогание и уплотнение в месте введении вакцины не более чем в 2% от всех привитых.
Кого в первую очередь необходимо вакцинировать против гриппа
Вакцинация рекомендуется всем лицам старше 6-месячного возраста. Однако существуют категории людей, которым из-за состояния здоровья, профессии и прочих условий вакцинация показана в первую очередь. Эти лица можно разделить на следующие категории:
Группы риска по возможным осложнениям:
— люди преклонного возраста,
— страдающие хроническими соматическими заболеваниями,
— часто болеющие ОРВИ,
— дети дошкольного возраста,
— беременные женщины.
По официальным данным, вакцинация позволяет резко снизить количество осложнений (на 50-60%) и смертельных случаев от гриппа (на 80%) у этих категорий населения.
Группы высокого риска заражения:
— медицинский персонал,
— работники сферы обслуживания,
— служащие учебных заведений,
— воинские контингенты,
— школьники.
Другие группы лиц, кому необходима вакцинация:
— работающие люди, кому болеть невыгодно,
-лица, которые часто посещают территории с высокой заболеваемостью гриппом,
— люди, посещающие тропики в любое время года (так как в тропиках грипп может возникать в течение года),
— люди, посещающие Южное полушарие в период с апреля по сентябрь (так как в Южном полушарии всплеск гриппа наблюдается с апреля по сентябрь).

Почему нужно вакцинировать детей
У детей в возрасте от 6 месяцев до 2 лет очень высока вероятность осложнений при гриппозной инфекции в связи с нарушением функции сердечно-сосудистой и даже центральной нервной систем.
Частота госпитализации детей от 6 месяцев до 2 лет при гриппе из-за возникающих осложнений очень высока и почти такая же, как и у людей с хроническими заболеваниями, отнесенных к группе высокого риска осложнений и смертности при гриппе. По данным исследований у детей этого возраста грипп в 40% случаев осложняется отитом, что нередко приводит к глухоте. Для того, чтобы снизить заболеваемость гриппом детей этого возраста в ряде стран рекомендуют вакцинировать против гриппа не только детей, но также их родителей.
Вакцинация детей от 3 до 17 лет также желательна для формирования популяционного иммунитета, так как дети этого возраста являются основными распространителями гриппозной инфекции, что повышает риск инфицирования родителей и других членов семьи.
Почему нужно вакцинировать здоровых трудоспособных людей
Взрослые здоровые люди заболевают гриппом реже, чем дети, однако и у них нередко возникают послегриппозные осложнения, особенно пневмонии, а ослабленный иммунитет после гриппа может способствовать возникновению различных инфекций. Кроме того, заболевание гриппом работающих людей приводит к серьезному экономическому ущербу, как для самих заболевших (покупка лекарств), так и для учреждений, в которых они работают (за счет потери рабочих дней). Вакцинация против гриппа работающих лиц защищает от заболевания гриппом 80% вакцинированных и существенно снижает экономический ущерб от эпидемий гриппа.
Особенно важно вакцинировать против гриппа лиц определенных профессий, например медицинских работников, работников торговли и общественного транспорта и т.п., которые в результате частых и многочисленных контактов с людьми в процессе работы подвергаются наибольшему риску заболеть гриппом, и, кроме того, сами могут стать источниками инфекции.
Последствия заболевания гриппом в рабочее время
Возникновение проблем со здоровьем работников может иметь множество негативных последствий для компании, в которой они работают. Это связано с невыходом на работу, потерей производительности и даже преждевременной смертью работников.
Основным аспектом проблемы гриппа является невыход на работу: больной, как правило, бывает вынужден оставаться в постели от 3 до 5 дней и утрачивает работоспособность в среднем на 5-10 дней (в случае осложнений – до 1 мес.).
Независимо от мер, принимаемых с целью ограничения экономических последствий, эти проблемы в конечном итоге приводят к потере производительности или увеличению издержек.
Последствия для работодателя
1.Спад производства, который может быть компенсирован только увеличением расходов.
2.Невыполнение планов и обязательств в срок.
3.Для того, чтобы поддержать общую производительность компании, работодатель вынужден находить временную замену отсутствующему сотруднику либо просить его коллег работать сверхурочно, причем и в том, и в другом случае возникают дополнительные затраты.
4.Снижение эффективности труда вследствие повышенной нагрузки на здоровый персонал.
5.Если не будут приняты такие компенсирующие меры, рентабельность компании может пострадать.
Последствия для сотрудника
1.Как минимум финансовые потери выражаются в уменьшении дохода за период утраты трудоспособности.
2.Увеличение расходов на медицинское обслуживание (необходимость консультации врача и приобретение лекарственных средств).
3.Повышенная нагрузка на работе после болезни (необходимо «наверстать упущенное»).
4.Повышение риска потерять работу.
Почему нужно вакцинировать пожилых и людей с хроническими заболеваниями
Пожилые люди, у большинства из которых имеются те или иные хронические заболевания, а также лица любого возраста с хроническими заболеваниями, особенно сердечно-сосудистой и дыхательной систем, страдающие сахарным диабетом, относятся к группе высокого риска осложнений и смертности при гриппе. Именно у этой группы людей чаще всего наблюдаются серьезные осложнения после гриппа, нередко со смертельным исходом. Среди пациентов, страдающих сердечно-сосудистыми и легочными заболеваниями, смертность от гриппа или его осложнения во время эпидемии может достигать 870 человек на 100 000 населения (ВОЗ). Самый высокий риск развития пневмонии у лиц с хроническими заболеваниями легких и сердца, а также циррозом печени. Для людей, больных сахарным диабетом, особенно опасны грипп и его осложнения, включая пневмонию. Фактически, смертность среди больных сахарным диабетом повышается до 5-15% во время эпидемии, и они в шесть раз чаще госпитализируются с осложнениями гриппа, чем люди, не больные диабетом.
Именно у этой группы людей чаще всего наблюдаются серьезные осложнения после гриппа, нередко со смертельным исходом. Среди пациентов, страдающих сердечно-сосудистыми и легочными заболеваниями, смертность от гриппа или его осложнения во время эпидемии может достигать 870 человек на 100 000 населения (ВОЗ). Самый высокий риск развития пневмонии у лиц с хроническими заболеваниями легких и сердца, а также циррозом печени. Для людей, больных сахарным диабетом, особенно опасны грипп и его осложнения, включая пневмонию. Фактически, смертность среди больных сахарным диабетом повышается до 5-15% во время эпидемии, и они в шесть раз чаще госпитализируются с осложнениями гриппа, чем люди, не больные диабетом.
Ежегодная вакцинация лиц этой группы снижает заболеваемость гриппом примерно на 50%, возникновение осложнений на 80%, а смертность на 90%.
Когда нужно вакцинироваться
Согласно статистическим данным, эпидемия гриппа в нашем регионе достигает своего пика в ноябре-декабре. Учитывая то, что достаточная иммунная защита вырабатывается на 2-4 неделе после прививки, оптимальным временем для проведения вакцинации является период с сентября по ноябрь. Высокий титр антител, вызванный прививкой, держится несколько месяцев и начинает снижаться спустя 6 месяцев после вакцинации, поэтому слишком заблаговременная вакцинация не рекомендуется (титр антител может упасть к моменту начала эпидемии).
Учитывая то, что достаточная иммунная защита вырабатывается на 2-4 неделе после прививки, оптимальным временем для проведения вакцинации является период с сентября по ноябрь. Высокий титр антител, вызванный прививкой, держится несколько месяцев и начинает снижаться спустя 6 месяцев после вакцинации, поэтому слишком заблаговременная вакцинация не рекомендуется (титр антител может упасть к моменту начала эпидемии).
Если по каким-то причинам вакцинация не была сделана вовремя, то ее можно сделать и после начала эпидемии гриппа. Широко распространено ошибочное мнение, что после начала эпидемии вакцинация противопоказана. Это имеет отношение к живым противогриппозным вакцинам. Инактивированные вакцины не содержат живых вирусов и поэтому рекомендуются к применению на протяжении всей эпидемии (CDC, Атланта). Однако, если прививка была сделана тогда, когда человек был уже инфицирован вирусом гриппа (но клинические проявления еще не начались), то вакцина может оказаться неэффективной.
Организация вакцинации против гриппа в Удмуртской Республике
В Удмуртской Республике вакцинация детей против гриппа производится вакциной «Гриппол Плюс», взрослого населения — вакцина «Гриппол».
Характеристика вакцин «Гриппол» и «Гриппол плюс»
- Это отечественная противогриппозная полимер–субъединичная тривалентная вакцина.
- Применяется в медицинской практике для вакцинации всех групп населения с 1996 года.
- В состав вакцины входит высокомолекулярным иммуностимулятор Полиоксидоний, который позволяет повысить иммунологическую память, повысить устойчивость организма к другим инфекциям за счет коррекции иммунного статуса.
- Вакцина формирует специфический иммунитет против гриппа в течение 8-12 дней после вакцинации. Иммунитет сохраняется до 12 месяцев, в т.ч. у пожилых лиц. Защитные титры антител к вирусам гриппа после вакцинации лиц разного возраста определяются у 75-92% вакцинированных.
- Решение о вакцинации беременных должно приниматься врачом индивидуально с учетом риска заражения гриппом и возможных осложнений гриппозной инфекции. Наиболее безопасна вакцинация во II и III триместрах.
 В экспериментальных исследованиях установлено, что вакцина Гриппол не обладает эмбриотоксическим и тератогенным действием. Кормление грудью не является противопоказанием для вакцинации.
В экспериментальных исследованиях установлено, что вакцина Гриппол не обладает эмбриотоксическим и тератогенным действием. Кормление грудью не является противопоказанием для вакцинации. - Вакцина может вводиться на фоне базисной терапии основного заболевания.
Вакцина Гриппол может применяться одновременно с другими инактивированными вакцинами.
Вакцинация является наиболее эффективной мерой, обеспечивающей профилактику гриппа и установление контроля над этим заболеванием.
Клинические исследование Грипп, Человек: NBP607, Агриппал S1 — Реестр клинических исследований
Критерии включения:
— Здоровые взрослые люди от 19 лет и старше.
— Субъекты, которые дали письменное согласие на добровольное участие в исследовании и способен соответствовать всем требованиям обучения.
— Если женщина и способна вынашивать детей, тест на беременность в моче отрицательный. пройти обследование и соглашается применять адекватные меры контроля рождаемости через период обучения.
Критерий исключения:
— Субъекты с гиперчувствительностью к любому компоненту вакцины, например, яйцам, курице или куриные продукты.
— Субъекты с нарушением иммунной недостаточности.
— История синдрома Гийена-Барре.
— Тромбоцитопения или нарушение свертываемости крови, противопоказания к внутримышечной вакцинации.
— Субъекты, у которых была лихорадка в течение 24 часов до вакцинации или с лихорадкой заболевание (более 38,0 ℃) в день обследования или острая респираторная инфекция.
— Субъекты, которые получали иммунодепрессанты или иммуномодифицирующие препараты в течение 3 месяцев перед просмотром.
— Субъекты, которые получали продукты крови или иммуноглобулин в течение 3 месяцев до этого. скрининг.
— Субъекты, получившие вакцинацию против гриппа в течение 6 месяцев до скрининг.
— Субъекты, получившие другую вакцинацию в течение месяца до скрининга, или которым была назначена еще одна вакцинация в течение месяца после вакцинации в рамках исследования.
— Субъекты, которые участвовали в другом клиническом исследовании в течение 4 недель до исследования. вакцинация.
— Субъекты, сдавшие кровь в течение недели до вакцинации для исследования, или плановая сдача крови в течение 7 месяцев после вакцинации.
— Субъекты с клинически значимым хроническим заболеванием или злокачественным раком.
— Беременным, кормящим женщинам.
— Любое другое условие, которое, по мнению исследователя, мешает субъекту от участия в исследовании.
Вакцинация против инфекций: виды и вакцины
Услуга вакцинации в медицинском центре Доверие оказывается как для детей, так и для взрослых.
Вирусный гепатит BИнфекционное заболевание печени, обусловленное вирусом. Поражение печени приводит к тяжелым последствиям – циррозу и раку. Инфекция распространена и каждый легко подвергнуться заражению. Вирус гепатита B передается, главным образом через кровь. Вакцины против вируса гепатита В, дают надежную защиту от развития заболевания. Вакцины: Энджерикс В, Комбиотех, Эувакс и др..
Вакцины: Энджерикс В, Комбиотех, Эувакс и др..
Возбудитель туберкулеза – бактерия (Mycobacterium tuberculosis), которая чаще поражает легкие. Туберкулез распространяется от человека человеку по воздуху. Туберкулез, кроме лёгких, может поражать другие органы и ткани человека: глаза, кости, кожу, мочеполовую систему, кишечник. Выделяют открытую, когда микобактерии обнаруживаются в мокроте или другом отделяемом больного, и закрытую, когда микобактерии в отделяемом не определяются, больной не опасен, с точки зрения возможного заражения формы туберкулеза. Вакцины: БЦЖ.
Пневмококковая инфекцияВо многих случаях становится осложнением других инфекций, пример — пневмококковая пневмония после перенесенного гриппа или кори, воспаление среднего уха (отит) у детей, после или на фоне респираторной вирусной инфекции. Вакцины: 7-валентная конъюгированная вакцина Превенар (США), полисахаридная вакцина Пневмо 23 (Франция).
ДифтерияОстрое инфекционное заболевание, вызываемое дифтерийной палочкой (коринебактерия), характеризующееся воспалительным процессом с образованием фибринозной пленки на месте внедрения возбудителя, явлениями общей интоксикации в результате поступления в кровь экзотоксина, обусловливающее тяжелые осложнения по типу инфекционно-токсического шока, миокардита, полиневрита и нефроза. Вакцины: Вакцина АКДС (Россия), Пентаксим (Авентис), Инфарикс (Глаксо), Инфанрикс Гекса (Глаксо).
Вакцины: Вакцина АКДС (Россия), Пентаксим (Авентис), Инфарикс (Глаксо), Инфанрикс Гекса (Глаксо).
Острое инфекционное заболевание, вызывается специфической бактерией Bordetella pertussis. Микроб передается воздушно-капельным путем (при кашле, чихании, разговоре) при тесном общении с больным человеком. Сопровождается воспалительными явлениями в верхних дыхательных путях и приступообразным спазматическим кашлем. Часто заражаются непривитые дети до 5 лет, очень опасен коклюш для детей первого года жизни. Вакцины: Инфанрикс Гекса
СтолбнякИнфекционное заболевание, которое поражает нервную систему. Причина заболевания — бактерия Clostridium tetani. Бактерии попадают в организм даже через царапины и ранки, но опасны глубокие раны. В группе риска главным образом новорожденные, пожилые люди, непривитые люди, рабочие на фермах и наркоманы. Вакцины: вакцина АКДС (АДС), Пентаксим, Инфанрикс, Инфанрикс Гекса.
ПолиомиелитВысоко контагиозное заболевание, вызванное полиовирусом. Он поражает нервную систему и может вызвать паралич или даже смерть за несколько часов. Дикий полиовирус (ДП) попадает в организм через рот с водой или пищей, которые загрязнены фекалиями зараженного лица. Полиомиелит поражает главным образом детей до 5 лет. Вакцины: Пентаксим, Имовакс полио, Вакцина полиомиелитная пероральная 1,2,3 типов, Инфанрикс Гекса, Тетраксим, Полиорикс, Бивак полио.
Он поражает нервную систему и может вызвать паралич или даже смерть за несколько часов. Дикий полиовирус (ДП) попадает в организм через рот с водой или пищей, которые загрязнены фекалиями зараженного лица. Полиомиелит поражает главным образом детей до 5 лет. Вакцины: Пентаксим, Имовакс полио, Вакцина полиомиелитная пероральная 1,2,3 типов, Инфанрикс Гекса, Тетраксим, Полиорикс, Бивак полио.
Тяжелая инфекция детей раннего возраста, до 1 года жизни, проявляется гнойным менингитом, отитом, заболеваниями дыхательных путей (пневмония, бронхит, эпиглоттит), поражением со стороны сердца, суставов и др. Вакцины: Пентаксим, Акт-Хиб, Инфанрикс Гекса, Хиберикс.
КорьИнфекционное заболевание, которое вызывается вирусом кори. Вероятность заражения при контакте с больным около 100%. Чаще болеют дети дошкольного и школьного возраста. Инфекция передается воздушно-капельным путем — при кашле, чихании, разговоре и даже при дыхании. Возможен вертикальный путь передачи кори — от беременной женщины плоду. Вакцины: Приорикс.
Возможен вертикальный путь передачи кори — от беременной женщины плоду. Вакцины: Приорикс.
Высоко заразное острое инфекционное заболевание, вызываемое вирусом краснухи. Часто болеют непривитые дети 2—9 лет. Опасна краснуха в первые 3 месяца беременности — при этом часто развиваются тяжелые врожденные пороки развития ребенка, возможна внутриутробная гибель плода. Пути передачи — воздушно-капельный (при разговоре с больным, поцелуях) и вертикальный (от матери к плоду). Возможен контактный путь заражения — через детские игрушки. Вакцины: Приорикс.
Эпидемический паротитОстрое вирусное заболевание, при котором происходит воспаление слюнных желез. Распространена у детей 5—15 лет. Паротит опасен осложнениями: воспаление поджелудочной (панкреатит) и половых желез. Возможно воспаление щитовидной и других внутренних желез организма, поражение нервной системы в виде менингита или энцефалита. Нередко паротит становится причиной мужского бесплодия. Заражение происходит воздушно-капельным путём (при кашле, чихании, разговоре) от больного человека. Вакцины: Приорикс.
Заражение происходит воздушно-капельным путём (при кашле, чихании, разговоре) от больного человека. Вакцины: Приорикс.
Инфекционное (вирусное) заболевание, поражающее центральную нервную систему и передающееся через клещей. Вакцины: Энцепур, ФСМЕ-Иммун, Вакцина клещевого энцефалита культуральная, Клещ-Э-Вак.
РотавирусИнфекционное заболевание, вызванное ротавирусами. Характеризуется острым началом, симптомами гастроэнтерита или энтерита в сочетании кишечного и респираторного синдромов в начале болезни. Ротавирус инфицирует и повреждает клетки тонкого кишечника. Главный механизм передачи ротавирусов — Фекально-оральный, с участием различных путей и множественных факторов передачи. Эту инфекцию называют «болезнью грязных рук». Вакцины: моновалентная (RV1 – «Ротарикс») и пентавалентная (RV5 – «РотаТек»).
ПапилломавирусИнфекция, передающаяся половым путем, которая вызывается вирусом папилломы человека (ВПЧ). Известно более 100 типов (штаммов) ВПЧ. Разные типы вируса вызывают разные заболевания. ВПЧ 1 типа вызывает подошвенные бородавки, ВПЧ 2, 4 типа – бородавки, ВПЧ 3, 10 типа – плоские бородавки, ВПЧ 6, 11 типа — остроконечные кондиломы. ВПЧ 16, 18, 31, 33 и 35 типа вызывают истинную эрозию и дисплазию шейки матки и увеличивают риск развития рака шейки матки. Зачастую присутствие вируса в организме человека протекает бессимптомно, никак себя не проявляет. Вакцины: Гардасил, Церварикс.
Известно более 100 типов (штаммов) ВПЧ. Разные типы вируса вызывают разные заболевания. ВПЧ 1 типа вызывает подошвенные бородавки, ВПЧ 2, 4 типа – бородавки, ВПЧ 3, 10 типа – плоские бородавки, ВПЧ 6, 11 типа — остроконечные кондиломы. ВПЧ 16, 18, 31, 33 и 35 типа вызывают истинную эрозию и дисплазию шейки матки и увеличивают риск развития рака шейки матки. Зачастую присутствие вируса в организме человека протекает бессимптомно, никак себя не проявляет. Вакцины: Гардасил, Церварикс.
Высокозаразное острое инфекционное заболевание, характерно пузырьковой сыпью. Чаще болеют дети, посещающие детский сад или школу.
Заболевание вызывается вирусом герпеса (герпес-вирус 3-го типа). Вирус передается от больного человека к здоровому воздушно-капельным путем (при разговоре, пребывании в одном помещении). С током воздуха ветрянка распространяется на расстояния (до 20 м). Заражение может произойти от больного опоясывающим лишаем (вызывается той же разновидностью вируса герпеса). Вакцины: Варилрикс, Окавакс.
Вакцины: Варилрикс, Окавакс.
Острая инфекционное заболевание, вызываемое менингококком Neisseria meningitidis, с капельным (аэрозольным) механизмом передачи возбудителя. Клинически характеризуется поражением слизистой оболочки носоглотки (назофарингит), генерализацией в форме специфической септицемии (менингококкемия) и воспалением мягких мозговых оболочек (менингит). Вакцины: Менинго А +С, Менцевакс ACWY, Менактра.
ГриппЗаразное острое вирусное заболевание, характеризующееся симптомами специфической интоксикации и поражением верхних дыхательных путей. Сопровождается резким подъемом температуры тела до 39—40 градусов, ознобом, сильной головной болью, мышечными и суставными болями, кашлем, выделениями из носа. Грипп опасен осложнениями легких, центральной нервной системы. Вирус гриппа бывает трех типов: А, В и С. Наибольшую опасность представляют вирусы гриппа А и В, так как генетический материал постоянно мутирует. Передается воздушно-капельным путем (при разговоре, кашле, чихании) приводит к быстрому заражению большого количества людей. Вакцины: Флюарикс, Агриппал, Ваксигрипп, Гриппол, Инфлювак, Инфлексал.
Передается воздушно-капельным путем (при разговоре, кашле, чихании) приводит к быстрому заражению большого количества людей. Вакцины: Флюарикс, Агриппал, Ваксигрипп, Гриппол, Инфлювак, Инфлексал.
ПОСМОТРЕТЬ ЦЕНЫ √ РАСПИСАНИЕ РАБОТЫ
Записаться на прием, получить консультацию:
+7 (423) 267-61-30; +7 (423) 274-32-22; +7 914-704-32-22.
Записаться на приём он-лайн:
Если остались вопросы, задайте их в форме комментариев ниже↓↓↓
Вакцина против вируса гриппа Agrippal S1 — Seqirus
Нам нужна от вас некоторая информация, прежде чем вы начнете использовать платформу.
Эта информация позволит нам лучше понять, как используется AdisInsight.
Он не требует и не заменяет отдельные учетные записи для входа, которые многие из вас используют для сохранения результатов поиска и создания предупреждений по электронной почте. Защита вашей личной информации важна.
Вот почему AdisInsight собирает минимальный объем информации, необходимой для включения функциональности, отчетности об использовании и связи с вами с информацией об AdisInsight.Для получения дополнительной информации о том, как мы защищаем и обрабатываем вашу личную информацию, пожалуйста, обратитесь к нашему
политика конфиденциальности.
Защита вашей личной информации важна.
Вот почему AdisInsight собирает минимальный объем информации, необходимой для включения функциональности, отчетности об использовании и связи с вами с информацией об AdisInsight.Для получения дополнительной информации о том, как мы защищаем и обрабатываем вашу личную информацию, пожалуйста, обратитесь к нашему
политика конфиденциальности.
Пожалуйста, введите ваш официальный адрес электронной почты
Адрес электронной почты
Страна
Выберите CountryAfghanistanAlbaniaAlgeriaAmerican SamoaAndorraAngolaAnguillaAntarcticaAntigua и BarbudaArgentinaArmeniaArubaAustraliaAustriaAzerbaijanBahamasBahrainBangladeshBarbadosBelarusBelgiumBelizeBeninBermudaBhutanBoliviaBonaire, Синт-Эстатиус и SabaBosnia и HerzegovinaBotswanaBouvet IslandBrazilBritish Индийский океан TerritoryBrunei DarussalamBulgariaBurkina FasoBurundiCambodiaCameroonCanadaCape VerdeCayman IslandsCentral африканских RepublicChadChileChinaChristmas IslandCocos (Килинг) IslandsColombiaComorosCongoCongo, Демократическая Республика theCook IslandsCosta RicaCote D’IvoireCroatiaCubaCuraçaoCyprusCzech RepublicDenmarkDjiboutiDominicaDominican RepublicEcuadorEgyptEl SalvadorEquatorial GuineaEritreaEstoniaEthiopiaFalkland (Мальвинские) острова Фарерские IslandsFijiFinlandFranceFrench GuianaFrench PolynesiaFrench Южные территорииГабонГамбияГрузияГерманияГанаГибралтарГрецияГренландияГренадаГваделупаГуамГватемалаГернсиГвинеяГвинея-БисауГайанаГайтиHeard Island and Mcdonald I slandsHoly Престол (Ватикан) HondurasHong KongHungaryIcelandIndiaIndonesiaIran, Исламская Республика ofIraqIrelandIsle из ManIsraelItalyJamaicaJapanJerseyJordanKazakhstanKenyaKiribatiKorea, Корейская Народно-Демократическая Республика ofKorea, Республика ofKosovoKuwaitKyrgyzstanLao Народная Демократическая RepublicLatviaLebanonLesothoLiberiaLibyan Арабская JamahiriyaLiechtensteinLithuaniaLuxembourgMacaoMacedonia, бывшая югославская Республика ofMadagascarMalawiMalaysiaMaldivesMaliMaltaMarshall IslandsMartiniqueMauritaniaMauritiusMayotteMexicoMicronesia, Федеративные Штаты ofMoldova, Республика ofMonacoMongoliaMontenegroMontserratMoroccoMozambiqueMyanmarNamibiaNauruNepalNetherlandsNew CaledoniaNew ZealandNicaraguaNigerNigeriaNiueNorfolk IslandNorthern Mariana IslandsNorwayOmanPakistanPalauPalestinian край, OccupiedPanamaPapua Новая ГвинеяПарагвайПеруФилиппиныПиткэрнПольшаПортугалияПуэрто-РикоКатарВоссоединениеРумынияРоссийская ФедерацияРуандаСент-БартелемиСент-ЕленаСент-Китс и НевисСент-ЛюсияСент-Мартен (Френк) ч часть) Сен-Пьер и MiquelonSaint Винсент и GrenadinesSamoaSan MarinoSao Томе и PrincipeSaudi ArabiaSenegalSerbiaSeychellesSierra LeoneSingaporeSint Маартен (Голландская часть) SlovakiaSloveniaSolomon IslandsSomaliaSouth AfricaSouth Джорджия и Южные Сандвичевы IslandsSouth SudanSpainSri LankaSudanSurinameSvalbard и Ян MayenSwazilandSwedenSwitzerlandSyrian Arab RepublicTaiwanTajikistanTanzania, Объединенная Республика ofThailandTimor-LesteTogoTokelauTongaTrinidad и TobagoTunisiaTurkeyTurkmenistanTurks и Кайкос IslandsTuvaluUgandaUkraineUnited Араб ЭмиратыВеликобританияМалые отдаленные острова СШАСоединенные Штаты АмерикиУругвайУзбекистанВануатуВенесуэлаВьетнамВиргинские острова, Британские Виргинские острова, СШАСан-Уоллис и Футуна, Западная Сахара, Йемен, Замбия, Зимбабве, Аландские острова. Промышленность
Выберите отрасльБиотехнологииКонсалтингГосударствоИнженерия / ПроизводствоФинансы / ИнвестицииГосударственный институт или агентствоHMO / ClinicHospital (общественная) Больница (другое) Больница (университет или преподаватель) LegalMedia / PublishingMedical SchoolНеправительственная организацияДом для престарелых / Помощь в жизниФармацевтикаЧастный кабинет врача института колледжа (индивидуальная группа) Частный исследовательский кабинет (индивидуальная группа)
Название работы
Выберите должность доцент / лекторБизнес-консультантРазвитие бизнеса, лицензирование или передача технологийБизнес / финансовый аналитик или конкурентная разведкаКлинические вопросы / операции по клиническим испытаниямИнженерГлава академического отдела / факультетаДиректор лаборатории / руководитель библиотеки / Специалист по информационным технологиям Библиотекарь / Библиотекарь метаданных / Библиотекарь по открытым наукам / Библиотека данных по исследованиям Директор / руководитель библиотекиПрофессиональный врач / врачДругиеФармацевтический надзор, нормативные вопросы или качествоPhD СтудентПрезидент / генеральный директор / владелец компанииОсновной исследовательМенеджер по закупкамПрофессор Управление НИОКРПрофессиональный научный сотрудникПродажи и маркетингСтарший научный сотрудник Научный сотрудникСтудентСтажер / научный сотрудник
Промышленность
Выберите отрасльБиотехнологииКонсалтингГосударствоИнженерия / ПроизводствоФинансы / ИнвестицииГосударственный институт или агентствоHMO / ClinicHospital (общественная) Больница (другое) Больница (университет или преподаватель) LegalMedia / PublishingMedical SchoolНеправительственная организацияДом для престарелых / Помощь в жизниФармацевтикаЧастный кабинет врача института колледжа (индивидуальная группа) Частный исследовательский кабинет (индивидуальная группа)
Название работы
Выберите должность доцент / лекторБизнес-консультантРазвитие бизнеса, лицензирование или передача технологийБизнес / финансовый аналитик или конкурентная разведкаКлинические вопросы / операции по клиническим испытаниямИнженерГлава академического отдела / факультетаДиректор лаборатории / руководитель библиотеки / Специалист по информационным технологиям Библиотекарь / Библиотекарь метаданных / Библиотекарь по открытым наукам / Библиотека данных по исследованиям Директор / руководитель библиотекиПрофессиональный врач / врачДругиеФармацевтический надзор, нормативные вопросы или качествоPhD СтудентПрезидент / генеральный директор / владелец компанииОсновной исследовательМенеджер по закупкамПрофессор Управление НИОКРПрофессиональный научный сотрудникПродажи и маркетингСтарший научный сотрудник Научный сотрудникСтудентСтажер / научный сотрудник
Agrippal S1 — вакцина против гриппа, инактивированная (расщепленный вирион) для инъекций
Побочные эффекты:
У детей до 5 лет системные реакции (e. грамм. лихорадка, недомогание, миалгия) могут быть более выраженными.
грамм. лихорадка, недомогание, миалгия) могут быть более выраженными.
Местные реакции: Эритема (покраснение), отек, боль, экхимоз, уплотнение.
Системные реакции: лихорадка, недомогание, дрожь, утомляемость, головная боль, потливость, боль в суставах и мышцах. Эти реакции обычно проходят в течение 1-2 дней без лечения.
Редко: невралгия, парестезия, судороги и преходящая тромбоцитопения. Аллергические реакции, в редких случаях приводящие к шоку. Васкулит с преходящим поражением почек, в очень редких случаях.
Меры предосторожности:
Поскольку эта вакцина содержит следы формальдегида, октоксинола 9 (Triton X-100) и неомицина из-за использования этих веществ во время производства, ее следует использовать с осторожностью у субъектов с гиперчувствительностью к любому из этих веществ.
Пациенты с синдромом Гийена-Барре (СГБ) в анамнезе, начало которого связано со временем с вакцинацией против гриппа, могут подвергаться повышенному риску повторного развития СГБ при введении противогриппозной вакцины.
Использование во время беременности и кормления грудью: Безопасность использования во время беременности не установлена; преимущества вакцинации следует сопоставить с потенциальными рисками.Однако, будучи инактивированной вакциной, она не разделяет теоретических рисков, связанных с живыми вакцинами.
Неизвестно, выделяется ли он с грудным молоком; следовательно, следует соблюдать осторожность при введении вакцины кормящим грудью женщинам. Однако, будучи инактивированной вакциной, она не разделяет теоретических рисков, связанных с живыми вакцинами.
Принцип действия:
Инактивированная вакцина против вируса гриппа повышает иммунитет к вирусу гриппа, индуцируя образование специфических антител.
Индикация:
Профилактика гриппа, вызванного вирусами гриппа типов A и B, у взрослых и детей в возрасте от 6 месяцев и старше.
Противопоказание:
Известные анафилактические реакции гиперчувствительности на яичные белки (яйца или яичные продукты), куриные белки или любой другой компонент вакцины, включая следовые количества (формальдегид, октоксино
l 9 (Triton X-100) и неомицин).
Иммунизацию нельзя проводить во время лихорадки или острого заболевания.
Взаимодействие:
Иммунодепрессанты, противоопухолевые препараты или высокие дозы кортикостероидов могут снизить ответ на вакцины.Повышенный ответ антител с альдеслейкином и аспирином. Возможно усиление антикоагулянтного действия варфарина.
Вакцина против гриппа AGRIPPAL S-1
Вакцина против гриппа AGRIPPAL S-1AGRIPPAL S-1
Вакцина против гриппаСОБСТВЕННОЕ НАИМЕНОВАНИЕ
(и лекарственная форма): AGRIPPAL S-1 ОПИСАНИЕ ЛЕКАРСТВА:
Инактивированная подгруппа Вакцина против гриппа TRATION , типы A и B. НОМЕР:
27/30.1/584
ФАРМАКОЛОГИЧЕСКАЯ КЛАССИФИКАЦИЯ:
A.30.1 Биологические препараты — антиген
СТАТУС РАСПИСАНИЯ:
S2
СОСТАВ:
Agrippal S-1 представляет собой суспензию, содержащую высокоочищенные поверхностные антигены
Вирусы гриппа типов A и B размножаются в культурах клеток куриных эмбрионов и инактивированы
с бетапропиолактоном. Каждая доза 0,5 мл содержит инактивированный вирус гриппа.
субъединицы штаммов и в концентрациях, рекомендуемых в настоящее время для Южной Африки.
ВОЗ и Национальным управлением здравоохранения за 1996 год.
Каждая доза 0,5 мл содержит инактивированный вирус гриппа.
субъединицы штаммов и в концентрациях, рекомендуемых в настоящее время для Южной Африки.
ВОЗ и Национальным управлением здравоохранения за 1996 год.
Эти штаммы могут измениться в последующие годы.
| A / Техас / 36/91 (h2N1) | 15 мкг на дозу 0,5 мл |
| A / Johannesburg / 33/94 (h4N2) -подобный штамм | 15 мкг на дозу 0,5 мл. |
| Б / Харбин / 07/94 | 15 мкг на дозу 0,5 мл. |
| Консервант: тимеросал | 0,05 мг на дозу 0,5 мл. |
ИДЕНТИФИКАЦИЯ:
Слегка мутная бесцветная жидкость в прозрачной стеклянной ампуле или предварительно заполненном шприце.
ФАРМАКОЛОГИЧЕСКОЕ ДЕЙСТВИЕ МЕДИЦИНЫ:
Для активной иммунизации против гриппа.
ПОКАЗАНИЯ:
Для профилактики гриппа у лиц старше 6 месяцев. Вакцинация
рекомендуется для лиц с высоким риском осложнений гриппа и у кого
осложнения могут иметь серьезные последствия, например. пациентов с:
Вакцинация
рекомендуется для лиц с высоким риском осложнений гриппа и у кого
осложнения могут иметь серьезные последствия, например. пациентов с:
| — | хронические респираторные заболевания сердечно-сосудистой системы или почек, |
| – | сахарный диабет и болезнь Аддисона, |
| – | пожилых и ослабленных лиц (особенно госпитализированных.) |
ПРОТИВОПОКАЗАНИЯ:
Противогриппозная вакцина противопоказана при следующих условиях:
| — | Повышенная чувствительность к яйцам, куриным или куриным перьям. |
| – | Любое лихорадочное респираторное заболевание или другая активная лихорадочная инфекция. |
| – | Беременные или планирующие стать
беременна в течение 3 месяцев после вакцинации. |
| – | Пациенты, получающие терапию АКТГ, кортикостероидами, облучение, алкилирующие агенты или антиметаболиты. Это противопоказание не распространяется на пациентов. прием кортикостероидов в качестве заместительной терапии в физиологических дозах, например для Аддисона болезнь. |
ДОЗИРОВКА И НАПРАВЛЕНИЯ ПРИМЕНЕНИЯ:
Перед использованием хорошо взболтать. Ввести внутримышечно или глубоко подкожно.
НЕ ВПРЫСКАТЬ ВНУТРИВЕННО.
От 6 до 35 месяцев : 2 дозы по 0,25 мл каждая, 4 недели
Кроме.
От 3 лет : 2 дозы по 0,5 мл каждая с интервалом 4 недели.
Разовая доза 0,5 мл может быть введена при вакцинации против гриппа в предыдущем
12 месяцев.
Активная иммунизация однократной дозой рекомендуется ежегодно лицам с высоким риском.
ПОБОЧНЫЕ ДЕЙСТВИЯ И ОСОБЫЕ МЕРЫ ПРЕДОСТОРОЖНОСТИ:
В месте прививки возможно легкое покраснение или припухлость. Систематический
проявления (e.грамм. недомогание).
Систематический
проявления (e.грамм. недомогание).
НЕ вводите внутривенно Меры по лечению анафилаксии, включая шприц, содержащий
При введении Агриппала S-1 должно быть доступно 1 мл адреналина (1: 1000).
Вакцинацию следует проводить с осторожностью людям с личным или семейным анамнезом.
аллергии.
ИЗВЕСТНЫЕ СИМПТОМЫ ПЕРЕДОЗИРОВКИ И ОСОБЕННОСТИ ЛЕЧЕНИЯ:
См. «Побочные эффекты и особые меры предосторожности». Лечение симптоматическое и
поддерживающий.
ПРЕДСТАВЛЕНИЕ:
| a) 1 ампула из прозрачного стекла объемом 0,5 мл | c) 1 предварительно заполненный шприц 0,5 мл |
| б) 10 ампул по 0,5 мл из прозрачного стекла | d) 10 предварительно заполненных шприцев по 0,5 мл. |
НАПРАВЛЕНИЯ ХРАНЕНИЯ:
Хранить в холодильнике при температуре от + 2С до + 8С. НЕ ЗАМОРАЖИВАТЬ. Храните в недоступном для детей месте.
Храните в недоступном для детей месте.
НАИМЕНОВАНИЕ И АДРЕС ЗАЯВИТЕЛЯ:
Biovac S.A. c.c., 1 Manchester Road, Wadeville, South Africa.
ДАТА ПУБЛИКАЦИИ ВСТАВКИ НА УПАКОВКУ:
Ноябрь 1995 г.
http://home.intekom.com/pharm/biovac/agrippal.html
Оценка безопасности, переносимости и иммуногенности
d.sindoni et al.
126
группа, получившая адъювант, чем группа
, которая получала неадъювантную вакцину. Эти результаты
приобретают особое значение, если учесть, что иммунная система
слабее у пожилых людей. Следовательно, введение
адъювантной вакцины таким субъектам
явно предпочтительнее, поскольку оно обеспечивает большую и более длительную защиту
.
Ни у одного из
вакцинированных субъектовне было серьезных побочных эффектов, что подтверждает превосходный профиль безопасности
.
Как сообщалось в предыдущих публикациях [15, 19-22], Fluad®
вызывал больше требуемых местных и системных реакций, чем
Agrippal®. Реакции обычно были легкой или умеренной
Реакции обычно были легкой или умеренной
интенсивности и преходящими и не требовали медицинского вмешательства
.
Выводы
Более высокая иммуногенность Fluad® в этом исследовании ena-
дает нам основания сделать вывод, что адъювантная вакцина Fluad®
предпочтительнее неадъювантных составов в стратегиях борьбы с гриппом in-
, нацеленных на пожилых людей. .
Повышенная экспрессия антител, наблюдаемая после введения адъювантной вакцины
, означает, что
пожилых субъектов, чья иммунная реактивность может быть обещанной, не останутся с недостаточным титром антител
для части гриппа. время года.
В соответствии с данными, представленными в национальной и
международной литературе [15, 19-22], наши результаты показывают, что
как местные, так и системные реакции пренебрежимо малы с точки зрения
интенсивности и продолжительности.
n Получено 28 апреля 2009 г. Принято 18 мая 2009 г.
n Для переписки: Донателла Панатто, Департамент здравоохранения —
ces, Университет Генуи, via Pastore 1, 16132 Genoa, Italy — тел.
+39010 3538109 — Факс +39010 3538541 — Электронная почта: panatto @
unige.it
Справочная информация
[1] Hay AJ. Действие адамантаминов против вирусов гриппа A
ингибирование белка ионного канала M2. Семин Вирол
1992; 3: 21-30.
[2] Aoki FY, Macleod MD, Paggiaro P, Carewicz O, El Sawy
A, Wat C, et al. Раннее введение осельтамивира увеличивает эффективность лечения гриппа. J Антимикробная терапия
2003; 51: 123-9.
[3] Hayden FG, Osterhaus AD, Treanor JJ, Fleming DM, Aoki
FY, Nicholson KG, et al. Эффективность и безопасность занамивира, ингибитора нидазы нейрами-
, в лечении инфекций, вызванных вирусом гриппа
.GG167 Исследовательская группа по гриппу. N Engl J Med
1997; 337: 874-80.
[4] Tu Q, Pinto LH, Luo G, Shaughnessy MA, Mullaney D, Kur-
tz S, et al. Характеристика ингибирования активности ионного канала M2
Характеристика ингибирования активности ионного канала M2
с помощью BL-1743, ингибитора вируса гриппа А. Дж. Вирол
1996; 70: 4246-52.
[5] Ансальди Ф., Валле Л., Амициция Д., Банфи Ф., Пасторино Б., Стикки
Л. и др. Лекарственная устойчивость вирусов гриппа А, выделенных в
Италии с 2000 по 2005 г .: появление устойчивых к адамантану
вирусов вызывает беспокойство? Пред. Med Hyg 2006; 47: 1-3.
[6] Смит В., Эндрюс С.Х., Лейдлоу П.П. Вирус, полученный от
больных гриппом. Ланцет 1933; 2: 66-8.
[7] O’Hagan DT. MF59 представляет собой безопасный и мощный вакцинный адъювант, который
усиливает защиту от инфекции вирусом гриппа. Экспорт
рев. Вакцин 2007; 6: 699-710.
[8] Эллоуз Ф., Адам А., Чорбару Р., Лердер Э. Минимальные структурные требования
для адъювантной активности производных бактериального пептидогликана
.Biochem Biophys Res Comm 1974; 59: 1317-25.
[9] Глюк Р.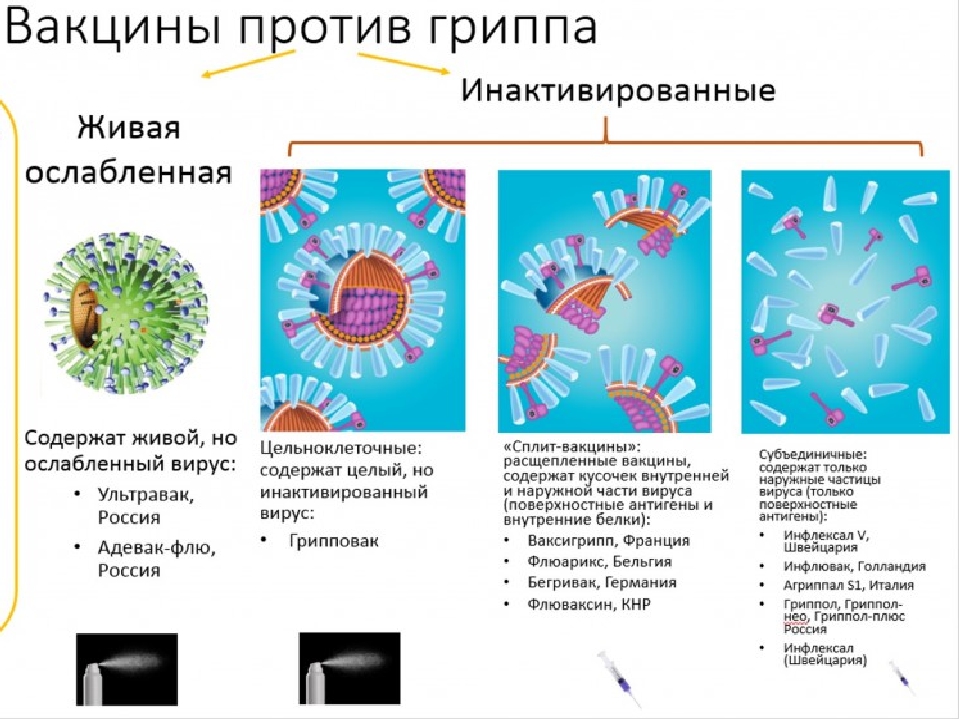 , Вегманн А. Липосомная презентация гриппа anti-
, Вегманн А. Липосомная презентация гриппа anti-
gens. В: Николсон К.Г., Вебстер Р.Г., Хэй А.К., ред. Учебник
гриппа. Оксфорд: Balckwell Science Ltd 1998, стр. 400-409.
[10] Клементс М., Стивенс И. Новые и улучшенные вакцины против гриппа
. В: Levine MM, Woodrow GC, Kaper JB, Cobon GS,
изд. Вакцины нового поколения. 2-е изд. Нью-Йорк, Нью-Йорк: Марсель
Деккер 1997, стр.545-570.
[11] Вуд Дж. М., Кумбс АГА, майор Д., минор П., Дэвис С.С. Поли-
Микрочастицы лактидав качестве адъювантов для парентеральной доставки вакцин против вируса гриппа
. В: Brown LE, Hampson AW, Webster
RG, eds. Варианты борьбы с гриппом III. Амстердам:
Elsevier Science BV 1996, стр. 310-314.
[12] Отт Г., Барчфельд Г.Л., Чернофф Д., Радхакришнан Р., Ван
Хугевест П., Ван Нест Г. MF59: Разработка и оценка
безопасного и мощного адъюванта для человеческих вакцин.В: Powell MF,
Newman MJ, ред. Дизайн вакцины: субъединица и адъювант
. Нью-Йорк: Plenum Press 1995, стр. 277-295.
Нью-Йорк: Plenum Press 1995, стр. 277-295.
[13] Ruf BR, Colberg K, Frick M, Preusche A. Открытое рандомизированное исследование
для сравнения иммуногенности и реактогенности сплит-вакцины против гриппа
с субъединицей вак-
с адъювантом MF59 и виросомой. субъединичная вакцина для пожилых людей. Инфекция
2004; 32: 191-98.
[14] Пуиг-Барбера Дж., Диез-Доминго Дж., Перес Ойос С., Беленгер
Вареа А., Гонсалес Видаль Д.Эффективность вакцины против гриппа MF59-адъю-
в предотвращении неотложной госпитализации
по поводу пневмонии у пожилых людей старше 64 лет. Вакцина
2004; 23: 283-9.
[15] Де Донато С., Гранофф Д., Минутелло М., Лекки Г., Фаччини М.,
Агнелло М. и др. Безопасность и иммуногенность вакцины против гриппа MF59-адъюван-
тед у пожилых людей. Вакцина 1999; 17: 3094-101.
[16] Эдельман Р. Адъюванты для вакцин.Ред. Infect Dis 1980; 2: 370-83.
[17] Van Nest GA, Steimer KS, Haigwood NL, Burke RL, OH
G. Усовершенствованные составы адъювантов для использования с рекомбинантными вакцинами
Усовершенствованные составы адъювантов для использования с рекомбинантными вакцинами
. В: Brown F, Chanock RM, Ginsberg HS,
Lerner RA, ред. Vaccines, Cold Spring Harbor: Cold Spring
Harbor Laboratory Press 1992, стр. 57-62.
[18] Гаспарини Р., Поцци Т., Монтомоли Е., Фрагапане Е., Сенаторе Ф.,
Минутелло М. и др.Повышенная иммуногенность вакцины против гриппа MF59-адъю-
по сравнению с традиционной субъединичной вакциной
для пожилых людей. Eur J Epidemiol 2001; 17: 135-40.
[19] Диван RB, Kasel JA. Вирусы гриппа. В: Lennette EH, Len-
nette DA, Lennette ET, eds. Диагностические процедуры для вирусных,
рахкетных и хламидийных инфекций. 7-е изд. Вашингтон: Ame-
Риканская ассоциация общественного здравоохранения, 1995, стр. 444-445.
[20] Минутелло М., Сенаторе Ф., Чеккинелли Дж., Бьянки М., Андреани
Т, Подда А. и др.Безопасность и иммуногенность вакцины против инактивированного вируса гриппа с субъединицей
в сочетании с адъювантом MF59
у пожилых субъектов, иммунизированных в течение трех последовательных сезонов гриппа
. Vaccine1999; 17: 99-104.
Vaccine1999; 17: 99-104.
[21] Подда А. Адъювантные противогриппозные вакцины с новым адъювантом
vants: опыт применения вакцины с адъювантом MF59. Вакцина
2001; 19: 2673-80.
[22] Фрей С., Польша Г., Перселл С., Подда А.Сравнение sa-
fety, переносимости и иммуногенности вакцины против гриппа
с адъювантом MF59 и вакцины против гриппа без адъюванта у
взрослых людей пожилого возраста. Vaccine 2003; 21: 4234-7.
[23] Durando P, Fenoglio D, Boschini A, Ansaldi F, Icardi G, Stic-
chi L, et al. Безопасность и иммуногенность двух субъединичных вакцин против вируса гриппа
, с адъювантом MF59 или без него, вводимых
взрослым с серопозитивным вирусом иммунодефицита человека 1-го типа и отрицательным -se-
взрослым.Clin Vaccine Immunol 2008; 15: 253-9.
[Сравнительное исследование безопасности и иммуногенности субъединичной вакцины против гриппа и сплит-вакцины]
Для сравнения реактогенности и серологии субъединичной вакцины против гриппа и сплит-вакцины. Было проведено рандомизированное двойное слепое исследование среди детей (возраст от 6 до 12 лет) с целью сравнения безопасности и иммуногенности субъединичной вакцины, инактивированной гриппом (Agrippal, Chiron Vaccines), и сплит-вакцины (Flurix, GSK). .Всего 499 субъектов были вакцинированы и включены в анализ безопасности. Всего 249 испытуемых получили Агриппал, а 250 — Флюрикс. Все субъекты находились под медицинским наблюдением в течение 30 минут, чтобы проверить наличие каких-либо немедленных местных и системных реакций. Записи ежедневных наблюдений собирались в течение 3-х дней после вакцинации. 6,4% случаев с лихорадкой> или = 37,5 ° C были зарегистрированы в группе Flurix, но 2,4% в группе Agrippal, что было значительно меньше, чем в первой группе (P> 0.05). Образцы крови (сыворотки до D0 и после вакцинации D23) были собраны у 224 человек из группы Agrippal и 223 из группы Flurix и проанализированы с помощью анализа ингибирования гемагглютинации (HI). Агриппал и Флурикс индуцировали аналогичную серопротекцию (титр HI> или = 1:40, h2N1 99,6% против 100,0%; h4N2 99,1% против 99,1%) и сероконверсию (увеличение в 4 раза, 95,1% против 97,8%; h4N2 74,5% против 79,8%).
Было проведено рандомизированное двойное слепое исследование среди детей (возраст от 6 до 12 лет) с целью сравнения безопасности и иммуногенности субъединичной вакцины, инактивированной гриппом (Agrippal, Chiron Vaccines), и сплит-вакцины (Flurix, GSK). .Всего 499 субъектов были вакцинированы и включены в анализ безопасности. Всего 249 испытуемых получили Агриппал, а 250 — Флюрикс. Все субъекты находились под медицинским наблюдением в течение 30 минут, чтобы проверить наличие каких-либо немедленных местных и системных реакций. Записи ежедневных наблюдений собирались в течение 3-х дней после вакцинации. 6,4% случаев с лихорадкой> или = 37,5 ° C были зарегистрированы в группе Flurix, но 2,4% в группе Agrippal, что было значительно меньше, чем в первой группе (P> 0.05). Образцы крови (сыворотки до D0 и после вакцинации D23) были собраны у 224 человек из группы Agrippal и 223 из группы Flurix и проанализированы с помощью анализа ингибирования гемагглютинации (HI). Агриппал и Флурикс индуцировали аналогичную серопротекцию (титр HI> или = 1:40, h2N1 99,6% против 100,0%; h4N2 99,1% против 99,1%) и сероконверсию (увеличение в 4 раза, 95,1% против 97,8%; h4N2 74,5% против 79,8%). ) и средний геометрический титр (GMT) увеличиваются (16,0 против 21,0; 5,4 против 6,4) по сравнению с двумя подтипами A. Аналогичный уровень серопротекции (94.2% против 96,4%) и увеличение GMT (21,2 против 18,2) против штамма гриппа B также были замечены в обеих вакцинах. Не было обнаружено существенной разницы в результатах иммунологического анализа между двумя вакцинами (P <0,05). Более низкая скорость сероконверсии против штамма B наблюдалась в группе Agrippal, чем в группе Flurix (91,1% против 97,3%).
С точки зрения безопасности обе вакцины в целом хорошо переносились. Реакция лихорадки наблюдалась реже в группе Агриппала. Обе вакцины вызвали у них эффективный иммунный ответ.
) и средний геометрический титр (GMT) увеличиваются (16,0 против 21,0; 5,4 против 6,4) по сравнению с двумя подтипами A. Аналогичный уровень серопротекции (94.2% против 96,4%) и увеличение GMT (21,2 против 18,2) против штамма гриппа B также были замечены в обеих вакцинах. Не было обнаружено существенной разницы в результатах иммунологического анализа между двумя вакцинами (P <0,05). Более низкая скорость сероконверсии против штамма B наблюдалась в группе Agrippal, чем в группе Flurix (91,1% против 97,3%).
С точки зрения безопасности обе вакцины в целом хорошо переносились. Реакция лихорадки наблюдалась реже в группе Агриппала. Обе вакцины вызвали у них эффективный иммунный ответ.
Италия объявляет Novartis AG о безопасности вакцин FLUAD; Результаты по вакцине против гриппа Agrippal
еще не получены2 декабря 2014 г.
Марк Терри, отдел последних новостей BioSpace.com
Всего через два дня после того, как Итальянское фармацевтическое агентство ( AIFA ) объявило , что оно расследует вакцину от гриппа Novartis , Fluad, в 13 случаях смерти, регулирующее агентство объявило вакцина безопасной.
«Результаты испытаний подтверждают безопасность вакцины против гриппа», — говорится в заявлении AIFA в совместном заявлении с Министерством здравоохранения Италии, — «исключают присутствие эндотоксинов и показывают, что партии соответствуют внешнему виду. и содержание вакцинного антигена вируса гриппа.”
Итальянское агентство исследовало две партии вакцины, 142701 и 143301, после трех смертей и одного случая серьезных побочных эффектов вскоре после вакцинации. В свете огласки стало известно еще около 13 случаев, хотя теперь агентство указывает, что эти случаи не связаны.
Fluad был одобрен в 1997 году и использовался более 65 миллионов раз. В заявлении компании Novartis Базеля, Швейцария, говорится: «Благодаря обширной системе фармаконадзора не было зарегистрировано необычной частоты нежелательных явлений.”
В новостях по теме, прокуратура Турина, Италия, провела расследование другой вакцины от гриппа, произведенной Novartis , Agrippal. Пока нет никаких указаний на то, будет ли расследование продолжено до этого увольнения.
Пока нет никаких указаний на то, будет ли расследование продолжено до этого увольнения.
В конце 2012 года Италия запретила вакцину против гриппа Novartis , включая Fluad, после того, как в некоторых партиях были обнаружены частицы белка. После непродолжительного исследования было обнаружено, что частицы являются частицами яичного белка, ингредиента вакцины.
По крайней мере, один источник, согласно Wall Street Journal , указывает, что AIFA продолжит тестирование Fluad, отметив, что разворот был основан на первоначальном анализе. Novartis опубликовала заявление на выходных, в котором говорится, что «на сегодняшний день причинно-следственная связь с вакциной не установлена». Две подозрительные партии, составляющие 500 000 доз, были распределены только в Италии. Компания Novartis сообщила, что Fluad «часто прописывают пациентам, которые страдают от уже существующих заболеваний и имеют более слабую иммунную систему.К сожалению, среди этой группы пациентов довольно часто случаются серьезные медицинские события и смертельные случаи ».
Из всех смертей, зарегистрированных в ноябре, большинство было старше 80 лет. Указывая, что около 8000 человек ежегодно умирают от гриппа в Италии, AIFA и министерство здравоохранения Италии призвали людей продолжать получать вакцины от гриппа. «На основании этих выводов [агентства] приглашают всех субъектов, особенно тех, кто находится в группе риска [заболеть гриппом], пройти вакцинацию, чтобы избежать осложнений этого инфекционного заболевания.”
Ожидается, что продажи Flucelvax QIV и Flublok QIV будут расти после ожидаемых нормативных разрешений в ЕС в 4 квартале 2020 г.
Дублин, 4 декабря 2020 г. (GLOBE NEWSWIRE) — Отчет «Вакцины от сезонного гриппа» добавлен в Предложение от ResearchAndMarkets.com.
Ожидается, что рынок вакцин против сезонного гриппа в США, Японии и на пяти основных европейских рынках (Франция, Германия, Италия, Испания и Великобритания) продолжит расширяться в течение следующих 10 лет, в основном из-за продолжающегося внедрения вакцины по премиальной цене для пожилых людей, включая четырехвалентные формы Fluzone High-Dose (HD) и Fluad, а также запуск первой в своем классе вакцины с наночастицами с адъювантами, NanoFlu.
Кроме того, старение населения в США, Японии, пяти основных европейских рынках и других развитых странах увеличит количество пациентов в возрастной группе 65 лет, где уровень охвата выше. Кроме того, пандемия COVID-19 вызвала неожиданный всплеск спроса на вакцины против гриппа из-за повышения осведомленности общественности об угрозе, которую представляют респираторные вирусы для пожилых людей и лиц с сопутствующими заболеваниями, а также потенциальной нагрузке на медицинские службы из-за совпадения COVID и волны гриппа.
Три основных производителя доминируют на рынке вакцин против сезонного гриппа, а именно GlaxoSmithKline, Seqirus и Sanofi, с продажами вакцин в 2019 году 684 млн, 799 млн и 2144 млн долларов соответственно. В каждой компании наблюдался рост продаж в 2018 и 2019 годах, при этом GlaxoSmithKline (Fluarix и Flulaval), Sanofi (Fluzone, Fluzone HD, Vaxigrip и Flublok) и Seqirus (Afluria, Agrippal, Fluad и Flucelvax) выросли на 3%, 7%. , и 19% соответственно. Кроме того, AstraZeneca является второстепенным игроком на рынке только с одной продаваемой вакциной, FluMist QIV, которая столкнулась с проблемами после получения отрицательных рекомендаций CHMP в сезонах 2016/17 и 2017/18, а также с производственными проблемами в сезоне 2019/20.
Вакцины, произведенные традиционным методом на основе яиц, включая Афлурию / Агриппал (CSL), Флуарикс / Флулаваль (GlaxoSmithKline) и Флузон / Ваксигрип (Санофи), в совокупности занимают наибольшую долю рынка сезонного гриппа и в основном используются за пределами страны. прибыльная подгруппа пожилых людей, где другие вакцины, продемонстрировавшие более высокую эффективность по сравнению с инактивированными вакцинами со стандартной дозой (Fluzone HD, Fluad, Flucelvax и Flublok), в последние годы набирают все большее распространение.
Поскольку нет никаких различий между инактивированными вакцинами со стандартной дозой в отношении эффективности или безопасности, потребление в первую очередь основывается на маркетинговых и производственных возможностях, а также на процессах конкурентных торгов. Недостатком вакцин на основе яиц являются длительные сроки производства, а вирусные антигены НА склонны к мутациям в процессе репликации на основе яиц. С другой стороны, рекомбинантные вакцины или вакцины на основе клеток имеют более короткие сроки производства и сниженный риск мутаций HA, что приводит к потенциально более высокой защите.
На рынке представлены две вакцины не на основе яиц: рекомбинантная белковая вакцина Санофи Flublok QIV и клеточная вакцина Seqirus Flucelvax QIV, причем последняя имеет более широкую маркировку в США (люди в возрасте от 4 лет по сравнению с возрастом 18 лет для Флублока). Появляется все больше свидетельств того, что производственный процесс без яиц Флублока и Флюсельвакса (и последующее отсутствие мутаций на основе яиц, которые могут привести к продуцированным антигенам НА, отличным от антигенов циркулирующих штаммов) приводит к более высокой реальной эффективности по сравнению с инактивированными яичными антигенами. вакцины, особенно для пожилых людей, где эффективность вакцины неоптимальна.
Ожидается, что продажи Flucelvax QIV и Flublok QIV будут расти после ожидаемых разрешений регулирующих органов в ЕС в четвертом квартале 2020 года. Утверждение Flublok QIV в ЕС позволит вакцине конкурировать с Flucelvax QIV, Fluad QIV и собственной Efluelda QIV Санофи. в сегменте пожилых людей из сезона 2021/22, где все вакцины продемонстрировали повышенную эффективность по сравнению со стандартными инактивированными вакцинами.
Одобрение ЕС в 2020 году Fluad QIV компании CSL и Fluzone HD QIV компании Sanofi открывает значительные возможности для обоих производителей.В Европе Fluad обладает преимуществом первого выхода на рынок и преимуществами от предпочтительной рекомендации для пожилых людей в Великобритании. Исторические проблемы с производственными мощностями не позволили Санофи продавать Fluzone HD за пределами США, но после инвестиций в увеличение производственных мощностей Санофи решила продавать вакцину в других регионах, включая Европу, что представляет собой серьезную угрозу европейскому доминированию Fluad в сегменте пожилых людей. . Учитывая отсутствие прямых испытаний, сравнивающих Fluad и Fluzone HD, конкурентоспособные цены будут иметь первостепенное значение для сохранения своей доли рынка Fluad.
NanoFlu, первая в своем классе вакцина на основе наночастиц, является наиболее передовым активом в разработке гриппа. Novavax рассчитывает подать BLA в четвертом квартале 2020 года с последующим одобрением в середине 2021 года (из-за статуса ускоренной процедуры) и вероятным запуском в сезоне гриппа 2022/23 года. Вакцина будет одобрена на основании исследования фазы III, показывающего лучшую иммуногенность у пожилых людей по сравнению со стандартной дозой Fluzone; однако после утверждения потребуется подтверждающее исследование эффективности, скорее всего, против Fluzone HD.Основываясь на многообещающей иммуногенности против штаммов, гомологичных вакцине, и исторически дрейфующих штаммов, издатель ожидает, что NanoFlu будет сильным конкурентом Fluzone HD, Flublok и Fluad в пожилом сегменте, но многое будет зависеть от результатов подтверждающего исследования эффективности, как считают некоторые врачи. Плательщики / плательщики не захотят сделать вывод, что улучшенная иммуногенность обязательно приведет к улучшению реальной защиты.
Вакцина будет одобрена на основании исследования фазы III, показывающего лучшую иммуногенность у пожилых людей по сравнению со стандартной дозой Fluzone; однако после утверждения потребуется подтверждающее исследование эффективности, скорее всего, против Fluzone HD.Основываясь на многообещающей иммуногенности против штаммов, гомологичных вакцине, и исторически дрейфующих штаммов, издатель ожидает, что NanoFlu будет сильным конкурентом Fluzone HD, Flublok и Fluad в пожилом сегменте, но многое будет зависеть от результатов подтверждающего исследования эффективности, как считают некоторые врачи. Плательщики / плательщики не захотят сделать вывод, что улучшенная иммуногенность обязательно приведет к улучшению реальной защиты.
В области гриппа существует высокая неудовлетворенная потребность в универсальной противогриппозной вакцине, которая обеспечивает защиту от более широкого спектра штаммов, в идеале в течение нескольких сезонов, хотя на данном этапе неясно, как долго продлится какой-либо защитный эффект. Кроме того, универсальные вакцины должны обеспечивать защиту от новых пандемических штаммов, которые могут возникнуть, чего не может обеспечить вакцина против сезонного гриппа.
Кроме того, универсальные вакцины должны обеспечивать защиту от новых пандемических штаммов, которые могут возникнуть, чего не может обеспечить вакцина против сезонного гриппа.
Несмотря на положительные данные об иммуногенности, полученные в ходе клинических испытаний фазы I и фазы II, в октябре 2020 года BiondVax сообщил, что его универсальная вакцина-кандидат M-001 не смогла продемонстрировать эффективность в его ключевом исследовании фазы III. Исходя из этих отрицательных данных и отсутствия у компании финансирования для начала нового испытания, издатель ожидает, что BiondVax вскоре прекратит выпуск вакцины.Хотя в настоящее время вакцина FLU-v от Imutex является наиболее совершенной универсальной вакциной в разработке, прогресс в настоящее время застопорился, пока компания ищет партнера для финансирования основного испытания, и поэтому кажется, что универсальная вакцина выйдет на рынок раньше всего в 2024 году.
Ключевые темы:
ОБЗОР
ИСТОРИЯ ЗАБОЛЕВАНИЙ
- Определение
- Симптомы
- Группы риска
905 905 9COMMEDEED 905 Основные европейские рынки Рекомендации по вакцинации против гриппа, по странам ПРОДАЖИМЫЕ ВАКЦИНЫ ТРУБОПРОВОДНЫЕ ВАКЦИНЫ КЛЮЧЕВЫЕ НОРМАТИВНЫЕ СОБЫТИЯ ВЕРОЯТНОСТЬ УСПЕХА КЛИНИЧЕСКИЙ ИССЛЕДОВАТЕЛЬСКИЙ ЛАНДШАФТ РЫНОЧНАЯ ДИНАМИКА 9ENDS605 КОНСЕНСУСНЫЕ ПРОГНОЗЫ ПОСЛЕДНИЕ СОБЫТИЯ И МНЕНИЕ АНАЛИЗА НЕОБХОДИМЫЕ ПОТРЕБНОСТИ БИБЛИОГРАФИЯ ПРИЛОЖЕНИЕ Для получения дополнительной информации об этом отчете посетите https: // www.05 Завершение перехода на QIV приведет к постепенному росту



 В экспериментальных исследованиях установлено, что вакцина Гриппол не обладает эмбриотоксическим и тератогенным действием. Кормление грудью не является противопоказанием для вакцинации.
В экспериментальных исследованиях установлено, что вакцина Гриппол не обладает эмбриотоксическим и тератогенным действием. Кормление грудью не является противопоказанием для вакцинации.